Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Co原子的价电子排布式为_______ ,Co2+核外3d能级上有_____ 对成对电子。
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是________ 。1 mol配离子中所含σ键的数目为________ ,配位体N3-中心原子的杂化类型为________ 。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是_________________________________________________ 。
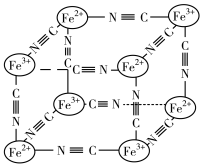
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为________ ,立方体中Fe2+间连接起来形成的空间构型是________ 。K+空缺率(体心中没有K+的占总体心的百分比)为_____________ 。
(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为________ 。
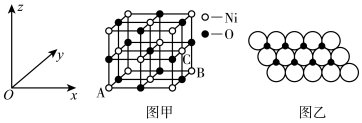
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为________ g(用含a、NA的代数式表示)。
(1)基态Co原子的价电子排布式为
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为

(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为
更新时间:2019-05-27 16:14:19
|
相似题推荐
【推荐1】以ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。请回答:
(1)基态O原子的电子排布式_______ ,其中未成对电子与成对电子个数比________ 。
(2)Zn原子价层电子的轨道表示式___________ ,按照核外电子排布,可将元素周期表划分为5个区,Zn位于___________ 区。
(3)金属Zn能溶于氨水,生成以氮为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为___________ 。
(4)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是___________ 。
(1)基态O原子的电子排布式
(2)Zn原子价层电子的轨道表示式
(3)金属Zn能溶于氨水,生成以氮为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(4)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是
您最近一年使用:0次
【推荐2】完成下列问题:
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为_______ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为_______ 。在四大晶体类型中,GaN属于_______ 晶体。
(2)铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有_______ 的原子或离子
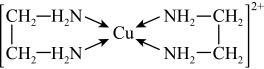
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
①H、N、O三种元素的电负性由大到小的顺序是_______ 。
②SO2分子的空间构型为_______ 。与SnCl4互为等电子体的一种离子的化学式为_______ 。
③乙二胺分子中氮原子轨道的杂化类型为_______ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______ 。
④中所形成的配离子中含有的化学键类型有_______ 。
A.配位键 B.极性键 C.离子键 D.非极性键
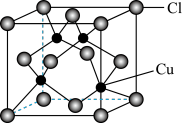
⑤CuCl的晶胞结构如图所示,其中Cl原子的配位数为_______ 。
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为
(2)铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有

(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
①H、N、O三种元素的电负性由大到小的顺序是
②SO2分子的空间构型为
③乙二胺分子中氮原子轨道的杂化类型为
④中所形成的配离子中含有的化学键类型有
A.配位键 B.极性键 C.离子键 D.非极性键
⑤CuCl的晶胞结构如图所示,其中Cl原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】如图甲,铜离子与有机物HA可形成一种螯合物 ,从而萃取水中的铜离子。
,从而萃取水中的铜离子。
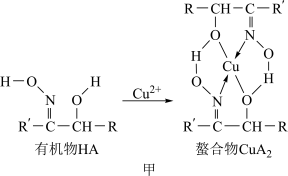
图中的R、R′均为烷烃基,该萃取反应可简单表示为2HA+Cu2+ CuA2+2H+
CuA2+2H+
回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。
(2)有机物HA中,C、N、O三种元素电负性由大到小的顺序是_______ 。
(3)螯合物 中的氮原子杂化方式为
中的氮原子杂化方式为_______ ,氧原子的杂化方式为_______ 。
(4)下列关于螯合物 的说法中,正确的是
的说法中,正确的是_______ (填序号)。
① 中O的配位能力比N强
中O的配位能力比N强
②与 配位的4个原子可能呈平面构型
配位的4个原子可能呈平面构型
③ 既溶于水又溶于有机溶剂
既溶于水又溶于有机溶剂
④每个 分子中含2个氢键、2个π键
分子中含2个氢键、2个π键
(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子的富集及提纯,则反萃取时常加入的试剂是_______ 。
(6)金属铜与铝可形成多种不同的合金,其中一种合金的晶胞如图乙所示,晶胞参数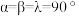 ,
, ,
,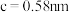 ,按图乙中阴影面进行投影得到图丙。
,按图乙中阴影面进行投影得到图丙。
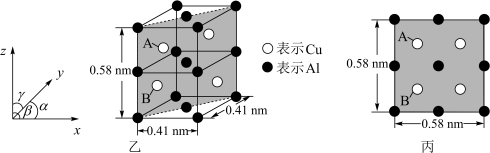
该晶体的化学式为_______ ,密度为_______  (结果保留两位有效数字)。
(结果保留两位有效数字)。
 ,从而萃取水中的铜离子。
,从而萃取水中的铜离子。
图中的R、R′均为烷烃基,该萃取反应可简单表示为2HA+Cu2+
 CuA2+2H+
CuA2+2H+回答下列问题:
(1)基态铜原子的价电子排布式为
(2)有机物HA中,C、N、O三种元素电负性由大到小的顺序是
(3)螯合物
 中的氮原子杂化方式为
中的氮原子杂化方式为(4)下列关于螯合物
 的说法中,正确的是
的说法中,正确的是①
 中O的配位能力比N强
中O的配位能力比N强②与
 配位的4个原子可能呈平面构型
配位的4个原子可能呈平面构型③
 既溶于水又溶于有机溶剂
既溶于水又溶于有机溶剂④每个
 分子中含2个氢键、2个π键
分子中含2个氢键、2个π键(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子的富集及提纯,则反萃取时常加入的试剂是
(6)金属铜与铝可形成多种不同的合金,其中一种合金的晶胞如图乙所示,晶胞参数
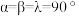 ,
, ,
,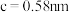 ,按图乙中阴影面进行投影得到图丙。
,按图乙中阴影面进行投影得到图丙。
该晶体的化学式为
 (结果保留两位有效数字)。
(结果保留两位有效数字)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为___________ ,装置B的作用是___________ 。
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是___________ ,实验时需要向C中通入稍过量的SO2,目的是___________ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为___________ ,判断反应完成的现象是___________ 。
(4)连二硫酸结构式为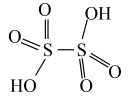 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上_________ 孤电子对(填“有”或“无”),已知甲磺酸的结构简式为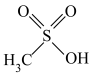 ,连二硫酸H-O的极性
,连二硫酸H-O的极性________ 甲磺酸H-O的极性(填“大于”“小于”或“等于”)。
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
(4)连二硫酸结构式为
 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上 ,连二硫酸H-O的极性
,连二硫酸H-O的极性
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】照相底片定影时,常用定影液硫代硫酸钠( )溶解未曝光的溴化银(
)溶解未曝光的溴化银( ),生成含
),生成含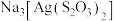 的废定影液再向其中加入
的废定影液再向其中加入 使
使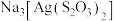 中的银转化为
中的银转化为 ,使定影液再生。将
,使定影液再生。将 在高温下转化为Ag,达到回收银的目的。回答下列问题:
在高温下转化为Ag,达到回收银的目的。回答下列问题:
(1)元素周期表中,铜、银、金位于同一副族相邻周期,则基态银原子的最外层电子排布式为__________________ 。
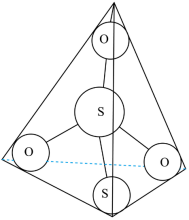
(2) 离子结构如图所示,其中心硫原子的杂化方式为
离子结构如图所示,其中心硫原子的杂化方式为___________ 。基态S原子中,核外电子占据的最高能级的符号是__________ ,占据最高能级电子的电子云轮廓图为________ 形。
(3)写出 溶于
溶于 溶液反应的离子方程式
溶液反应的离子方程式______ 。 中存在的作用力有离子键、共价键、
中存在的作用力有离子键、共价键、__________ 。
(4)在空气中灼烧 生成
生成 和
和 ,
, 分子的空间构型为
分子的空间构型为__________ 。分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数n代表参与形成大
键的原子数n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则
),则 中的大
中的大 键应表示为
键应表示为_________ 。
(5) 的键角小于
的键角小于 的键角,原因是
的键角,原因是_________________ 。
(6)用X射线衍射法可测定阿伏加 德罗常数。由金的X射线衍射图象可知金的晶胞属于面心立方晶胞。若金原子的半径为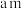 ,金的密度为
,金的密度为 ,摩尔质量为
,摩尔质量为 ,列出计算阿伏加 德罗常数的算式
,列出计算阿伏加 德罗常数的算式_________ (用含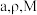 的表达式表示)。
的表达式表示)。
 )溶解未曝光的溴化银(
)溶解未曝光的溴化银( ),生成含
),生成含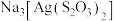 的废定影液再向其中加入
的废定影液再向其中加入 使
使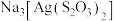 中的银转化为
中的银转化为 ,使定影液再生。将
,使定影液再生。将 在高温下转化为Ag,达到回收银的目的。回答下列问题:
在高温下转化为Ag,达到回收银的目的。回答下列问题:
(1)元素周期表中,铜、银、金位于同一副族相邻周期,则基态银原子的最外层电子排布式为
(2)
 离子结构如图所示,其中心硫原子的杂化方式为
离子结构如图所示,其中心硫原子的杂化方式为(3)写出
 溶于
溶于 溶液反应的离子方程式
溶液反应的离子方程式 中存在的作用力有离子键、共价键、
中存在的作用力有离子键、共价键、(4)在空气中灼烧
 生成
生成 和
和 ,
, 分子的空间构型为
分子的空间构型为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数n代表参与形成大
键的原子数n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则
),则 中的大
中的大 键应表示为
键应表示为(5)
 的键角小于
的键角小于 的键角,原因是
的键角,原因是(6)用X射线衍射法可测定阿伏加 德罗常数。由金的X射线衍射图象可知金的晶胞属于面心立方晶胞。若金原子的半径为
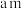 ,金的密度为
,金的密度为 ,摩尔质量为
,摩尔质量为 ,列出计算阿伏加 德罗常数的算式
,列出计算阿伏加 德罗常数的算式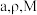 的表达式表示)。
的表达式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】氮和磷元素的单质和化合物在农药生产及工业制造业等领域用途非常广泛,请根据提示回答下列问题:
(1)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为___ ,其中的阴离子的空间构型为___ 。
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N4H44+两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H44+中含有___ 个σ键。
(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因___ 。
(4)P4S3可用于制造火柴,其分子结构如图1所示。
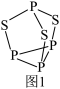
①P4S3分子中硫原子的杂化轨道类型为___ 。
②每个P4S3分子中含孤电子对的数目为___ 。
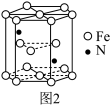
(5)某种磁性氮化铁的晶胞结构如图2所示,该化合物的化学式为___ 。若晶胞底边长为anm,高为cnm,则这种磁性氮化铁的晶体密度为__ g·cm−3(用含a、c和NA的式子表示)
(6)高温超导材料,是具有高临界转变温度(Te)能在液氮温度条件下工作的超导材料。高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为[Ar]__ ;化合物中,稀土元素最常见的化合价是+3,但也有少数的稀土元素可以显示+4价,观察下面四种稀土元素的电离能数据,判断最有可能显示+4价的稀土元素是___ (填元素符号)。
几种稀土元素的电离能(单位:kJ·mol−1)
(1)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N4H44+两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H44+中含有
(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因
(4)P4S3可用于制造火柴,其分子结构如图1所示。

①P4S3分子中硫原子的杂化轨道类型为
②每个P4S3分子中含孤电子对的数目为
(5)某种磁性氮化铁的晶胞结构如图2所示,该化合物的化学式为

(6)高温超导材料,是具有高临界转变温度(Te)能在液氮温度条件下工作的超导材料。高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为[Ar]
几种稀土元素的电离能(单位:kJ·mol−1)
| 元素 | I1 | I2 | I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 7019 |
| Y(铱) | 616 | 1181 | 1980 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3547 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】Ti、Fe、Cu、Ni为过渡金属元素,在工业生产中有重要的应用.

(1)①常温下Fe(CO)5呈液态,熔点为-20.5℃,沸点为103℃.据此可以判断其晶体为_________ 晶体,Fe(CO)5中铁的化合价为0,则该物质中含有的化学键类型有______ (填字母).
A 离子键 B 极性共价键 C 非极性共价键 D 配位键
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为________ ,配体H2O中O原子的杂化方式为________ .
③NiO、FeO的晶体结构类型均与氧化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO_______ FeO(填“<”或“>”).
(2)Cu、N两元素形成某种化合物的晶胞结构如图(灰色球表示Cu原子),已知紧邻的白球与灰球之间的距离为a cm,该晶胞的密度为________ g•cm-3.

(1)①常温下Fe(CO)5呈液态,熔点为-20.5℃,沸点为103℃.据此可以判断其晶体为
A 离子键 B 极性共价键 C 非极性共价键 D 配位键
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为
③NiO、FeO的晶体结构类型均与氧化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
(2)Cu、N两元素形成某种化合物的晶胞结构如图(灰色球表示Cu原子),已知紧邻的白球与灰球之间的距离为a cm,该晶胞的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】回答下列问题:
I、有下列实验:

(1)向蓝色沉淀中继续添加氨水,沉淀溶解,写出沉淀溶解的离子方程式为_______ 。
(2)该深蓝色晶体的化学式为_______ ,溶剂X可以是_______ (填名称),
(3)该实验能说明 、
、 与
与 结合能力的强到弱的顺序是
结合能力的强到弱的顺序是_______ 。
(4)下列有关化学实验“操作→现象→解释”均正确的是_______ 。
(5)高温下, 比CuO稳定的原因是
比CuO稳定的原因是_______ 。
Ⅱ、 在水溶液中与
在水溶液中与 发生如下反应:
发生如下反应:
(6)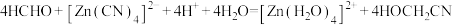 。在
。在 中含有
中含有 键的数目为
键的数目为_______ 。
(7) 中
中 与
与 的形成配位键。不考虑空间构型,
的形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为_______ ,此配离子中,配体为_______ ,中心离子为_______ 。
(8)独立的 分子中H—N—H的键角为107°,
分子中H—N—H的键角为107°, 离子中H—N—H的键角
离子中H—N—H的键角_______ 107°(填“大于”、“小于”或“等于”)。
I、有下列实验:

(1)向蓝色沉淀中继续添加氨水,沉淀溶解,写出沉淀溶解的离子方程式为
(2)该深蓝色晶体的化学式为
(3)该实验能说明
 、
、 与
与 结合能力的强到弱的顺序是
结合能力的强到弱的顺序是(4)下列有关化学实验“操作→现象→解释”均正确的是
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 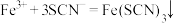 |
| B | 向由0.1molCrCl3·6H2O配成的溶液加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知 的配位数为6.则CrCl3·6H2O的化学式可表示为 的配位数为6.则CrCl3·6H2O的化学式可表示为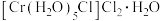 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加l0滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在: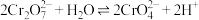 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
 比CuO稳定的原因是
比CuO稳定的原因是Ⅱ、
 在水溶液中与
在水溶液中与 发生如下反应:
发生如下反应:(6)
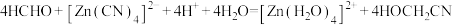 。在
。在 中含有
中含有 键的数目为
键的数目为(7)
 中
中 与
与 的形成配位键。不考虑空间构型,
的形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为(8)独立的
 分子中H—N—H的键角为107°,
分子中H—N—H的键角为107°, 离子中H—N—H的键角
离子中H—N—H的键角
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】“天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。75号元素铼Re,熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅、锗等矿物中。
(1)基态Ge原子的核外电子排布式为____ 。
(2)在元素周期表中,铼与锰在同族,铼在元素周期表中的位置是____ ;铼易形成高配位数的化合物如Re2(CO)10,该配合物中由____ (填名称)原子提供孤对电子与铼成键。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3•3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为____ ;CO 的空间结构为
的空间结构为____ 。
(4)甲苯比 的熔、沸点
的熔、沸点____ (填“高”或“低”),原因是____ 。
(5)三氧化铼晶胞如图所示(小黑点代表Re或O原子),摩尔质量为Mg•mol-1,晶胞密度为bg•cm-3,铼原子配位数为____ ,铼原子填在了氧原子围成的____ (填“四面体”“立方体”或“八面体”)空隙中,该晶胞的空间利用率为____ (铼的原子半径为rRepm,氧原子半径为ropm,设NA为阿伏加德罗常数的值,列出计算式)。

(1)基态Ge原子的核外电子排布式为
(2)在元素周期表中,铼与锰在同族,铼在元素周期表中的位置是
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3•3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为
 的空间结构为
的空间结构为(4)甲苯比
 的熔、沸点
的熔、沸点(5)三氧化铼晶胞如图所示(小黑点代表Re或O原子),摩尔质量为Mg•mol-1,晶胞密度为bg•cm-3,铼原子配位数为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】钴广泛应用于电池、合金等领域。以含钴废料(主要含 和
和 ,还含有
,还含有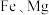 等元素以及
等元素以及 、碳、有机物)为原料制备钴的流程如下:
、碳、有机物)为原料制备钴的流程如下: 难溶于水。
难溶于水。
② (焦亚硫酸钠)常作食品抗氧化剂。
(焦亚硫酸钠)常作食品抗氧化剂。
③常温下,部分氢氧化物沉淀的 如表所示。
如表所示。
④氧化性: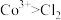 。
。
回答下列问题:
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是___________ (用离子方程式表示)。
(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与 的关系如图2所示(不考虑
的关系如图2所示(不考虑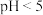 的情况)。
的情况)。___________ 。在此条件下,实际消耗的双氧水远大于理论用量,可能的原因是___________ 。
(3)有人认为“除镁”可以通过调节 代替加入
代替加入 ,请你评价:
,请你评价:___________ (判断是否可行,简述理由)。
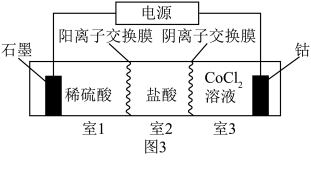
(4)工业上也可利用图3装置实现制备 。
。___________ 。生成 时,室1中溶液理论上减少
时,室1中溶液理论上减少___________ g。
②相较于直接电解 溶液,图3中“三室两膜”装置突出优点是
溶液,图3中“三室两膜”装置突出优点是___________ 。(从绿色化学角度分析)
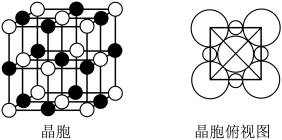
(5)钴的一种氧化物的晶胞如图所示,已知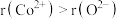 。钴离子的配位数为
。钴离子的配位数为___________ ,晶胞中原子空间利用率为___________ 。[用含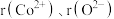 和π的代数式表示,已知:晶胞中原子空间利用率
和π的代数式表示,已知:晶胞中原子空间利用率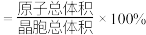 ]
]
 和
和 ,还含有
,还含有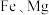 等元素以及
等元素以及 、碳、有机物)为原料制备钴的流程如下:
、碳、有机物)为原料制备钴的流程如下: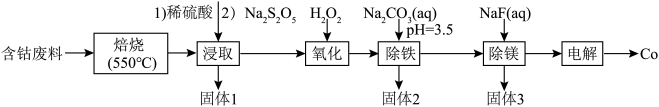
 难溶于水。
难溶于水。②
 (焦亚硫酸钠)常作食品抗氧化剂。
(焦亚硫酸钠)常作食品抗氧化剂。③常温下,部分氢氧化物沉淀的
 如表所示。
如表所示。 |  |  |  |  | |
开始沉淀 | 0.3 | 2.7 | 7.6 | 7.2 | 9.6 |
完全沉淀 | 1.2 | 3.2 | 9.6 | 9.2 | 11.1 |
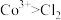 。
。回答下列问题:
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是
(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与
 的关系如图2所示(不考虑
的关系如图2所示(不考虑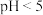 的情况)。
的情况)。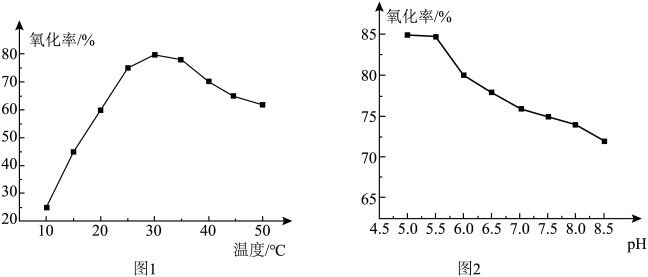
(3)有人认为“除镁”可以通过调节
 代替加入
代替加入 ,请你评价:
,请你评价:(4)工业上也可利用图3装置实现制备
 。
。
 时,室1中溶液理论上减少
时,室1中溶液理论上减少②相较于直接电解
 溶液,图3中“三室两膜”装置突出优点是
溶液,图3中“三室两膜”装置突出优点是(5)钴的一种氧化物的晶胞如图所示,已知
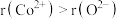 。钴离子的配位数为
。钴离子的配位数为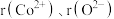 和π的代数式表示,已知:晶胞中原子空间利用率
和π的代数式表示,已知:晶胞中原子空间利用率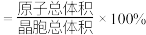 ]
]
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】镧系为元素周期表中第ⅢB族、原子序数为57〜71的元素。
(1)镝Dy)的基态原子电子排布式为[Xe] 4f106s2,画出镝(Dy)原子价层电子排布图:____________ .
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为____________ 。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是_____ 填元素名称)。
几种镧系元素的电离能(单位:kJ∙mol-1)
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为_______ (用元素符号表示)。
②画出氨的最简单气态氢化物水溶液中存在的氢键:________ (任写一种)。
③元素Al也有类似成键情况,气态氯化铝分子表示为((AlCl3)2,分子中A1原子杂化方式为_____ ,分子中所含化学键类型有 _______ (填字母)。
a.离子键 b.极性键 c.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中错原子位于面心和顶点,则PrO2 (二氧化镨)的晶胞中有_____ 个氧原子;已知晶胞参数为apm,密度为ρg∙cm-3,NA=_______ (用含a、ρ的代数式表示)。
(1)镝Dy)的基态原子电子排布式为[Xe] 4f106s2,画出镝(Dy)原子价层电子排布图:
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是
几种镧系元素的电离能(单位:kJ∙mol-1)
| 元素 | Ⅰ1 | Ⅰ2 | Ⅰ3 | Ⅰ4 |
| Yb (镱) | 604 | 1217 | 4494 | 5014 |
| Lu (镥) | 532 | 1390 | 4111 | 4987 |
| La (镧) | 538 | 1067 | 1850 | 5419 |
| Ce (铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为
②画出氨的最简单气态氢化物水溶液中存在的氢键:
③元素Al也有类似成键情况,气态氯化铝分子表示为((AlCl3)2,分子中A1原子杂化方式为
a.离子键 b.极性键 c.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中错原子位于面心和顶点,则PrO2 (二氧化镨)的晶胞中有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】过渡金属及其化合物在生产、生活中有重要的应用。回答下列问题:
(1)基态 的价电子轨道表达式为
的价电子轨道表达式为_______ 。
(2)一种含 的催化剂
的催化剂 能催化乙烯、丙烯等的聚合,其结构如图甲所示。
能催化乙烯、丙烯等的聚合,其结构如图甲所示。 中,
中, 原子的杂化类型有
原子的杂化类型有_______ , 中含有的作用力类型有
中含有的作用力类型有_______ (填序号),非金属元素电负性由大到小的顺序为_______ 。
A.π键 B. 氢键 C. 配位键 D.σ键 E. 离子键

(3)分子中的大 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数。
键的电子数。 离子由
离子由 、
、 、
、 三种元素组成,其结构如图乙所示,则
三种元素组成,其结构如图乙所示,则 离子中的大
离子中的大 键应表示为
键应表示为_______ 。
(4) 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的 的结构式为
的结构式为_______ 。
(5)黄铜矿是提炼铜的主要原料,其主要成分的晶胞结构如图。

① 周围距离最近的
周围距离最近的 数为
数为_______ 。
②黄铜矿炼铜过程中会产生硫的氧化物废气,其中 分子空间构型为
分子空间构型为_______ ,与 互为等电子体的阴离子有
互为等电子体的阴离子有_______ (写一种即可)。
③该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,设 为阿伏加德罗常数的值,请计算该晶体的密度
为阿伏加德罗常数的值,请计算该晶体的密度
_______  。
。
(1)基态
 的价电子轨道表达式为
的价电子轨道表达式为(2)一种含
 的催化剂
的催化剂 能催化乙烯、丙烯等的聚合,其结构如图甲所示。
能催化乙烯、丙烯等的聚合,其结构如图甲所示。 中,
中, 原子的杂化类型有
原子的杂化类型有 中含有的作用力类型有
中含有的作用力类型有A.π键 B. 氢键 C. 配位键 D.σ键 E. 离子键

(3)分子中的大
 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数。
键的电子数。 离子由
离子由 、
、 、
、 三种元素组成,其结构如图乙所示,则
三种元素组成,其结构如图乙所示,则 离子中的大
离子中的大 键应表示为
键应表示为(4)
 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的 的结构式为
的结构式为(5)黄铜矿是提炼铜的主要原料,其主要成分的晶胞结构如图。

①
 周围距离最近的
周围距离最近的 数为
数为②黄铜矿炼铜过程中会产生硫的氧化物废气,其中
 分子空间构型为
分子空间构型为 互为等电子体的阴离子有
互为等电子体的阴离子有③该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,设
 为阿伏加德罗常数的值,请计算该晶体的密度
为阿伏加德罗常数的值,请计算该晶体的密度
 。
。
您最近一年使用:0次



