连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为___________ ,装置B的作用是___________ 。
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是___________ ,实验时需要向C中通入稍过量的SO2,目的是___________ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为___________ ,判断反应完成的现象是___________ 。
(4)连二硫酸结构式为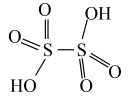 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上_________ 孤电子对(填“有”或“无”),已知甲磺酸的结构简式为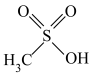 ,连二硫酸H-O的极性
,连二硫酸H-O的极性________ 甲磺酸H-O的极性(填“大于”“小于”或“等于”)。
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
(4)连二硫酸结构式为
 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上 ,连二硫酸H-O的极性
,连二硫酸H-O的极性
更新时间:2024-02-01 17:22:06
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】MBTH(熔点 )常用于检测室内空气中甲醛(HCHO)含量,结构如图所示:
)常用于检测室内空气中甲醛(HCHO)含量,结构如图所示:

回答下列问题
(1)甲醛所含元素的电负性由小到大的顺序为___________ (用元素符号表示),基态 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为___________
(2)甲醛分子的VSEPR模型为___________ ,甲醛沸点(19.5℃)低于甲醇沸点(64.8℃),其原因是___________ 。
(3)甲醛能和一些极性试剂如 进行加成反应(氢原子加到电负性相对大的氧原子上),该反应的化学方程式为
进行加成反应(氢原子加到电负性相对大的氧原子上),该反应的化学方程式为___________ 。
(4)MBTH分子中碳原子采取的杂化类型为___________ ,基态 原子核外电子有
原子核外电子有___________ 种空间运动状态(原子轨道)。
(5) 与
与 的比较,熔点更高的是
的比较,熔点更高的是___________ 。
(6)下列现代分析手段中,可用于检测MBTH的分子结构的是___________。
 )常用于检测室内空气中甲醛(HCHO)含量,结构如图所示:
)常用于检测室内空气中甲醛(HCHO)含量,结构如图所示:
回答下列问题
(1)甲醛所含元素的电负性由小到大的顺序为
 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为(2)甲醛分子的VSEPR模型为
(3)甲醛能和一些极性试剂如
 进行加成反应(氢原子加到电负性相对大的氧原子上),该反应的化学方程式为
进行加成反应(氢原子加到电负性相对大的氧原子上),该反应的化学方程式为(4)MBTH分子中碳原子采取的杂化类型为
 原子核外电子有
原子核外电子有(5)
 与
与 的比较,熔点更高的是
的比较,熔点更高的是(6)下列现代分析手段中,可用于检测MBTH的分子结构的是___________。
| A.X射线衍射 | B.原子光谱 | C.元素分析 | D.红外光谱 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】卤化物、氢化物在科研和生活中占有重要地位。回答下列问题:
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
(2) 的VSEPR模型名称为
的VSEPR模型名称为____________ 。
(3)二氟氮烯(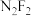 )分子中,每个原子均满足八电子稳定结构,则
)分子中,每个原子均满足八电子稳定结构,则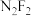 的结构式为
的结构式为____________ 。
(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键的键能( )如下表:
)如下表:
A-A键的键能依次降低的原因是____________________________________________________________ 。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺( )半导体作为吸光材料。
)半导体作为吸光材料。 的晶胞如图所示,其中
的晶胞如图所示,其中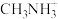 位于顶点(大空心球)位置。已知
位于顶点(大空心球)位置。已知 晶体的晶胞参数为a nm,阿伏加德罗常数的值为
晶体的晶胞参数为a nm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为____________  。(用最简式表达)
。(用最简式表达)

(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
A. | B. | C. | D. |
 的VSEPR模型名称为
的VSEPR模型名称为(3)二氟氮烯(
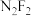 )分子中,每个原子均满足八电子稳定结构,则
)分子中,每个原子均满足八电子稳定结构,则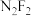 的结构式为
的结构式为(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键的键能(
 )如下表:
)如下表:
|
| HO-OH |
346 | 247 | 207 |
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(
 )半导体作为吸光材料。
)半导体作为吸光材料。 的晶胞如图所示,其中
的晶胞如图所示,其中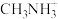 位于顶点(大空心球)位置。已知
位于顶点(大空心球)位置。已知 晶体的晶胞参数为a nm,阿伏加德罗常数的值为
晶体的晶胞参数为a nm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为 。(用最简式表达)
。(用最简式表达)
您最近一年使用:0次
【推荐3】研究物质的微观结构,有助于理解物质变化规律和本质。
(1)氨气的水溶液中存在多种氢键,任意表示出其中一种:_______ 。
(2)CO与N2分子结构相似,下表是二者的键能数据( )。
)。
①1个CO分子中含有的π键数目是个_______ 个。
②结合数据比较活泼性:CO_______ N2(填“>”或“<”)。
(3)利用 可以合成化工原料
可以合成化工原料 、配合物
、配合物 等。
等。
① 分子结构式为:
分子结构式为: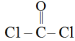 ,该分子空间结构为
,该分子空间结构为_______ 。
② 常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断
常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断 晶体属于
晶体属于___ 晶体。
③ 在一定条件下发生分解反应:
在一定条件下发生分解反应: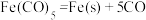 ,反应过程中,断裂的化学键只有配位键,形成的化学键是
,反应过程中,断裂的化学键只有配位键,形成的化学键是___ 。
(4)羧酸的酸性可用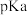 的大小衡量
的大小衡量 ,
,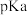 越小,酸性越强,相同温度下的三种酸:①乙酸(CH3COOH)②氯乙酸(CH2ClCOOH)③三氟乙酸(CF3COOH)的
越小,酸性越强,相同温度下的三种酸:①乙酸(CH3COOH)②氯乙酸(CH2ClCOOH)③三氟乙酸(CF3COOH)的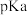 由小到大的顺序
由小到大的顺序___ (填序号)。
(5)过硫酸(分子式:H2S2O8;结构式: )为无色晶体,易溶于水,在热水中易水解。下列说法正确的是
)为无色晶体,易溶于水,在热水中易水解。下列说法正确的是___ (填序号)。
a.过硫酸属于共价化合物
b.过硫酸分子中含有与过氧化氢分子中相同的化学键
c.过硫酸分子可看作2个硫酸分子脱去1个水分子
(1)氨气的水溶液中存在多种氢键,任意表示出其中一种:
(2)CO与N2分子结构相似,下表是二者的键能数据(
 )。
)。| 分子 | C-O | C=O | C≡O | 分子 | N-N | N=N | N≡N |
| CO | 351 | 745 | 1071 | N2 | 193 | 418 | 946 |
②结合数据比较活泼性:CO
(3)利用
 可以合成化工原料
可以合成化工原料 、配合物
、配合物 等。
等。①
 分子结构式为:
分子结构式为: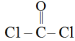 ,该分子空间结构为
,该分子空间结构为②
 常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断
常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断 晶体属于
晶体属于③
 在一定条件下发生分解反应:
在一定条件下发生分解反应: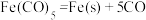 ,反应过程中,断裂的化学键只有配位键,形成的化学键是
,反应过程中,断裂的化学键只有配位键,形成的化学键是(4)羧酸的酸性可用
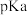 的大小衡量
的大小衡量 ,
,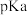 越小,酸性越强,相同温度下的三种酸:①乙酸(CH3COOH)②氯乙酸(CH2ClCOOH)③三氟乙酸(CF3COOH)的
越小,酸性越强,相同温度下的三种酸:①乙酸(CH3COOH)②氯乙酸(CH2ClCOOH)③三氟乙酸(CF3COOH)的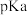 由小到大的顺序
由小到大的顺序(5)过硫酸(分子式:H2S2O8;结构式:
 )为无色晶体,易溶于水,在热水中易水解。下列说法正确的是
)为无色晶体,易溶于水,在热水中易水解。下列说法正确的是a.过硫酸属于共价化合物
b.过硫酸分子中含有与过氧化氢分子中相同的化学键
c.过硫酸分子可看作2个硫酸分子脱去1个水分子
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】钴具有广泛用途,其正三价化合物具有强氧化性。利用含钴废料(主要成分为CoO、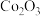 、
、 ,还含有少量的铝箔)制备碳酸钴和碳酸锂的工艺流程如下图所示:
,还含有少量的铝箔)制备碳酸钴和碳酸锂的工艺流程如下图所示:
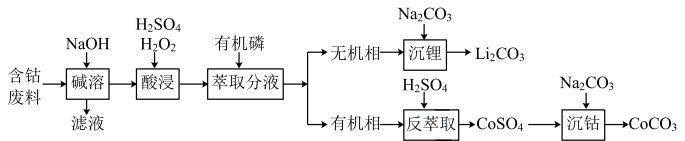
(1)碱溶过程中要保持强制通风,原因是_______ 。
(2)酸浸过程中 发生反应的方程式
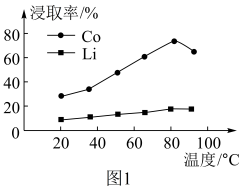
发生反应的方程式_______ ,Co、Li元素的浸出率随温度的变化如图1所示,酸浸时最适宜温度是_______ ℃,在生产过程中不能用盐酸没出错的主要原因是_______ 。
(3)在萃取分液的过程中,把分液漏斗玻璃塞上的凹槽对准漏斗口上的小孔,其目的是_______ 。
(4)沉锂过程中有关物质的溶解度随温度变化如图2所示,获取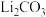 的操作依次是
的操作依次是_______ 、洗涤、干燥。
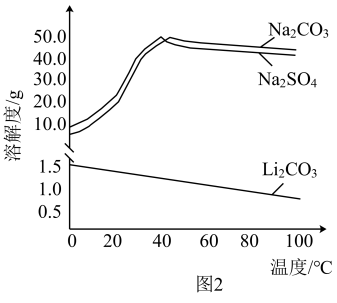
(5)在空气中煅烧 生成钴的氧化物和
生成钴的氧化物和 ,测得充分煅烧后固体质量为36.15g,
,测得充分煅烧后固体质量为36.15g, 的体积为10.08L(标准状况),则该钴氧化物的化学式为
的体积为10.08L(标准状况),则该钴氧化物的化学式为_______ 。
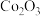 、
、 ,还含有少量的铝箔)制备碳酸钴和碳酸锂的工艺流程如下图所示:
,还含有少量的铝箔)制备碳酸钴和碳酸锂的工艺流程如下图所示:
(1)碱溶过程中要保持强制通风,原因是
(2)酸浸过程中
 发生反应的方程式
发生反应的方程式
(3)在萃取分液的过程中,把分液漏斗玻璃塞上的凹槽对准漏斗口上的小孔,其目的是
(4)沉锂过程中有关物质的溶解度随温度变化如图2所示,获取
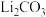 的操作依次是
的操作依次是
(5)在空气中煅烧
 生成钴的氧化物和
生成钴的氧化物和 ,测得充分煅烧后固体质量为36.15g,
,测得充分煅烧后固体质量为36.15g, 的体积为10.08L(标准状况),则该钴氧化物的化学式为
的体积为10.08L(标准状况),则该钴氧化物的化学式为
您最近一年使用:0次
【推荐2】三氯化六氨合钴 是一种重要的化工原料。利用含钴废料(含少量Fe、Al等杂质)制取
是一种重要的化工原料。利用含钴废料(含少量Fe、Al等杂质)制取 的工艺流程如图所示:
的工艺流程如图所示: 、
、 、
、 、
、 等。
等。
②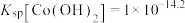
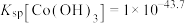 、
、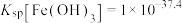
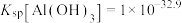
已知:溶液中金属离子物质的量浓度低于 时,可认为沉淀完全。
时,可认为沉淀完全。
③ 具有较强还原性。
具有较强还原性。
回答下列问题:
(1)制备 。
。
“除杂”过程中加 调节pH后会生成两种沉淀,同时得到含
调节pH后会生成两种沉淀,同时得到含 的滤液,调节pH的范围为
的滤液,调节pH的范围为___________ 。
(2)制备 。
。
①“混合”过程中需先将 ,
, 溶液混合,然后再加入活性炭,
溶液混合,然后再加入活性炭, 的作用是
的作用是___________ 。
②“氧化”过程应先加入___________ (选填“氨水”或“双氧水”),原因是___________ 。
③生成 的离子方程式为
的离子方程式为___________ 。
(3)分离提纯。将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到 晶体。该过程中加入浓盐酸的目的是
晶体。该过程中加入浓盐酸的目的是___________ 。
(4)含量测定。通过碘量法可测定产品中的钴元素的含量。称取0.10g产品加入稍过量的NaOH溶液并加热,将Co完全转化为难溶的 ,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的KI和2~3滴淀粉溶液,再用
,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的KI和2~3滴淀粉溶液,再用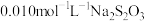 溶液滴定(反应原理:
溶液滴定(反应原理: 、
、
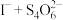 ),达到滴定终点时消耗
),达到滴定终点时消耗 溶液24.00mL,则产品中钴元素的含量
溶液24.00mL,则产品中钴元素的含量___________ 。
 是一种重要的化工原料。利用含钴废料(含少量Fe、Al等杂质)制取
是一种重要的化工原料。利用含钴废料(含少量Fe、Al等杂质)制取 的工艺流程如图所示:
的工艺流程如图所示: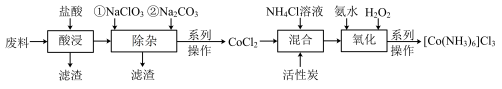
 、
、 、
、 、
、 等。
等。②
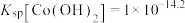
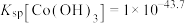 、
、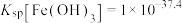
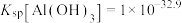
已知:溶液中金属离子物质的量浓度低于
 时,可认为沉淀完全。
时,可认为沉淀完全。③
 具有较强还原性。
具有较强还原性。回答下列问题:
(1)制备
 。
。“除杂”过程中加
 调节pH后会生成两种沉淀,同时得到含
调节pH后会生成两种沉淀,同时得到含 的滤液,调节pH的范围为
的滤液,调节pH的范围为(2)制备
 。
。①“混合”过程中需先将
 ,
, 溶液混合,然后再加入活性炭,
溶液混合,然后再加入活性炭, 的作用是
的作用是②“氧化”过程应先加入
③生成
 的离子方程式为
的离子方程式为(3)分离提纯。将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到
 晶体。该过程中加入浓盐酸的目的是
晶体。该过程中加入浓盐酸的目的是(4)含量测定。通过碘量法可测定产品中的钴元素的含量。称取0.10g产品加入稍过量的NaOH溶液并加热,将Co完全转化为难溶的
 ,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的KI和2~3滴淀粉溶液,再用
,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的KI和2~3滴淀粉溶液,再用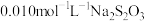 溶液滴定(反应原理:
溶液滴定(反应原理: 、
、
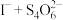 ),达到滴定终点时消耗
),达到滴定终点时消耗 溶液24.00mL,则产品中钴元素的含量
溶液24.00mL,则产品中钴元素的含量
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】硫酸四氨合锌[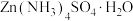 ]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:
]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:
在仪器X内加入1.5g 、2.5g尿素(
、2.5g尿素(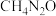 ,过量)和5.0
,过量)和5.0 乙二醇(
乙二醇( )及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题:
)及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题:_________ ;尿素易溶于水的原因是_______________ 。
(2)仪器X的名称是_________ ;冷凝管中进水口是_________ (填“a”或“b”)。
(3)尿素与水反应的化学方程式为_________ ;乙二醇的作用是_________ 。
(4)加热“回流”时温度不宜高于120℃,其原因是_________ 。
(5)烘干产品时宜选择的加热方式为_________ (填标号)。
a.酒精灯直接加热 b.沙浴 c.水浴加热
(6)用乙醇洗涤产品,而不用水洗涤,利用了乙醇的性质是_________ 。
(7)若最终得到1.976g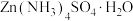 ,则产率为
,则产率为_________ (保留3位有效数字)。
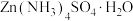 ]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:
]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:在仪器X内加入1.5g
 、2.5g尿素(
、2.5g尿素(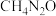 ,过量)和5.0
,过量)和5.0 乙二醇(
乙二醇( )及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题:
)及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题: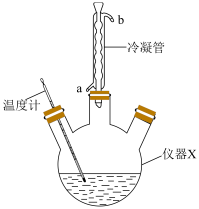
(2)仪器X的名称是
(3)尿素与水反应的化学方程式为
(4)加热“回流”时温度不宜高于120℃,其原因是
(5)烘干产品时宜选择的加热方式为
a.酒精灯直接加热 b.沙浴 c.水浴加热
(6)用乙醇洗涤产品,而不用水洗涤,利用了乙醇的性质是
(7)若最终得到1.976g
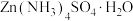 ,则产率为
,则产率为
您最近一年使用:0次





