100 mL 6 mol·L-1的H2SO4跟过量锌粉反应,在一定温度下,要想减缓反应进行的速率,但又不影响生成的氢气的总量,可向反应物中加入适量的( )
| A.硫酸钠固体 | B.稀盐酸 |
| C.硫酸钾溶液 | D.硝酸钾溶液 |
更新时间:2019-06-28 22:22:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,容积一定的密闭容器中进行以下反应:2X(g)+Y(g) Z(g)+W(s) ΔH>0,下列叙述中正确的是
Z(g)+W(s) ΔH>0,下列叙述中正确的是
 Z(g)+W(s) ΔH>0,下列叙述中正确的是
Z(g)+W(s) ΔH>0,下列叙述中正确的是| A.升高温度,可增大活化分子的百分数,有效碰撞次数增多 |
| B.加入少量W,逆反应速率增大 |
| C.增大压强,正反应速率增大,逆反应速率减小 |
| D.在容器中通入X气体,正反应反应速率增大,逆反应速率减小,所以V正>V逆 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在带有活塞的密闭容器中发生如下反应:Fe2O3(s)+3H2(g) 2Fe(s)+3H2O(g),采取下列措施不能改变反应速率的是
2Fe(s)+3H2O(g),采取下列措施不能改变反应速率的是
 2Fe(s)+3H2O(g),采取下列措施不能改变反应速率的是
2Fe(s)+3H2O(g),采取下列措施不能改变反应速率的是| A.将容器的体积减小一半 | B.保持容器容积不变,增加H2通入量 |
| C.保持容器内压强不变,充入N2 | D.增加Fe的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在催化剂a和催化剂b的作用下,氮气分子参与反应的有关反应历程如图所示。下列说法正确的是
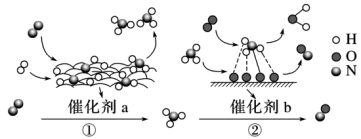

| A.过程①氮气会完全转化为氨气 |
| B.过程②中参加反应的分子,化学键未完全断裂 |
| C.过程①的反应若在恒压条件下充入氩气,反应速率不变 |
| D.温度不变,缩小体积,过程①②的反应速率均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知反应:2NO(g)+Br2(g) 2NOBr(g) △H=-akJ•mol-1(a>0),其反应机理如下
2NOBr(g) △H=-akJ•mol-1(a>0),其反应机理如下
①NO(g)+Br2(g) NOBr2(g) 快
NOBr2(g) 快
②NO(g)+NOBr2(g) 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法不正确的是
 2NOBr(g) △H=-akJ•mol-1(a>0),其反应机理如下
2NOBr(g) △H=-akJ•mol-1(a>0),其反应机理如下①NO(g)+Br2(g)
 NOBr2(g) 快
NOBr2(g) 快②NO(g)+NOBr2(g)
 2NOBr(g) 慢
2NOBr(g) 慢下列有关该反应的说法不正确的是
| A.温度对反应②的速率影响更大 |
| B.NOBr2是该反应的催化剂 |
| C.正反应的活化能比逆反应的活化能小akJ•mol-1 |
| D.增大Br2(g)浓度能增加单位体积内的活化分子数目,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】100mL0.01mol·L-1的稀盐酸与足量铁粉反应,反应速率太慢,为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O②加NaOH固体③滴入几滴浓盐酸④加CuO固体⑤加NaCl固体⑥滴加几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol·L-1的盐酸
①加H2O②加NaOH固体③滴入几滴浓盐酸④加CuO固体⑤加NaCl固体⑥滴加几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol·L-1的盐酸
| A.⑥⑦⑧ | B.③⑦⑧ | C.①②⑤ | D.③④⑦⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,进行下列实验操作,能达到预期目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 在滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 证明CO 在溶液中存在水解平衡 在溶液中存在水解平衡 |
| B | 分别测定盐酸和醋酸溶液的pH | 证明相同温度下,HCl的电离程度大于CH3COOH |
| C | 向0.1mol•L-1的稀硫酸中加入ag锌粉,向0.4mol•L-1的稀硫酸中加入ag锌粒 | 探究固体表面积对反应速率的影响 |
| D | 向两支装有4mL0.0lmol•L-1KMnO4酸性溶液的试管中分别加入2rnL0.04mol•L-1H2C2O4(草酸)溶液、2mL0.2mol•L-1H2C2O4(草酸)溶液 | 探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学课外小组的同学通过实验探究温度和浓度对反应速率的影响。实验原理及方案:在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生反应生成碘,反应原理是2IO +5SO
+5SO +2H+=I2+5SO
+2H+=I2+5SO +H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
下列判断正确的是
 +5SO
+5SO +2H+=I2+5SO
+2H+=I2+5SO +H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。| 实验序号 | 0.01 mol·L-1 KIO3酸性溶液(含淀粉)的体积/mL | 0.01 mol·L-1 Na2SO3溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 | V1 | 5 | t1 |
| ② | 5 | 5 | 40 | 25 | t2 |
| ③ | 5 | V2 | 35 | 25 | t3 |
| A.实验①③中V1=10,V2=40 |
| B.最先出现蓝色的一组是实验③ |
| C.开始出现蓝色的时间:t1<t2 |
| D.探究温度对化学反应速率的影响应该选择实验①③ |
您最近一年使用:0次