关于 溶液的叙述正确的是
溶液的叙述正确的是
 溶液的叙述正确的是
溶液的叙述正确的是A.加入盐酸,抑制 水解 水解 | B.升温,抑制 水解 水解 |
C.浓度越大, 水解程度越大 水解程度越大 | D.将溶液蒸干可得 固体 固体 |
更新时间:2019-08-22 18:46:11
|
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐1】醋酸溶液中存在电离平衡CH3COOH⇌H++CH3COO-,下列叙述不正确的是:
| A.升高温度,平衡正向移动 |
| B.25℃时,欲使醋酸溶液pH和电离常数Ka都减小,可加入少量冰醋酸 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.往0.10mol·L-1的CH3COOH溶液中加水稀释,促进CH3COOH的电离 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】下列有关盐类水解的说法不正确的是
| A.盐类水解过程破坏了纯水的电离平衡 |
| B.盐类水解反应是酸碱中和反应的逆反应 |
| C.盐类水解的结果使溶液不一定呈中性 |
| D.Na2S溶液中c(Na+)是c(S2-)的2倍 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】下列说法不正确的是
| A.可以用勒夏特列原理解释实验室中常用排饱和食盐水的方法收集氯气 |
| B.热的碳酸钠溶液可用于去除餐具的油污 |
| C.燃烧木柴时,采用较细木材并将木柴架空 |
| D.农业上将草木灰和铵态氮肥混合使用,可以增强肥效 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】化学与生产和生活密切相关,下列说法正确的是
| A.“光化学烟雾”、“硝酸型酸雨”的形成与氮氧化物有关 |
| B.二氧化硅具有半导体性质,用于制造光导纤维 |
| C.明矾具有消毒杀菌的作用,常用作净水剂 |
D. 、 、 都是优良的净水剂 都是优良的净水剂 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】在一定条件下,Na2S溶液存在水解平衡;S2-+H2O HS-+OH-。下列说法正确的是
HS-+OH-。下列说法正确的是
 HS-+OH-。下列说法正确的是
HS-+OH-。下列说法正确的是A.升高温度, 增大 增大 |
| B.加入CuSO4固体,HS-浓度增大 |
| C.稀释溶液,水解平衡常数增大 |
| D.加入NaOH固体,溶液pH减小 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】能够使CH3COONa溶液pH增大且水解程度也增大的条件是
| A.加水 | B.升温 | C.加压 | D.加CH3COONa固体 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】下列盐在水溶液中不能发生水解的是( )
| A.NH4NO3 | B.CH3COOK | C.NaCl | D.FeSO4 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列图示与对应的叙述不相符的是
 | 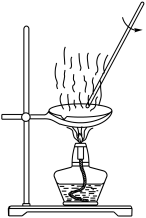 |  |  |
| A.银氨溶液的制备 | B.蒸干 溶液得 溶液得 固体 固体 | C.铁片上镀铜 | D. 的收集 的收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



