下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

下列说法不正确的是( )

下列说法不正确的是( )
A.通过计算,可知系统(Ⅰ)制备氢气的热化学方程式为:H2O(l)= H2(g)+1/2O2(g) ΔH = 286 kJ· mol-1 |
| B.通过计算,可知系统(Ⅱ)制备氢气的热化学方程式为:H2S(g)=H2(g)+S(s) ΔH =20kJ·mol-1 |
C.若反应H2(g)+1/2O2(g)=H2O(g) ΔH = -a kJ · mol-1, 则a>286  |
| D.制得等量H2所需能量较少的是热化学硫碘循环硫化氢分解法 |
18-19高三·浙江·阶段练习 查看更多[4]
浙江省稽阳2018-2019学年高三联考化学试题江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(B)(已下线)课时28 焓变与热化学方程式-2022年高考化学一轮复习小题多维练(全国通用)山西省太原市2019-2020学年高二上学期期中测评化学试题
更新时间:2019-08-11 10:56:50
|
相似题推荐
单选题
|
较难
(0.4)
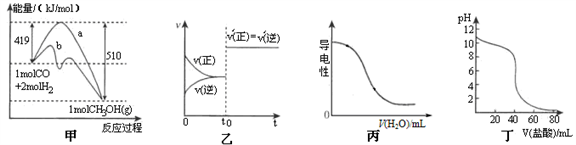
【推荐1】下列图示与对应的叙述相符合的是
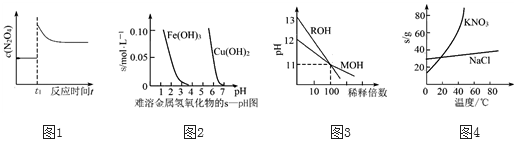

A.图1表示平衡2NO2(g) N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
| B.图2表示除去CuSO4溶液中的Fe3+可采用加入CuO调节溶液pH到4~5 |
| C.图3表示MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化,则碱性:MOH>ROH |
| D.图4为KNO3和NaCl溶解度曲线,若除去NaCl中少量的KNO3,可在较高温度下制得浓溶液后,再冷却结晶、过滤、洗涤、干燥得纯净NaCl |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定条件下,Na2CO3溶液中存在如下平衡:CO +H2O
+H2O HCO
HCO +OH-,下列说法正确的是( )
+OH-,下列说法正确的是( )
 +H2O
+H2O HCO
HCO +OH-,下列说法正确的是( )
+OH-,下列说法正确的是( )A.稀释溶液,平衡正向移动,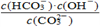 增大 增大 |
| B.通入CO2,平衡逆向移动,溶液pH减小 |
| C.加入NaOH固体,平衡逆向移动,pH减小 |
D.升高温度, 增大 增大 |
您最近一年使用:0次
【推荐1】将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一,煤转化为水煤气的主要反应为 。
。 、
、 和
和 完全燃烧的热化学方程式分别如下:
完全燃烧的热化学方程式分别如下:
①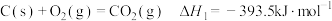
②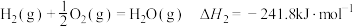
③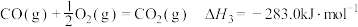
下列说法不正确的是
 。
。 、
、 和
和 完全燃烧的热化学方程式分别如下:
完全燃烧的热化学方程式分别如下:①
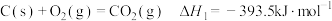
②
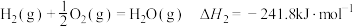
③
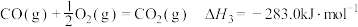
下列说法不正确的是
A.制取水煤气的热化学方程式为 |
B.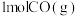 和 和 完全燃烧放出的热量之和比 完全燃烧放出的热量之和比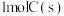 完全燃烧放出的热量多 完全燃烧放出的热量多 |
| C.煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量 |
| D.将煤转化为水煤气再燃烧的整个过程中放出的热量,与直接燃烧等质量的煤放出的热量相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列有关说法正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) △H=akJ/mol、2C(s)+ O2(g)=2CO(g) △H=bkJ/mol,则a>b |
| B.25℃时,溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于l0-14 |
| C.一种锂电池,总反应为4Li+2SOCl2=4LiCl+S+SO2↑,放电时,每产生22.4 L的SO2,就有4 mole-从电池负极流出 |
| D.根据HClO的Ka=3.0×l0-8, H2CO3的Ka1=4.3×l0-7,Ka2=5.6×l0-11,可推测相同状况下,等浓度的NaClO与Na2CO3溶液中,pH前者小于后者 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】意大利罗马大学的Fulvio Cacace等人获得极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,断裂1molN≡N吸收942kJ热量.根据以上信息和数据,下列说法正确的是
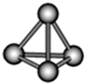

| A.N4属于一种新型的化合物,与N2互为同素异形体 |
| B.N4的沸点比白磷(P4)的高 |
| C.1mol N4转化为2mol N2的同时放出能量 |
| D.相同质量的N4和 N2所含原子个数比为1:2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】反应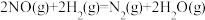 中,每生成
中,每生成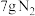 ,放出166kJ的热量,该反应的速率表达式为
,放出166kJ的热量,该反应的速率表达式为 (k、m、n待测),其反应包含下列两步:
(k、m、n待测),其反应包含下列两步:
①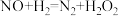 (慢)
(慢)
②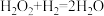 (快)
(快)
T℃时测得有关实验数据如表:
下列说法正确的是
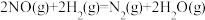 中,每生成
中,每生成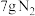 ,放出166kJ的热量,该反应的速率表达式为
,放出166kJ的热量,该反应的速率表达式为 (k、m、n待测),其反应包含下列两步:
(k、m、n待测),其反应包含下列两步:①
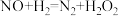 (慢)
(慢)②
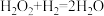 (快)
(快)T℃时测得有关实验数据如表:
| 序号 | c(NO)/( mol/L) | c(H2)/ ( mol/L) | 速率/( ) ) |
| Ⅰ | 0.0060 | 0.0010 | 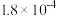 |
| Ⅱ | 0.0060 | 0.0020 | 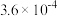 |
| Ⅲ | 0.0010 | 0.0060 | 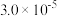 |
| Ⅳ | 0.0020 | 0.0060 |  |
| A.整个反应速率由第②步反应决定 |
| B.正反应的活化能一定是①<② |
C.该反应速率表达式: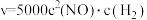 |
D.该反应的热化学方程式为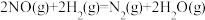 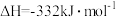 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】烟气脱硫可用生物质热解气(CO、CH4、H2)将SO2在高温下还原为单质硫,原理如下:
① 2CO(g)+SO2(g)===S(g)+2CO2(g) ΔH1=+8.0 kJ•mol-1
② 2H2(g)+SO2(g)=== S(g)+2H2O(g) ΔH2=+90.4 kJ•mol-1
③ 2CO(g)+O2(g) ===2CO2(g) ΔH3=-566.0 kJ•mol-1
④ 2H2(g)+O2(g)=== 2H2O(g) ΔH4
下列说法不正确 的是
① 2CO(g)+SO2(g)===S(g)+2CO2(g) ΔH1=+8.0 kJ•mol-1
② 2H2(g)+SO2(g)=== S(g)+2H2O(g) ΔH2=+90.4 kJ•mol-1
③ 2CO(g)+O2(g) ===2CO2(g) ΔH3=-566.0 kJ•mol-1
④ 2H2(g)+O2(g)=== 2H2O(g) ΔH4
下列说法
| A.升高温度,能提高烟气中SO2的去除率 |
| B.S(g)+O2(g) === SO2(g) ΔH=-574.0 kJ•mol-1 |
| C.H2O(l) === H2(g)+1/2O2(g) ΔH<-1/2ΔH4 |
| D.反应③、④将化学能转化为热能,有利于烟气脱硫 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】在298K、100kPa时,已知:H2O(g)= O2(g)+H2(g) △H1
O2(g)+H2(g) △H1
H2(g)+Cl2(g)= 2HCl(g) △H2
2H2O(g)+2Cl2(g)= 4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是( )
 O2(g)+H2(g) △H1
O2(g)+H2(g) △H1 H2(g)+Cl2(g)= 2HCl(g) △H2
2H2O(g)+2Cl2(g)= 4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是( )
| A.△H3 =2△H1+2△H2 | B.△H3 =2△H1—△H2 |
| C.△H3 =2△H1—2△H2 | D.△H3 =2△H1+△H2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列叙述不正确的是
| A.2CO(g)+O2(g) =2CO2(g)△H=-566 kJ/mol,有关键能(kJ/mol)为O=O:498 C=O:745。则1molCO分解为碳原子与氧原子所需要的能量至少为1916 kJ/mol |
| B.加入催化剂可以降低正逆反应的活化能但不改变反应的反应热 |
| C.氢氧化钠稀溶液分别与盐酸、醋酸、浓硫酸反应生成1mol液态水时的焓变分别为△H1、△H2、△H3,则△H2>△H1>△H3 |
| D.已知C2H4(g)和C2H5OH⑴的燃烧热分别为1411.0kJ/mol和1366 .8kJ/mol,则C2H4(g)合成C2H5OH⑴的△H为-44.2kJ/mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在恒温条件下,向盛有足量NaCl(s)的2L恒容密闭容器中加入0.2molNO2、0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) △H1<0 K1
NaNO3(s)+ClNO(g) △H1<0 K1
②2NO(g)+Cl2(g) 2ClNO(g) △H2<0 K2
2ClNO(g) △H2<0 K2
10分钟时反应达到平衡,测得体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1。下列说法正确的是
①2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) △H1<0 K1
NaNO3(s)+ClNO(g) △H1<0 K1②2NO(g)+Cl2(g)
 2ClNO(g) △H2<0 K2
2ClNO(g) △H2<0 K210分钟时反应达到平衡,测得体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1。下列说法正确的是
| A.平衡后c(NO)=2.5×10-2mol·L-1 |
| B.平衡时NO2的转化率为50% |
| C.其它条件保持不变,反应在绝热条件下进行,则平衡常数K2增大 |
D.反应4NO2(g)+2NaCl(s)  2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数为 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数为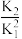 |
您最近一年使用:0次

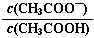
 CH3OH(g)。该反应的△H=-91.kJ·mol-1
CH3OH(g)。该反应的△H=-91.kJ·mol-1

