能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,8gCH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式_____________ 。
(2)已知:
C(s)+O2(g) = CO2(g) △H=-437.3kJ·mol -1
H2(g)+1/2O2(g) = H2O(g) △H=-285.8kJ·mol-1
CO(g)+1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1
则煤气化反应C(s)+H2O(g) = CO(g)+H2(g)的焓变△H=___ kJ·mol-1。
(1)在25℃、101kPa时,8gCH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式
(2)已知:
C(s)+O2(g) = CO2(g) △H=-437.3kJ·mol -1
H2(g)+1/2O2(g) = H2O(g) △H=-285.8kJ·mol-1
CO(g)+1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1
则煤气化反应C(s)+H2O(g) = CO(g)+H2(g)的焓变△H=
更新时间:2019-09-11 04:35:24
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】沼气(主要成分是甲烷)是一种廉价的能源,把农村中大量存在的农作物秸秆、杂草、人畜粪便等在沼气池中发酵,便可产生沼气,沼气完全燃烧可以用来点灯、做饭。
(1)在101kPa时,32gCH4燃烧生成CO2和气态H2O,放出1604kJ的热量,写出甲烷燃烧的热化学方程式为__________________________________________________________ 。
(2)120℃,取CH4和过量O2的混合气体共0.4mol,点燃使其充分反应,将燃烧后的气体通过足量的碱石灰(NaOH和CaO的固体混合物)充分吸收,碱石灰增重8g。计算:
①原混合气体中CH4和O2的体积比是多少? ②反应放出多少热量?
___________
(1)在101kPa时,32gCH4燃烧生成CO2和气态H2O,放出1604kJ的热量,写出甲烷燃烧的热化学方程式为
(2)120℃,取CH4和过量O2的混合气体共0.4mol,点燃使其充分反应,将燃烧后的气体通过足量的碱石灰(NaOH和CaO的固体混合物)充分吸收,碱石灰增重8g。计算:
①原混合气体中CH4和O2的体积比是多少? ②反应放出多少热量?
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】如图1是反应A(g)+3B(g) 2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。

(1)由示意图知,反应物的总能量____ (填“>”、“<”或“=”)生成物的总能量,此反应中反应物的总键能____ (填“>”、“<”或“=”)生成物的总键能。
(2)a=____ (用Ec和Ec′表示)。
(3)加入催化剂对该反应的ΔH____ 影响(填“有”或“无”)。
(4)已知:
2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-akJ•mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=-bkJ•mol-1;
H2O(g)=H2O(l) ΔH3=-ckJ•mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为:_____ 。
(5)工业上用H2(g)和Cl2(g)反应制HCl(g),各键能为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是_____ 。
(6)298K时,0.5molC2H4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出表示C2H4(g)燃烧热的热化学方程式:_____ 。
 2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
(1)由示意图知,反应物的总能量
(2)a=
(3)加入催化剂对该反应的ΔH
(4)已知:
2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-akJ•mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=-bkJ•mol-1;
H2O(g)=H2O(l) ΔH3=-ckJ•mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为:
(5)工业上用H2(g)和Cl2(g)反应制HCl(g),各键能为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是
(6)298K时,0.5molC2H4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出表示C2H4(g)燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】人们常常利用化学反应中的能量变化为人类服务。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是_________ 。
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是_________ 。
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:
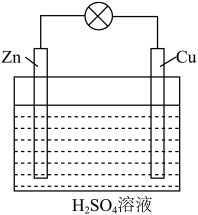
①负极材料是_______ ,正极上能够观察到的现象是_______________________ ,
②正极的电极反应式是______________ 。
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体________ L(标况下)。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:

①负极材料是
②正极的电极反应式是
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。
(1)有机物M经过太阳光光照可转化成N,转化过程如下。
 (M)
(M)
 (N)
(N) 
则M的化学式为,M、N相比,较稳定的是___________ (填“M”或“N”)。
(2)已知 (1)的燃烧热为
(1)的燃烧热为 ,
,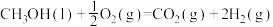

 ,则a
,则a___________ 238.6(填“>”“<”或“=”)。
(3)使 和
和 (g)通过灼热的炭层,生成HCl和
(g)通过灼热的炭层,生成HCl和 ,当有1mol
,当有1mol  参与反应时释放出145kJ热量,写出该反应的热化学方程式:
参与反应时释放出145kJ热量,写出该反应的热化学方程式:___________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,
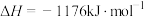 ,则反应过程中,每转移1mol电子时放出的热量为
,则反应过程中,每转移1mol电子时放出的热量为___________ 。
(5)已知:
①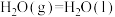
 ;
;
②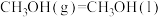
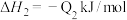 ;
;
③
 (
( 、
、 、
、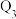 均大于0)。
均大于0)。
若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为___________ kJ。
(1)有机物M经过太阳光光照可转化成N,转化过程如下。
 (M)
(M)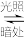
 (N)
(N) 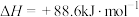
则M的化学式为,M、N相比,较稳定的是
(2)已知
 (1)的燃烧热为
(1)的燃烧热为 ,
,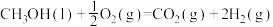

 ,则a
,则a(3)使
 和
和 (g)通过灼热的炭层,生成HCl和
(g)通过灼热的炭层,生成HCl和 ,当有1mol
,当有1mol  参与反应时释放出145kJ热量,写出该反应的热化学方程式:
参与反应时释放出145kJ热量,写出该反应的热化学方程式:(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,

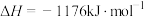 ,则反应过程中,每转移1mol电子时放出的热量为
,则反应过程中,每转移1mol电子时放出的热量为(5)已知:
①
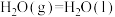
 ;
;②
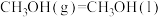
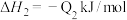 ;
;③

 (
( 、
、 、
、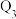 均大于0)。
均大于0)。若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】通过盖斯定律计算。已如在 、
、 时,①
时,①
 ,②
,②
 ,写出
,写出 与
与 反应生成
反应生成 的热化学方程式:
的热化学方程式:___________ 。
 、
、 时,①
时,①
 ,②
,②
 ,写出
,写出 与
与 反应生成
反应生成 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) ΔH=-570 kJ/mol
②2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ/mol
③2CO(g)=2C(s)+O2(g) ΔH=+220.8 kJ/mol
④2C(s)+2O2(g)=2CO2(g) ΔH=-787 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是___________ (填写序号)。
(2)H2的燃烧热为___________ 。
(3)燃烧10 g H2生成液态水,放出的热量为___________ 。
(4)C(s)的燃烧热的热化学方程式为___________ 。
(5)已知:1 L1 mol/LH2SO4溶液与2 L1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为___________ 。
①2H2(g)+O2(g)=2H2O(l) ΔH=-570 kJ/mol
②2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ/mol
③2CO(g)=2C(s)+O2(g) ΔH=+220.8 kJ/mol
④2C(s)+2O2(g)=2CO2(g) ΔH=-787 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10 g H2生成液态水,放出的热量为
(4)C(s)的燃烧热的热化学方程式为
(5)已知:1 L1 mol/LH2SO4溶液与2 L1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为
您最近一年使用:0次



