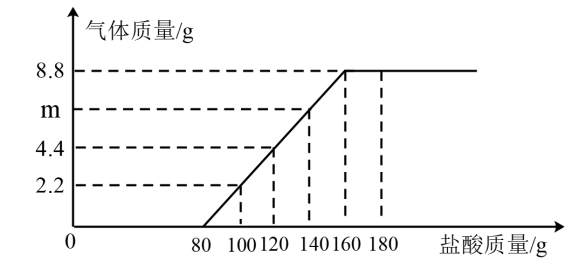
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
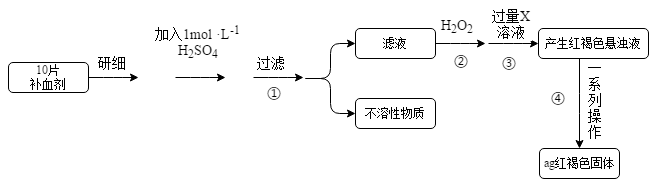
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加_____ ,该过程的现象为________ 。
(2)步骤②加入过量H2O2的目的是________ 。
(3)步骤③中反应的离子方程式是_________ 。
(4)步骤④中一系列处理的操作步骤:过滤、_____ 、灼烧、冷却、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为_______ g。

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加
(2)步骤②加入过量H2O2的目的是
(3)步骤③中反应的离子方程式是
(4)步骤④中一系列处理的操作步骤:过滤、
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为
19-20高二上·山东淄博·开学考试 查看更多[2]
更新时间:2019-09-11 13:06:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有下列4种物质:①NO2②Al(OH)3③FeCl2④SiO2
(1)与水反应产生无色气体的是___ (填序号,下同),反应的化学方程式为___ 。
(2)光导纤维的主要成分是___ 。
(3)既能与酸反应又能与强碱溶液反应的两性氢氧化物是___ ,该物质与强碱反应的离子方程式为___ 。
(4)有人预测①与③的溶液能发生化学反应,可能出现的现象是___ 。
(1)与水反应产生无色气体的是
(2)光导纤维的主要成分是
(3)既能与酸反应又能与强碱溶液反应的两性氢氧化物是
(4)有人预测①与③的溶液能发生化学反应,可能出现的现象是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求填空。
(1)过氧化钠与CO2反应的化学方程式:__ ;
(2)铁与水蒸气反应的化学方程式:__ 。
(3)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,配制完毕后要加入少量铁屑,其目的是___ ,向FeSO4溶液中滴加NaOH溶液,并放置一段时间,此过程中观察到的现象__ 。
(1)过氧化钠与CO2反应的化学方程式:
(2)铁与水蒸气反应的化学方程式:
(3)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,配制完毕后要加入少量铁屑,其目的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物,试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________(填字母)。
(2)某同学把新制的氯水(主要成分Cl2)加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___________ 。
(3) 与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是___________ (填字母)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________(填字母)。
| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
| C.维生素C将Fe3+还原为Fe2+ | D.亚硝酸盐是还原剂 |
(3)
 与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是a.Cl2 b.Fe c.H2O2 d.HNO3
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列4种物质:①NO;②SiO2;③Cl2;④FeCl3,能与O2反应生成红棕色气体的是__________ (填序号,下同);其水溶液具有漂白性的是___________ ;能与强碱反应的氧化物是_______ ;遇KSCN溶液变红色的是_______ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有物质的量浓度均为0.1mo/L的下列溶液:
(1)①NH3·H2O ②FeCl2 ③NaHSO4 ④KOH ⑤Ba(OH)2 ⑥H2SO4,其pH由大到小的顺序排列的是(填序号)___ 。
(2)写出氯化亚铁溶液中,亚铁离子水解的离子方程式___ 。
(3)写出硫酸氢钠与氢氧化钡2:1反应的离子方程式___ 。
(4)将氢氧化钾与氯化亚铁溶液混合,现象___ 。依次发生的化学方程式____ 、___ 。
(5)氯化亚铁保存时为何加少量铁粉___ ,若保存硫酸铁溶液时应向溶液中加入____ 。
(6)如何利用氯水和硫氰化钾检验氯化亚铁溶液中的Fe2+,写出加入试剂的先后顺序和对应现象__ 。
(1)①NH3·H2O ②FeCl2 ③NaHSO4 ④KOH ⑤Ba(OH)2 ⑥H2SO4,其pH由大到小的顺序排列的是(填序号)
(2)写出氯化亚铁溶液中,亚铁离子水解的离子方程式
(3)写出硫酸氢钠与氢氧化钡2:1反应的离子方程式
(4)将氢氧化钾与氯化亚铁溶液混合,现象
(5)氯化亚铁保存时为何加少量铁粉
(6)如何利用氯水和硫氰化钾检验氯化亚铁溶液中的Fe2+,写出加入试剂的先后顺序和对应现象
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如图:
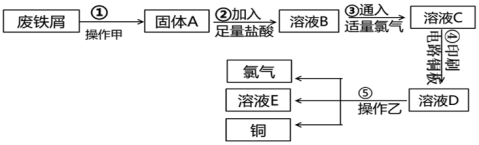
请回答下列问题:
(1)步骤①中操作甲是加饱和碳酸钠溶液并加热其作用是___________ 。
(2)写出步骤②中生成Fe2+的离子方程式___________ 。(写一个即可)
(3)若将③改加入H2O2,写出反应的离子方程式:___________ 。
(4)若溶液B中只含有Fe2+而不含Fe3+,可证明该事实的实验方法是___________ (填序号)。
①先加氯水,后加KSCN溶液后显红色
②先加KSCN溶液,不显红色,再加氯水后显红色
③滴加NaOH溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
④只滴加KSCN溶液不显红色
A.①② B.②③ C.③④ D.①④
(5)溶液D中可能含有的金属阳离子___________ 。
(6)若除去氯化铜中的氯化铁可以加入试剂___________ 。(填序号,可选的试剂有A.NaOH B.CuO C.Fe粉 D.Cu(OH)2 E.CaO)

请回答下列问题:
(1)步骤①中操作甲是加饱和碳酸钠溶液并加热其作用是
(2)写出步骤②中生成Fe2+的离子方程式
(3)若将③改加入H2O2,写出反应的离子方程式:
(4)若溶液B中只含有Fe2+而不含Fe3+,可证明该事实的实验方法是
①先加氯水,后加KSCN溶液后显红色
②先加KSCN溶液,不显红色,再加氯水后显红色
③滴加NaOH溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
④只滴加KSCN溶液不显红色
A.①② B.②③ C.③④ D.①④
(5)溶液D中可能含有的金属阳离子
(6)若除去氯化铜中的氯化铁可以加入试剂
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】推断题善于归纳元素及其化合物之间的转化关系,对学习元素化合物具有重要意义。现有下列物质:金属铁、钠、镁、氯气、氧气、二氧化硫、二氧化碳、水、NaOH溶液、氨水、HCl溶液、KI溶液、稀HNO3、FeCl2溶液。根据要求回答问题:
(1)置换反应是中学常见基本反应类型之一。
①写出非金属单质置换出非金属单质的离子方程式___________________ 。
②写出金属单质置换出非金属单质的化学反应方程式(任写一个)_________ 。
(2)“三角转化”是上述单质及其化合物间常见的转化关系之一。现有如图转化关系:
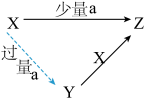
①若X是一种强碱,a是一种酸性氧化物,则Z为________ (填“化学式)。
②若Z是一种能够与血红蛋白结合造成人体缺氧的气体,则a的名称为_____ 。
③若X是常见金属单质,a为含氧酸,则Y Z的离子方程式为
Z的离子方程式为__________
请写出检验Z中金属离子的操作:____________________________
(1)置换反应是中学常见基本反应类型之一。
①写出非金属单质置换出非金属单质的离子方程式
②写出金属单质置换出非金属单质的化学反应方程式(任写一个)
(2)“三角转化”是上述单质及其化合物间常见的转化关系之一。现有如图转化关系:

①若X是一种强碱,a是一种酸性氧化物,则Z为
②若Z是一种能够与血红蛋白结合造成人体缺氧的气体,则a的名称为
③若X是常见金属单质,a为含氧酸,则Y
 Z的离子方程式为
Z的离子方程式为请写出检验Z中金属离子的操作:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有某种含有少量FeCl2杂质的FeCl3样品。现要测定其中铁元素的质量分数,实验采用下列步骤进行:
①准确称量mg样品(在2—3g范围内):
②向样品中加入10mL 6 moL·L-1的盐酸,再加入蒸馏水,配制成250mL溶液:
③量取25mL操作②中配得的溶液,加入3mL氯水,加热使其反应完全;
④趁热迅速加入10%氨水至过量,充分搅拌,使沉淀完全:
⑤过滤,将沉淀洗涤后,移至坩埚,灼烧、冷却、称重,并重复操作至恒重。
试回答下列问题:
(1)溶解样品时,要加入盐酸,原因是___________ ;
(2)加入氯水后,反应的离子方程式为___________ ;
(3)加入过量氨水生成沉淀的离子方程式为___________ ;
(4)若不用氯水,可用下列试剂中的___________ 代替(填序号)。
A.H2O2 B.碘水 C.NaClO
(5)步骤⑤中检验沉淀是否洗净的方法是___________ 。
(6)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为___________ (请把结果约到最简)。
①准确称量mg样品(在2—3g范围内):
②向样品中加入10mL 6 moL·L-1的盐酸,再加入蒸馏水,配制成250mL溶液:
③量取25mL操作②中配得的溶液,加入3mL氯水,加热使其反应完全;
④趁热迅速加入10%氨水至过量,充分搅拌,使沉淀完全:
⑤过滤,将沉淀洗涤后,移至坩埚,灼烧、冷却、称重,并重复操作至恒重。
试回答下列问题:
(1)溶解样品时,要加入盐酸,原因是
(2)加入氯水后,反应的离子方程式为
(3)加入过量氨水生成沉淀的离子方程式为
(4)若不用氯水,可用下列试剂中的
A.H2O2 B.碘水 C.NaClO
(5)步骤⑤中检验沉淀是否洗净的方法是
(6)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
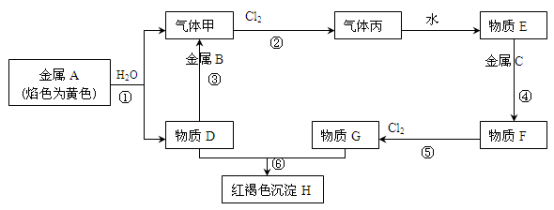
请回答下列问题:
(1)写出下列物质的化学式:B________ 、丙________
(2)写出下列反应的化学方程式:
反应①________________________________________________________________ ;
反应③________________________________________________________________ ;
反应⑥_______________________________________________________________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑥
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】普通泡沫灭火器的铁筒里装着一只小玻璃筒,玻璃筒内盛装硫酸铝溶液,铁筒里盛装碳酸氢钠饱和溶液。使用时,倒置灭火器,两种药液相混合就会喷出含二氧化碳的白色泡沫。
(1)产生此现象的离子方程式是_______ 。
(2)不能把硫酸铝溶液装在铁筒里的主要原因是_______ 。
(3)一般不用碳酸钠代替碳酸氢钠,是因为___________ 。
(1)产生此现象的离子方程式是
(2)不能把硫酸铝溶液装在铁筒里的主要原因是
(3)一般不用碳酸钠代替碳酸氢钠,是因为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的Fe2+。反应式:  +6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为_______ %。
 +6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
您最近半年使用:0次