下面的排序不正确的是( )
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由低到高:Na<Mg<Al |
| D.晶格能由大到小:NaI >NaBr>NaCl> NaF |
更新时间:2019-09-14 13:24:29
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】列有关说法正确的是
| A.含阳离子的化合物一定有阴离子 |
| B.晶格能由大到小:NaF<NaCl<NaBr<NaI |
| C.含有共价键的晶体一定具有高的熔、沸点及硬度 |
| D.空间利用率:面心立方>六方密堆积>体心立方 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法中正确的是
| A.离子晶体中不可能存在共价键、氢键 |
| B.石墨晶体中片层间距远大于层内碳原子间距,说明层间靠范德华力维系 |
| C.可通过溶于水是否导电,区分离子晶体与分子晶体 |
| D.硫单质熔点高于白磷的原因是硫硫键键能大于磷磷键键能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】解释下列物质性质的变化规律与物质结构间的因果关系时,与化学键无关的变化规律是( )
| A.HF、HCl、 HBr、HI的热稳定性依次减弱 |
| B.NaF、NaCl、NaBr、NaI的熔点依次减低 |
| C.金刚石、碳化硅、晶体硅的硬度依次降低 |
| D.H2S的熔沸点小于H2O的熔、沸点 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】SiH4与NH3制备氮化硅(熔点1900℃)的反应为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是| A.熔点:单晶硅>氮化硅 | B.未成对电子数:Si<N |
| C.键角:SiH4>NH3 | D.NH3是由极性键构成的三角锥形分子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法中,正确的是( )
| A.冰融化时,分子中H—O键发生断裂 |
| B.原子晶体中,共价键越强,熔点越高 |
| C.分子晶体中,共价键键能越大,该分子晶体的熔沸点一定越高 |
| D.在晶体中只要有阳离子就一定有阴离子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关金属的说法正确的是
| A.金属原子的核外电子在金属晶体中都是“自由电子” |
| B.金属导电的实质是金属阳离子在外电场作用下的定向移动 |
| C.金属原子的价电子数越多,其金属性就越强 |
| D.自由电子在运动时与金属原子碰撞,引起两者能量交换,从而使金属具有导热性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】 的晶格能可通过下图中的
的晶格能可通过下图中的 循环计算得到,下列说法正确的是
循环计算得到,下列说法正确的是

 的晶格能可通过下图中的
的晶格能可通过下图中的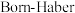 循环计算得到,下列说法正确的是
循环计算得到,下列说法正确的是
A. 属于共价化合物 属于共价化合物 | B.Li的第一电离能为1040kJ/mol |
| C.O=O键的键能为703kJ/mol | D. 的晶格能为2908kJ/mol 的晶格能为2908kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
| A.已知KCl与MgO的晶体结构跟NaCl的晶体结构相似,则晶体的熔点:MgO>KCl>NaCl |
| B.向滴有酚酞的碳酸钠溶液中加入BaCl2溶液,溶液褪色 |
| C.分散系中分散质粒子的直径:Fe(OH)3胶体>Fe(OH)3悬浊液>FeCl3溶液 |
| D.Na2O、MgO、Al2O3均属于碱性氧化物 |
您最近一年使用:0次

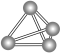
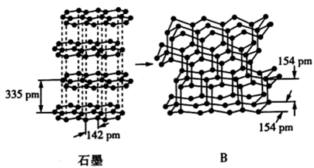
 杂化,键角均为120°
杂化,键角均为120°

