甲型H1N1流感病毒曾在全球广泛传播,给人类健康、社会经济带来了巨大的负面影响。我国采取积极应对措施,使病毒得到了有效的控制,从很大程度上减少了损失,在这里,消毒液功不可没。
(1)生产消毒液是将氯气通入NaOH溶液中,发生的离子反应方程式为_____ 。
(2)取少量消毒液滴加AgNO3溶液,现象是出现白色沉淀,说明消毒液中有___ 离子。
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,写出此过程的离子反应方程式:____ ;该物质有漂白性是因为它有强氧化性,但是它也很不稳定,写出它分解的化学方程式: ___ 。
(1)生产消毒液是将氯气通入NaOH溶液中,发生的离子反应方程式为
(2)取少量消毒液滴加AgNO3溶液,现象是出现白色沉淀,说明消毒液中有
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,写出此过程的离子反应方程式:
更新时间:2019-09-26 09:23:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求书写化学方程式
(1)过氧化钠作为潜艇供氧剂的原理:_______
(2)钠在空气中加热:_______
(3)漂白粉生效原理:_______
(4)制备84消毒液:_______
(5)把钠放入硫酸铜溶液中:_______
(1)过氧化钠作为潜艇供氧剂的原理:
(2)钠在空气中加热:
(3)漂白粉生效原理:
(4)制备84消毒液:
(5)把钠放入硫酸铜溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某兴趣小组探究氯的单质及其化合物的性质。
Ⅰ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。
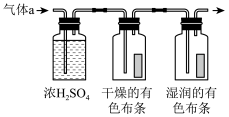
(1)浓硫酸的作用是___________ 。
(2)证明氯气和水反应的实验现象为___________ 。
(3)Cl2溶于水可制得氯水,检验氯水中的Cl-,可选择___________(填字母序号)试剂。
Ⅱ.回答下列问题
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。向“84消毒液”中滴入盐酸,可能发生反应: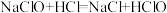 ,其属于
,其属于___________ (填四大基本反应类型)反应。乙同学认为上述过程中还发生了氧化还原反应并生成Cl2,反应的离子方程式为___________ 。
Ⅰ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。

(1)浓硫酸的作用是
(2)证明氯气和水反应的实验现象为
(3)Cl2溶于水可制得氯水,检验氯水中的Cl-,可选择___________(填字母序号)试剂。
| A.硝酸银溶液 | B.酚酞溶液 | C.碳酸钠溶液 | D.品红溶液 |
Ⅱ.回答下列问题
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。向“84消毒液”中滴入盐酸,可能发生反应:
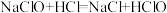 ,其属于
,其属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】判断正误:
1.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂。_______
2.漂白粉可用于生活用水的消毒。_______
3.标准状况下,11.2LCl2与水充分反应转移电子数为0.5NA。_______
4.“84”消毒液的消毒原理与H2O2的相同,都是利用强氧化性。_______
5.漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3。_______
6.NaClO和Ca(ClO)2的溶液能杀菌消毒的原理是二者水解均呈碱性。_______
7.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合产生的HClO易分解。_______
1.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂。
2.漂白粉可用于生活用水的消毒。
3.标准状况下,11.2LCl2与水充分反应转移电子数为0.5NA。
4.“84”消毒液的消毒原理与H2O2的相同,都是利用强氧化性。
5.漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3。
6.NaClO和Ca(ClO)2的溶液能杀菌消毒的原理是二者水解均呈碱性。
7.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合产生的HClO易分解。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氯气可用于制取漂白剂和自来水消毒。
(1)实验室利用二氧化锰和浓盐酸反应制氯气的化学方程式为_______ 。
(2)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是_______ (填名称)。
(3)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为_______ 。
(4)同学们探究“84”消毒液在不同 下使红纸褪色的情况,做了如下实验:
下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的 ;
;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用 溶液将3个烧杯内溶液的
溶液将3个烧杯内溶液的 分别调至10、7和4.(溶液体积变化忽略不计)
分别调至10、7和4.(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知,溶液中 、
、 和
和 物质的量分数(
物质的量分数( )随溶液
)随溶液 变化的关系如图所示:
变化的关系如图所示:
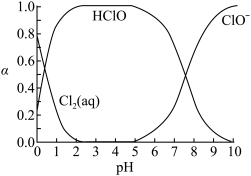
说明: 的物质的量分数可表示为:
的物质的量分数可表示为: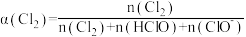
①由实验现象可获得以下结论:溶液的 在4~10范围内,
在4~10范围内, 越大,红纸褪色
越大,红纸褪色_______ 。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______ 。
(5)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如 气体就是一种新型高效含氯消毒剂。
气体就是一种新型高效含氯消毒剂。
①一种制备 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为_______ 。
②另一种制备 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 体积约占
体积约占 ,每生成0.5mol
,每生成0.5mol ,转移
,转移_______  。
。
(6)下列事实能说明氯气的氧化性比硫强的是________
a.硫的沸点比氯气的高
b.与金属单质反应,硫被还原为-2价,氯被还原为-1价
c.铜与 反应生成
反应生成 ,与硫生成
,与硫生成
d.将 通入
通入 溶液中,溶液变浑浊
溶液中,溶液变浑浊
(1)实验室利用二氧化锰和浓盐酸反应制氯气的化学方程式为
(2)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是
(3)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入
 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为(4)同学们探究“84”消毒液在不同
 下使红纸褪色的情况,做了如下实验:
下使红纸褪色的情况,做了如下实验:步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的
 ;
;步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用
 溶液将3个烧杯内溶液的
溶液将3个烧杯内溶液的 分别调至10、7和4.(溶液体积变化忽略不计)
分别调至10、7和4.(溶液体积变化忽略不计)步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的 | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色比b烧杯更浅;4h后红纸褪色 |
已知,溶液中
 、
、 和
和 物质的量分数(
物质的量分数( )随溶液
)随溶液 变化的关系如图所示:
变化的关系如图所示:
说明:
 的物质的量分数可表示为:
的物质的量分数可表示为: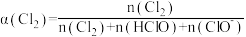
①由实验现象可获得以下结论:溶液的
 在4~10范围内,
在4~10范围内, 越大,红纸褪色
越大,红纸褪色②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
(5)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如
 气体就是一种新型高效含氯消毒剂。
气体就是一种新型高效含氯消毒剂。①一种制备
 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为②另一种制备
 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 体积约占
体积约占 ,每生成0.5mol
,每生成0.5mol ,转移
,转移 。
。(6)下列事实能说明氯气的氧化性比硫强的是
a.硫的沸点比氯气的高
b.与金属单质反应,硫被还原为-2价,氯被还原为-1价
c.铜与
 反应生成
反应生成 ,与硫生成
,与硫生成
d.将
 通入
通入 溶液中,溶液变浑浊
溶液中,溶液变浑浊
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84”消毒液,可以说化学让生活更美好。图为“84”消毒液说明书。请回答下列问题:
(1)工业上常用氯气生产84消毒液,请写出反应的离子方程式___________ ,其有效成分为___________ (写化学式)。
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是___________ (用离子方程式表达)。
(3)游泳池水的消毒多用漂粉精,写出漂白精显效的化学方程式___________ 。
(4)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的___________。
 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等1:200水溶液;餐饮具、瓜果等1:100水溶液 |
(1)工业上常用氯气生产84消毒液,请写出反应的离子方程式
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是
(3)游泳池水的消毒多用漂粉精,写出漂白精显效的化学方程式
(4)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的___________。
| A.增强漂白能力和消毒作用 |
| B.使它转化为较稳定物质,便于保存和运输 |
| C.使它转化为较易溶于水的物质 |
| D.提高氯的质量分数,有利于漂白、消毒 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】海水中存在大量的氯元素,通过对海水中氯元素的提取,可制取单质氯气,也可制取氯的多种氧化物。回答下列问题:
(1)氯气可溶于水形成氯水,溶液中含氯元素的微粒有_______ 种。氯水中属于弱电解质的是_______ (除水外,写化学式),写出该物质的电离方程式_______ 。
(2)常温时,氯气可与 NaOH 溶液反应制取漂白液(俗称 84 消毒液),漂白液的有效成分是_______ 。84 消毒液可作家庭消毒剂,但不能与洁厕精(主要成分是盐酸)混合使用,原因是_______ (用离子反应方程式表示)。
(3)一定条件下,氯气与 NaOH 溶液充分反应后溶液中的 ClO3-和 ClO-的个数比为 1:2,则溶液中 ClO-和 Cl-的个数比为_______ 。
(4)Cl2O 是一种酸性氧化物,常温时是一种棕黄色气体,有毒。制备原理如下: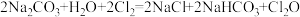 ,请用双线桥表示出该反应中电子转移的方向和数目
,请用双线桥表示出该反应中电子转移的方向和数目_______ 。制备过程中可用NaOH溶液除去剩余Cl2O,写出该反应的化学反应方程式_______ 。
(1)氯气可溶于水形成氯水,溶液中含氯元素的微粒有
(2)常温时,氯气可与 NaOH 溶液反应制取漂白液(俗称 84 消毒液),漂白液的有效成分是
(3)一定条件下,氯气与 NaOH 溶液充分反应后溶液中的 ClO3-和 ClO-的个数比为 1:2,则溶液中 ClO-和 Cl-的个数比为
(4)Cl2O 是一种酸性氧化物,常温时是一种棕黄色气体,有毒。制备原理如下:
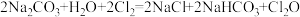 ,请用双线桥表示出该反应中电子转移的方向和数目
,请用双线桥表示出该反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
(1)标准状况下,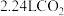 与足量的
与足量的 充分反应,转移的电子总数为
充分反应,转移的电子总数为 ,判断依据:
,判断依据:_______ 。
(2)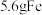 和
和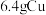 分别与
分别与 充分反应,转移的电子数均为
充分反应,转移的电子数均为 ,判断依据:
,判断依据:_______ 。
(3)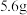 铁粉与硝酸反应失去的电子数一定为
铁粉与硝酸反应失去的电子数一定为 ,判断依据:
,判断依据:_______ 。
(4)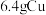 与S完全反应,转移的电子数为
与S完全反应,转移的电子数为 ,判断依据:
,判断依据:_______ 。
(5)向 溶液中通入适量
溶液中通入适量 ,当有
,当有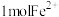 被氧化时,转移的电子总数一定等于
被氧化时,转移的电子总数一定等于 ,判断依据:
,判断依据:_______ 。
 为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。(1)标准状况下,
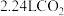 与足量的
与足量的 充分反应,转移的电子总数为
充分反应,转移的电子总数为 ,判断依据:
,判断依据:(2)
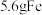 和
和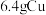 分别与
分别与 充分反应,转移的电子数均为
充分反应,转移的电子数均为 ,判断依据:
,判断依据:(3)
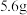 铁粉与硝酸反应失去的电子数一定为
铁粉与硝酸反应失去的电子数一定为 ,判断依据:
,判断依据:(4)
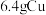 与S完全反应,转移的电子数为
与S完全反应,转移的电子数为 ,判断依据:
,判断依据:(5)向
 溶液中通入适量
溶液中通入适量 ,当有
,当有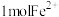 被氧化时,转移的电子总数一定等于
被氧化时,转移的电子总数一定等于 ,判断依据:
,判断依据:
您最近一年使用:0次

 的电离方程式
的电离方程式 属于
属于 溶液中通入
溶液中通入 、③
、③ 中的一种,均会产生沉淀。回答下列问题:
中的一种,均会产生沉淀。回答下列问题:

