碳酸镁晶体是一种新型吸波隐形材料中的增强剂。
实验一:合成碳酸镁晶体的步骤:
①配制一定浓度的MgSO4溶液和NH4HCO3溶液;
②量取一定量的NH4 HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;
③用氨水调节溶液pH至9.5,放置一段时间后,过滤、洗涤、干燥得碳酸镁晶体产品。
称取3.000gMgSO4样品配制250mL溶液流程如图所示:
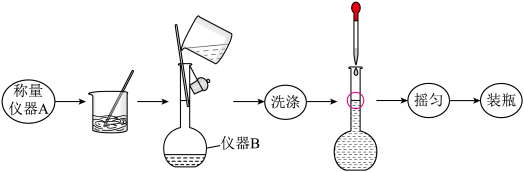
回答下列问题:
(1)写出实验仪器名称:A_____ ;B_____ 。配制溶液过程中定容后的“摇匀”的实验操作为______ 。
(2)检验碳酸镁晶体是否洗干净的方法是_________ 。
实验二:测定产品MgCO3·nH2O中的n值(仪器和药品如图所示):
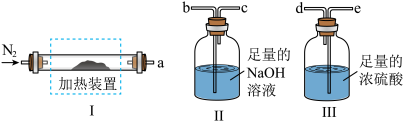
(3)实验二装置的连接顺序为_____ (按气流方向,用接口字母abcde表示),其中Ⅱ装置的作用是_____ 。
(4)加热前先通入N2排尽装置Ⅰ中的空气,然后称取装置Ⅱ、Ⅲ的初始质量。进行加热时还需通入N2的作用是______ 。
(5)若要准确测定n值,至少需要下列所给数据中的_____ (填选项字母),写出相应1种组合情景下,求算n值的数学表达式:n=______ 。
a.装置Ⅰ反应前后质量差m1 b.装置Ⅱ反应前后质量差m2 c.装置Ⅲ反应前后质量差m3
实验一:合成碳酸镁晶体的步骤:
①配制一定浓度的MgSO4溶液和NH4HCO3溶液;
②量取一定量的NH4 HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;
③用氨水调节溶液pH至9.5,放置一段时间后,过滤、洗涤、干燥得碳酸镁晶体产品。
称取3.000gMgSO4样品配制250mL溶液流程如图所示:

回答下列问题:
(1)写出实验仪器名称:A
(2)检验碳酸镁晶体是否洗干净的方法是
实验二:测定产品MgCO3·nH2O中的n值(仪器和药品如图所示):

(3)实验二装置的连接顺序为
(4)加热前先通入N2排尽装置Ⅰ中的空气,然后称取装置Ⅱ、Ⅲ的初始质量。进行加热时还需通入N2的作用是
(5)若要准确测定n值,至少需要下列所给数据中的
a.装置Ⅰ反应前后质量差m1 b.装置Ⅱ反应前后质量差m2 c.装置Ⅲ反应前后质量差m3
更新时间:2019-10-26 12:28:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】“84”消毒液能有效杀灭新型冠状病毒,某同学购买了一瓶“84”消毒液,其说明有如下信息:NaClO相对分子质量74.5、质量分数25% 、密度1.19 g·cm-3、 1000 mL,稀释后使用。请根据信息和相关知识回答下列问题:
(1)该“84”消毒液的物质的量浓度为___________ mol·L-1;(保留至小数点后一位)
(2)现实验室需要480 mL 0.2 mol/L的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。
①应用托盘天平称取NaClO固体___________ g ;
②配制NaClO溶液时需用的主要仪器有:托盘天平、药匙、玻璃棒、烧杯、___________ 、___________ ;
③容量瓶在使用前必须先___________ ;
④实验时遇下列情况,会导致溶液物质的量浓度偏高的是___________ 。
A.容量瓶内壁附有水珠而未干燥处理
B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤
D.溶解后没有冷却便进行定容
E.定容时仰视刻度线
F.摇匀后发现液面低于刻度线后未作处理
(1)该“84”消毒液的物质的量浓度为
(2)现实验室需要480 mL 0.2 mol/L的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。
①应用托盘天平称取NaClO固体
②配制NaClO溶液时需用的主要仪器有:托盘天平、药匙、玻璃棒、烧杯、
③容量瓶在使用前必须先
④实验时遇下列情况,会导致溶液物质的量浓度偏高的是
A.容量瓶内壁附有水珠而未干燥处理
B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤
D.溶解后没有冷却便进行定容
E.定容时仰视刻度线
F.摇匀后发现液面低于刻度线后未作处理
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】FeSO4•7H2O广泛用于医药和工业领域。以下是FeSO4•7H2O的实验室制备流程图。

根据题意完成下列填空:
(1)碳酸钠溶液能除去酯类油污,是因为_________________ (用离子方程式表示)。
(2)废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答)_________ ,__________ 。
以下是测定某补血剂(FeSO4•7H2O)中铁元素含量的流程图。根据题意完成下列填空:
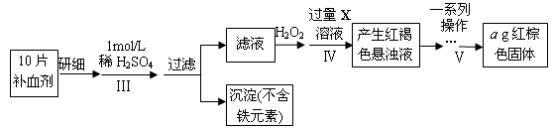
(3)步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及_________________ 。
(4)步骤Ⅴ一系列操作依次是:①过滤②洗涤③_______ ④冷却⑤称量⑥恒重操作。操作⑥的目的是___________________________________ 。
(5)假设实验无损耗,则每片补血剂含铁元素的质量______________ g(用含a的代数式表示)。

根据题意完成下列填空:
(1)碳酸钠溶液能除去酯类油污,是因为
(2)废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答)
以下是测定某补血剂(FeSO4•7H2O)中铁元素含量的流程图。根据题意完成下列填空:

(3)步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及
(4)步骤Ⅴ一系列操作依次是:①过滤②洗涤③
(5)假设实验无损耗,则每片补血剂含铁元素的质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】有下列化学仪器:①托盘天平;②玻璃棒;③药匙;④烧杯;⑤量筒;⑥容量瓶;⑦胶头滴管;⑧细口试剂瓶;⑨标签纸。
(1)现需要配制500 1
1 硫酸溶液,需用质量分数为98%、密度为1.84
硫酸溶液,需用质量分数为98%、密度为1.84 的浓硫酸
的浓硫酸__  。
。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是_______ 。
(3)容量瓶使用前检验漏水的方法是________ 。
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”“偏低”或“不变”)
①用以稀释硫酸的烧杯未洗涤,_________ 。
②未经冷却趁热将溶液注入容量瓶中,_______ 。
③摇匀后发现液面低于刻度线再加水,________ 。
④容量瓶中原有少量蒸馏水,________ 。
⑤定容时俯视观察液面,________ 。
(1)现需要配制500
 1
1 硫酸溶液,需用质量分数为98%、密度为1.84
硫酸溶液,需用质量分数为98%、密度为1.84 的浓硫酸
的浓硫酸 。
。(2)从上述仪器中,按实验使用的先后顺序,其编号排列是
(3)容量瓶使用前检验漏水的方法是
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”“偏低”或“不变”)
①用以稀释硫酸的烧杯未洗涤,
②未经冷却趁热将溶液注入容量瓶中,
③摇匀后发现液面低于刻度线再加水,
④容量瓶中原有少量蒸馏水,
⑤定容时俯视观察液面,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发黏、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。

①仪器m的名称为____ ,装置F中试剂的作用是____ 。
②装置连接顺序:A→____→____→____→E→D。____
③写出A中反应的化学方程式____ 。
④实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是____ 。
⑤为了提高S2Cl2的纯度,实验的关键是控制好温度和____ 。
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图实验方案来测定该混合气体中SO2的体积分数。
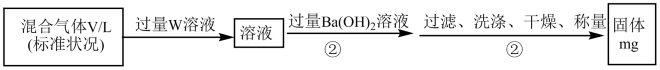
①W溶液可以是____ (填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为____ (用含V、m的式子表示)。
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解 ②S2Cl2+Cl2  2SCl2 2SCl2③遇高热或与明火接触,有引起燃烧的危险 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。

①仪器m的名称为
②装置连接顺序:A→____→____→____→E→D。
③写出A中反应的化学方程式
④实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
⑤为了提高S2Cl2的纯度,实验的关键是控制好温度和
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图实验方案来测定该混合气体中SO2的体积分数。

①W溶液可以是
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐2】三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中计入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL滴定中MnO4-被还原成Mn2+ 。重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液19.98mL。
请回答下列问题:
① 配制三草酸合铁酸钾溶液的操作步骤依次是:称量、_______ 、转移、洗涤并转移、________ 摇匀。
② 加入锌粉的目的是________ 。
③ 写出步骤三中发生反应的离子方程式________ 。
④ 实验测得该晶体中铁的质量分数为__________ 。在步骤二中,若加入的KMnO4的溶液的量不够,则测得的铁含量__________ 。(选填“偏低”“偏高”“不变”)
(2)结晶水的测定
将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,至于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误;_________ ;_________ 。
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中计入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL滴定中MnO4-被还原成Mn2+ 。重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液19.98mL。
请回答下列问题:
① 配制三草酸合铁酸钾溶液的操作步骤依次是:称量、
② 加入锌粉的目的是
③ 写出步骤三中发生反应的离子方程式
④ 实验测得该晶体中铁的质量分数为
(2)结晶水的测定
将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,至于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误;
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。某同学设计了如下实验步骤:①加入稀盐酸使溶液呈强酸性,再加入过量的BaCl2溶液。②加热干燥沉淀物。③过滤,用蒸馏水洗涤沉淀2~3次。④称量n g样品,置于烧杯中。⑤加入适量蒸馏水使样品溶解。⑥将沉淀物冷却至室温后称量。⑦重复上述部分操作直到合格,最后得到m g固体。
试回答下列问题:
(1)上述实验操作的正确顺序是:_______________ ,在操作⑦中需要重复的操作是:_____ 。
(2)本实验中能否用Ba(NO3)2代替BaCl2________ (填“能”或“不能”),理由是:__________ 。
(3)步骤③中加盐酸使溶液呈强酸性的目的是:____________ 。
(4)步骤⑦的合格标准是:_______________ 。
(5)实验测得样品中无水亚硫酸钠的质量分数是:__________ (列出算式,不需化简)。
试回答下列问题:
(1)上述实验操作的正确顺序是:
(2)本实验中能否用Ba(NO3)2代替BaCl2
(3)步骤③中加盐酸使溶液呈强酸性的目的是:
(4)步骤⑦的合格标准是:
(5)实验测得样品中无水亚硫酸钠的质量分数是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】二氧化氯消毒剂是国际公认的高效消毒灭菌剂。二氧化氯漂白液中常含有ClO2和Cl2两种主要成分。化学兴趣小组同学为测定某二氧化氯漂白液中ClO2的浓度,进行如下实验:
【实验Ⅰ】配制100 mL0.100 mol/L的Na2S2O3溶液,步骤如下:
①用托盘天平称取一定质量Na2S2O3∙5H2O固体,放入烧杯,用适量蒸馏水溶解;
②将烧杯中的溶液小心的注入100 mL容量瓶中;
③用蒸馏水_______;
④继续向容量瓶中加水至距刻度线1~2 cm处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是_______ ;
(2)配制溶液过程中需用托盘天平称量Na2S2O3∙5H2O固体的质量为_______ ;
(3)步骤②操作之前容量瓶中有少量水,则配制的溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”);
(4)补全步骤③操作:用蒸馏水_______ 。
【实验Ⅱ】测定二氧化氯漂白液中的物质的量浓度,步骤如下:
①量取10.00 mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到100 mL,再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应: 、
、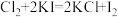 。
。
②加入淀粉作指示剂,向其中逐滴加入0.100 mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为: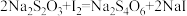
③加入稀硫酸调节溶液pH=3,发生反应: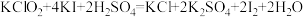
④再逐滴加入0.100 mol/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20.00 mL。
(5)该二氧化氯漂白液中ClO2的物质的量浓度为_______ 。(写出计算过程)
【实验Ⅰ】配制100 mL0.100 mol/L的Na2S2O3溶液,步骤如下:
①用托盘天平称取一定质量Na2S2O3∙5H2O固体,放入烧杯,用适量蒸馏水溶解;
②将烧杯中的溶液小心的注入100 mL容量瓶中;
③用蒸馏水_______;
④继续向容量瓶中加水至距刻度线1~2 cm处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是
(2)配制溶液过程中需用托盘天平称量Na2S2O3∙5H2O固体的质量为
(3)步骤②操作之前容量瓶中有少量水,则配制的溶液的浓度将
(4)补全步骤③操作:用蒸馏水
【实验Ⅱ】测定二氧化氯漂白液中的物质的量浓度,步骤如下:
①量取10.00 mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到100 mL,再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:
 、
、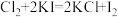 。
。②加入淀粉作指示剂,向其中逐滴加入0.100 mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:
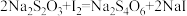
③加入稀硫酸调节溶液pH=3,发生反应:
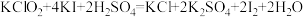
④再逐滴加入0.100 mol/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20.00 mL。
(5)该二氧化氯漂白液中ClO2的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】三氯化铬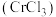 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
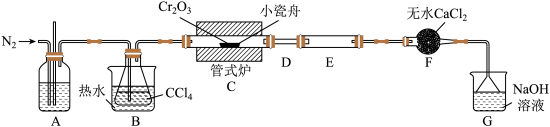
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为,其实验装置如图所示:
的反应为,其实验装置如图所示:
已知:① (俗称光气)有毒,遇水发生水解;
(俗称光气)有毒,遇水发生水解;
②碱性条件下, 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。
。
回答下列问题:
(1)基态 原子的简化核外电子排布式为
原子的简化核外电子排布式为___________ 。
(2)无水 的作用是
的作用是___________ 。
(3)装置E用来收集产物。实验过程中若D处出现堵塞,可通过___________ (填操作方法)使实验继续进行。
(4)装置G中发生生成两种盐的反应的化学方程式为___________ 。
(5)测定产品中 质量分数的实验步骤如下:
质量分数的实验步骤如下:
I.取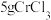 产品,在强碱性条件下,加入过量的
产品,在强碱性条件下,加入过量的 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;
II.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使 转化为
转化为 ,再加适量的蒸馏水将溶液稀释至
,再加适量的蒸馏水将溶液稀释至 ;
;
III.取 溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的
溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液
标准溶液 (已知
(已知 被
被 还原为
还原为 )。
)。
①该样品中 的质量分数为
的质量分数为___________  (保留小数点后两位,
(保留小数点后两位,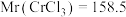 )
)
②下列操作将导致产品中 质量分数测定值偏低的是
质量分数测定值偏低的是___________ (填标号)。
A.步骤I中未继续加热一段时间
B.步骤III中所用 溶液已变质
溶液已变质
C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
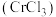 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为,其实验装置如图所示:
的反应为,其实验装置如图所示:
已知:①
 (俗称光气)有毒,遇水发生水解;
(俗称光气)有毒,遇水发生水解;②碱性条件下,
 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。
。回答下列问题:
(1)基态
 原子的简化核外电子排布式为
原子的简化核外电子排布式为(2)无水
 的作用是
的作用是(3)装置E用来收集产物。实验过程中若D处出现堵塞,可通过
(4)装置G中发生生成两种盐的反应的化学方程式为
(5)测定产品中
 质量分数的实验步骤如下:
质量分数的实验步骤如下:I.取
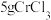 产品,在强碱性条件下,加入过量的
产品,在强碱性条件下,加入过量的 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;II.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使
 转化为
转化为 ,再加适量的蒸馏水将溶液稀释至
,再加适量的蒸馏水将溶液稀释至 ;
;III.取
 溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的
溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液
标准溶液 (已知
(已知 被
被 还原为
还原为 )。
)。①该样品中
 的质量分数为
的质量分数为 (保留小数点后两位,
(保留小数点后两位,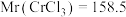 )
)②下列操作将导致产品中
 质量分数测定值偏低的是
质量分数测定值偏低的是A.步骤I中未继续加热一段时间
B.步骤III中所用
 溶液已变质
溶液已变质C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某活动小组利用如图装置验证N0的还原性及探究工业生产硝酸的原理。
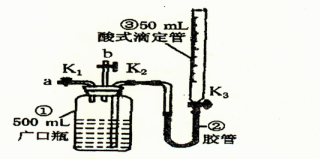
如何检查该装置气密性___________________ 。
(一)向广口瓶①中通入NO并测定NO的体积
(1)通入NO前,向广口瓶①中加入水,让水充满广口瓶①,且调节滴定管③中液面与①相平并记录滴定管③的刻度。
(2)从导管a通入一定量的NO并准确测定通入NO的体积的主要操作:_____________ ;计算出通入的NO的体积为V mL(V<50)。
(二)验证NO的还原性;探究工业生产硝酸的原理
(1)停止通入NO后关闭K1、K3,打开K2,从导管b缓缓通入O2,写出通入O2的过程中发生的化学反应方程式:____________________________ 。
(2)继续通入O2,打开K3并及时调整滴定管③液面与广口瓶①中液面相平,直到广口瓶①中刚好充满液体。
I.当通入氧气的体积为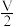 mL时,则广口瓶①的气体体积为
mL时,则广口瓶①的气体体积为________ ;
II.当广口瓶①的气体体积为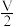 mL时,则通入氧气的体积可能为
mL时,则通入氧气的体积可能为__________ 。

如何检查该装置气密性
(一)向广口瓶①中通入NO并测定NO的体积
(1)通入NO前,向广口瓶①中加入水,让水充满广口瓶①,且调节滴定管③中液面与①相平并记录滴定管③的刻度。
(2)从导管a通入一定量的NO并准确测定通入NO的体积的主要操作:
(二)验证NO的还原性;探究工业生产硝酸的原理
(1)停止通入NO后关闭K1、K3,打开K2,从导管b缓缓通入O2,写出通入O2的过程中发生的化学反应方程式:
(2)继续通入O2,打开K3并及时调整滴定管③液面与广口瓶①中液面相平,直到广口瓶①中刚好充满液体。
I.当通入氧气的体积为
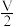 mL时,则广口瓶①的气体体积为
mL时,则广口瓶①的气体体积为II.当广口瓶①的气体体积为
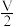 mL时,则通入氧气的体积可能为
mL时,则通入氧气的体积可能为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。
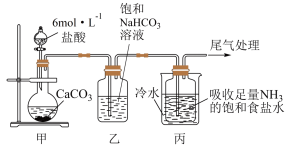
(1)装置甲中反应的离子方程式 为______________________________ ;
装置乙的作用是_______________ ,反应的化学方程式为____________________ 。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为__________ 。
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有__________ 、洗涤固体、__________ ,最后一步发生反应的化学方程式为_______________ 。
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:

(5)测定该纯碱样品的纯度:称取m1 g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为m2 g。则该纯碱样品的纯度为_______________ 。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。

(1)装置甲中反应的
装置乙的作用是
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:

| 选择的装置(填编号) | 实验现象 | 实验结论 |
| 样品中含NaHCO3 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ca3N2是一种重要试剂,极易潮解。某小组利用氨气与钙反应制备氮化钙。

回答下列问题:
(1)试剂R可能是__________ (填化学式);装置D中倒置干燥管的作用是__________ 。
(2)写出C的硬质玻璃管中发生反应的化学方程式:_____________ 。
(3)实验过程中,先启动A处反应,一段时间后点燃C处酒精灯,其目的是___________ 。
(4)从产品纯度考虑,有人建议在C、D装置之间增加下列装置__________ (填选项)。
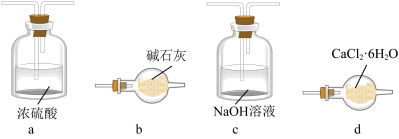

回答下列问题:
(1)试剂R可能是
(2)写出C的硬质玻璃管中发生反应的化学方程式:
(3)实验过程中,先启动A处反应,一段时间后点燃C处酒精灯,其目的是
(4)从产品纯度考虑,有人建议在C、D装置之间增加下列装置

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】一化学兴趣小组,探究从某工业废水(含有大量的FeSO4、较多的Cu2+ 和少量的Na+)中回收FeSO4制备绿矾(FeSO4·7H2O),同时回收金属铜的方法,以减少污染并变废为宝。以下是他们设计出的回收流程图,回答有关问题:
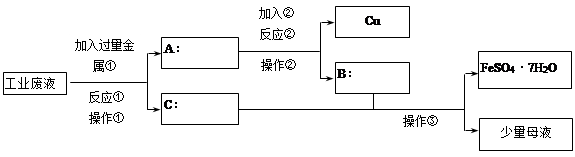
(1)加入的金属①为(填物质名称)______________ ,加入②后反应的离子方程式为_______________________ 。
(2)操作②的名称为_________________ ,用到的玻璃仪器有______________________ 。
(3)反应①和②都是氧化还原反应,写出反应①的离子方程式并用单线桥标出电子转移的方向和数目________________________ 。
(4)母液中含有的离子有(填离子符号):_______________________________ 。

(1)加入的金属①为(填物质名称)
(2)操作②的名称为
(3)反应①和②都是氧化还原反应,写出反应①的离子方程式并用单线桥标出电子转移的方向和数目
(4)母液中含有的离子有(填离子符号):
您最近一年使用:0次



