硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应方程式如下:Na2SO4+4C →Na2S+ 4CO,Na2SO4+4CO→Na2S+4CO2
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S_____ g,最多生成标况下的CO_____ L。
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是____ mol≤n≤___ mol,若生成等物质的量CO和CO2,则消耗的碳的物质的量为____ mol。
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。_____
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。
更新时间:2019-11-19 10:54:34
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。
(1)NO的体积为_______ ;
(2)NO2的体积为______ 。
(1)NO的体积为
(2)NO2的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】取一定量碳酸钠和碳酸氢钠的固体混合物样品,分成两等份,取其中一份加热到质量不再改变,冷却后称其质量减少6.2 g,另一份样品溶于水,向所得溶液中逐滴加入200 mL稀盐酸时产生CO22.24 L,过量时产生CO211.2 L(气体体积均为标准状况)。
(1)碳酸氢钠与碳酸钠的物质的量之比__________________ 。
(2)盐酸物质的量浓度为__________________ mol/L。
(1)碳酸氢钠与碳酸钠的物质的量之比
(2)盐酸物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将1.92 g铜与足量的稀硝酸完全反应,求:
(1)反应后生成硝酸铜的物质的量_____________________ ;
(2)被还原硝酸的物质的量___________________________ ;
(3)标准状况下,生成NO气体的体积_________________ 。
(1)反应后生成硝酸铜的物质的量
(2)被还原硝酸的物质的量
(3)标准状况下,生成NO气体的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】工业上用氢气与氯气的的反应生产盐酸。
若一定量氢气在氯气中燃烧,所得混合物用100mL 3.0mol/L NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含NaClO的物质的量为0.0500mol。
(1)写出氯气与氢氧化钠溶液反应的化学方程式______________________ 。
(2)原NaOH溶液的质量分数为_____________________________ 。(保留三位小数)
(3)所得溶液中Cl-的物质的量为____________________________ 。
(4)求所用氯气和参加反应的氢气的物质的量之比____________________________ 。(写出计算过程)
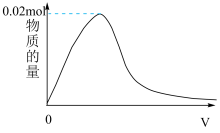
(5)若将H2和Cl2充分混合后,在光照条件下会发生爆炸。现取一份H2和Cl2组成的混合气体经光照充分反应后,通入1000mL 0.1mol/L的NaOH溶液中,如图表示某种离子的物质的量随通入气体的体积变化曲线。当n=0.02mol时,光照前的混合气体中H2和Cl2的物质的量之比为________ (已知HClO为弱酸,在水中主要以分子形式存在)
 。
。
若一定量氢气在氯气中燃烧,所得混合物用100mL 3.0mol/L NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含NaClO的物质的量为0.0500mol。
(1)写出氯气与氢氧化钠溶液反应的化学方程式
(2)原NaOH溶液的质量分数为
(3)所得溶液中Cl-的物质的量为
(4)求所用氯气和参加反应的氢气的物质的量之比
(5)若将H2和Cl2充分混合后,在光照条件下会发生爆炸。现取一份H2和Cl2组成的混合气体经光照充分反应后,通入1000mL 0.1mol/L的NaOH溶液中,如图表示某种离子的物质的量随通入气体的体积变化曲线。当n=0.02mol时,光照前的混合气体中H2和Cl2的物质的量之比为
 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】已知HCN有剧毒;HCN、HOCN中N元素的化合价相同。
a.碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1, Q与水反应的化学方程式为__________ 。
b.NaCN超标的电镀废水可用两段氧化法处理:
①.NaCN与NaClO反应,生成NaOCN和NaCl
②.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
完成下列填空:
①写出第二次氧化时发生反应的离子方程式__________________________
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成_________ 和H2O。
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
a.碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1, Q与水反应的化学方程式为
b.NaCN超标的电镀废水可用两段氧化法处理:
①.NaCN与NaClO反应,生成NaOCN和NaCl
②.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
完成下列填空:
①写出第二次氧化时发生反应的离子方程式
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为______________________ 。相关化学键的键能如下表所示:
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为______________________ 。
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中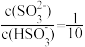 ,则该混合溶液的pH=
,则该混合溶液的pH=___________ (25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为
| 化学键 | Cl—Cl | N≡O(NO气体) | Cl—N | N=O |
| 键能/(kJ·mol-1) | 243 | 630 | 200 | 607 |
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中
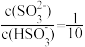 ,则该混合溶液的pH=
,则该混合溶液的pH=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】氯化铁和摩尔盐是铁的两种重要盐类,在净水和定量分析等方面具有重要作用。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是____________ 。
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中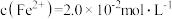 ,
,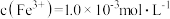 ,
,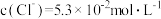 ,则该溶液的
,则该溶液的 约为
约为______ (不考虑水的电离和离子的水解)。
(3)摩尔盐 [(NH4)2Fe(SO4)2•6H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在 的该盐的溶液中,离子浓度由大到小的顺序是
的该盐的溶液中,离子浓度由大到小的顺序是____________ 。
(4)摩尔盐与酸性高锰酸钾发生反应: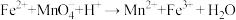
a.配平上述离子方程式:( ) Fe2++( ) MnO4-+( ) H+→( ) Mn2++( ) Fe3++( ) H2O
b.已知摩尔盐相对分子质量为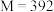 ,取摩尔盐产品
,取摩尔盐产品 (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成 溶液,取出
溶液,取出 用
用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液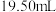 ,则产品中摩尔盐的质量分数为
,则产品中摩尔盐的质量分数为____________ (用小数表示,保留四位小数)。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中
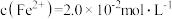 ,
,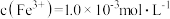 ,
,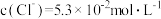 ,则该溶液的
,则该溶液的 约为
约为(3)摩尔盐 [(NH4)2Fe(SO4)2•6H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在
 的该盐的溶液中,离子浓度由大到小的顺序是
的该盐的溶液中,离子浓度由大到小的顺序是(4)摩尔盐与酸性高锰酸钾发生反应:
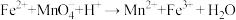
a.配平上述离子方程式:
b.已知摩尔盐相对分子质量为
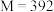 ,取摩尔盐产品
,取摩尔盐产品 (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成 溶液,取出
溶液,取出 用
用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液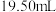 ,则产品中摩尔盐的质量分数为
,则产品中摩尔盐的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
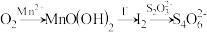
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:__________ 。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L−1表示),写出计算过程__________ 。
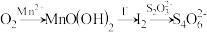
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L−1表示),写出计算过程
您最近一年使用:0次



