25℃,以0.10mol/LNaOH溶液滴定20.00mL醋酸溶液和20.00mL盐酸,滴定曲线如图所示,下列说法不正确的是
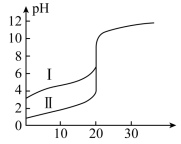

| A.曲线Ⅰ、Ⅱ分别表示醋酸溶液和盐酸的滴定曲线 |
| B.达到滴定终点时,两溶液pH均等于7 |
| C.初始时盐酸的浓度为0.10mol/L |
| D.滴定醋酸溶液、盐酸时,均可选择酚酞溶液做指示剂 |
更新时间:2019-11-15 15:52:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对于常温下 为2的盐酸,下列叙述正确的是
为2的盐酸,下列叙述正确的是
 为2的盐酸,下列叙述正确的是
为2的盐酸,下列叙述正确的是A.将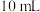 该溶液稀释至 该溶液稀释至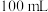 后, 后, 小于3 小于3 |
B.向该溶液中加入等体积的 为12的氨水恰好完全中和 为12的氨水恰好完全中和 |
C.该溶液中 电离出的 电离出的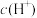 与水电离出的 与水电离出的 之比为 之比为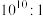 |
D.该溶液中由水电离出的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知 pOH=-lgc(OH-)。向20mL0.1mol·L-1的氨水中滴加未知浓度的稀 H2SO4,测得混合溶液的温度、pOH随加入稀硫酸体积的变化如下图所示,下列说法不正确的是( )


| A.稀H2SO4 的物质的量浓度为0.05mol·L-1 |
| B.当溶液中pH=pOH时,水的电离程度最大 |
| C.a点时溶液中存在[NH3·H2O]+2[OH-]=[NH4+]+2[H+] |
| D.a、b、c 三点对应 NH4+的水解平衡常数:Kh(b)>Kh(a)>Kh(c) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列叙述中,不正确的是
A.用0.1026mol/L的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为22.35mL |
| B.用标准烧碱溶液滴定待测的醋酸溶液,应以酚酞为指示剂 |
| C.若200mLc(H+)=1×10-3mol/L的某一元酸和100mLc(OH-)=1×10-3mol/L的某一元碱相混合后,溶液呈碱性。则所用的酸和碱可能是等浓度的弱酸和强碱 |
| D.25℃时,若pH=a的10体积某强酸溶液与pH=b的1体积某强碱溶液混合后溶液呈中性,则a+b=15 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各组离子在指定溶液中能大量共存的是
A.能使甲基橙变为黄色的溶液中: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.明矾溶液中: 、 、 、 、 、 、 |
D.加入铝粉会产生 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.提取海带中碘元素时,为保证I-完全被氧化为I2,最好加入过量的氧化剂(H2O2或新制氯水) |
| B.在醋酸总酸含量测定实验中,用标准NaOH溶液滴定醋酸时,最好选用酚酞作指示剂 |
| C.当锌完全溶解后,产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
| D.在层析实验操作时,不能让滤纸上的试样点接触展开剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】25℃时,向 溶液中逐渐滴入
溶液中逐渐滴入 溶液,得到如图的滴定曲线。下列粒子浓度的关系式正确的是
溶液,得到如图的滴定曲线。下列粒子浓度的关系式正确的是

 溶液中逐渐滴入
溶液中逐渐滴入 溶液,得到如图的滴定曲线。下列粒子浓度的关系式正确的是
溶液,得到如图的滴定曲线。下列粒子浓度的关系式正确的是
A.点①溶液中, |
B.点②溶液中, |
C.点③溶液中, |
| D.滴定过程中,水的电离程度大小:②>③>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组设计了如图甲所示的数字化实验装置,研究常温下,向1L0.1mol/LH2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的粒子的物质的量分数与溶液pH的关系如图乙所示,则下列说法中正确的是( )




| A.pH=4.0时,图中n(HA-)约为0.0091mol |
| B.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
| C.该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂 |
| D.常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
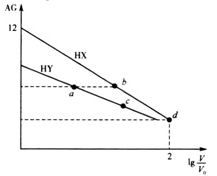
【推荐1】常温下,浓度均为0.1 mol·L-1、体积均为V0的HX和HY溶液,分别加水稀释至体积V,AG 随lg
随lg 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
 随lg
随lg 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
| A.相同条件下NaX溶液的pH大于NaY溶液的pH |
| B.水的电离程度:a=b<c |
| C.d点所示溶液的pH=2 |
D.当lg =2时,若两溶液同时升高温度,则c(X-)/c(Y-)增大 =2时,若两溶液同时升高温度,则c(X-)/c(Y-)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,下列事实不能说明某一元酸HX是弱酸的是
A. 溶液的 溶液的 |
B. 溶液 溶液 |
C. 的HA溶液稀释10倍,溶液pH小于5 的HA溶液稀释10倍,溶液pH小于5 |
D.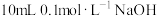 溶液与 溶液与 溶液恰好中和 溶液恰好中和 |
您最近一年使用:0次





