氯化亚铜(CuCI)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸。工业上采用如下工艺流程,从某酸性废液(主要含Cu2+、Fe3+、H+、CI-)中制备氯化亚铜。
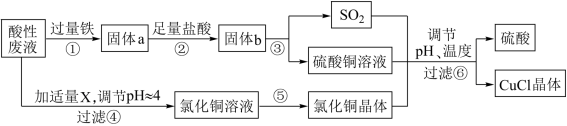
请回答下列问题:
(1)写出步骤①中发生的两个主要反应的离子方程式:___ 。
(2)步骤②的操作名称是___ 。
(3)步骤④中所加物质X为___ 。
(4)步骤⑤的操作是___ 。
(5)步骤⑥应调节溶液的pH呈酸性,且用乙醇洗涤CuCl晶体,目的是___ 。
(6)在CuCI的生成过程中,可以循环利用的物质是___ ,理论上___ (填“需要”或“不需要”)补充(不考虑调节等消耗);理由是___ 。
(7)工业上还可以采用以碳棒为电极电解CuCl2溶液得到CuCl。写出电解CuCl2溶液中的阴极上发生的电极反应:___ 。

请回答下列问题:
(1)写出步骤①中发生的两个主要反应的离子方程式:
(2)步骤②的操作名称是
(3)步骤④中所加物质X为
(4)步骤⑤的操作是
(5)步骤⑥应调节溶液的pH呈酸性,且用乙醇洗涤CuCl晶体,目的是
(6)在CuCI的生成过程中,可以循环利用的物质是
(7)工业上还可以采用以碳棒为电极电解CuCl2溶液得到CuCl。写出电解CuCl2溶液中的阴极上发生的电极反应:
更新时间:2019-12-01 21:56:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯化亚铜(CuCl)在生产中广泛用作催化剂、杀菌剂、脱色剂。某兴趣小组采用加热分解氯化铜晶体(CuCl2·xH2O)的方法制备CuCl,其装置如下(夹持仪器省略)。
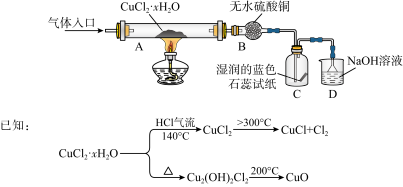
完成下列填空:
(1)在实验过程中,可以观察到C中试纸的颜色变化是___________________________ 。
(2)实验过程中需要全程通入干燥的HCl,其作用是___________________________ 。
(3)反应结束后,取出CuCl产品进行实验,发现其中含有少量的杂质,根据已知信息分析:
① 若杂质是CuCl2,则产生的原因可能是____________________________________ 。
② 若杂质是CuO,则产生的原因可能是_____________________________________ 。
(4)为测定原料CuCl2·xH2O中结晶水的数目x,可采取如下方案:
a.用电子天平称取一定质量氯化铜晶体 b.在______ (填仪器名称)中充分灼烧
c.在干燥器中冷却 d.称量所得黑色固体质量
e.重复b ~ d操作直至_____________________
① 完成上述实验操作步骤。
② 若氯化铜晶体质量为3.384 g,最终得到黑色固体质量为1.600 g,则x =________ (精确到0.1)。
③ 若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。____________________________

完成下列填空:
(1)在实验过程中,可以观察到C中试纸的颜色变化是
(2)实验过程中需要全程通入干燥的HCl,其作用是
(3)反应结束后,取出CuCl产品进行实验,发现其中含有少量的杂质,根据已知信息分析:
① 若杂质是CuCl2,则产生的原因可能是
② 若杂质是CuO,则产生的原因可能是
(4)为测定原料CuCl2·xH2O中结晶水的数目x,可采取如下方案:
a.用电子天平称取一定质量氯化铜晶体 b.在
c.在干燥器中冷却 d.称量所得黑色固体质量
e.重复b ~ d操作直至
① 完成上述实验操作步骤。
② 若氯化铜晶体质量为3.384 g,最终得到黑色固体质量为1.600 g,则x =
③ 若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_________________ 。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
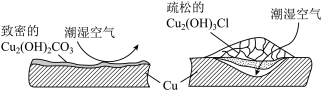
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因____________________________________________________________________________________ 。
(3)下图为青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu2(OH)3Cl的原理示意图。
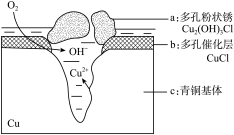
写出正极的电极反应式___________________________________________________ 。若生成2.145g Cu2(OH)3Cl,理论上消耗标准状况下氧气的体积为________ L。
(4)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
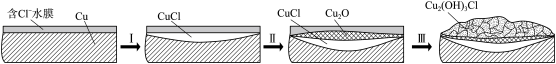
①过程Ⅰ的正极反应物是___________ 。
②过程Ⅰ负极的电极反应式是_____________________________________________________ 。
(5)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:

请回答下列问题:
①写出碳酸钠法的离子方程式________________________________________________ 。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________ 。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:

Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因
(3)下图为青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu2(OH)3Cl的原理示意图。

写出正极的电极反应式
(4)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:

①过程Ⅰ的正极反应物是
②过程Ⅰ负极的电极反应式是
(5)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:

请回答下列问题:
①写出碳酸钠法的离子方程式
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室以孔雀石[主要成分是CuCO3·Cu(OH)2,还含有少量杂质FeO、Fe2O3、SiO2]为原料制备CuSO4·5H2O步骤如下:
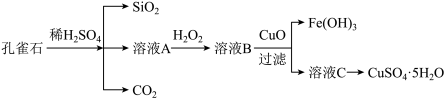
请回答下列问题:
(1)溶液A的金属离子有Fe3+和______________ 。
(2)溶液A中加入H2O2的目的是______________ ,发生的离子方程式为_____________________ 。
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、______________ 、过滤等操作。
(4)溶液B与CuO反应生成Fe(OH)3和溶液C的化学方程式为________________________ 。

请回答下列问题:
(1)溶液A的金属离子有Fe3+和
(2)溶液A中加入H2O2的目的是
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、
(4)溶液B与CuO反应生成Fe(OH)3和溶液C的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】(CH3COO)2Mn·4H2O主要用于纺织染色催化剂和分析试剂,其制备过程如图。回答下列问题:
步骤一:以MnO2为原料制备MnSO4
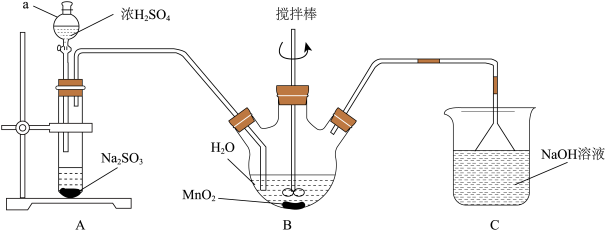
(1)仪器a的名称是___ ,C装置中NaOH溶液的作用是___________ 。
(2)B装置中发生反应的化学方程式是___________ 。
步骤二:制备MnCO3沉淀
充分反应后将B装置中的混合物过滤,向滤液中加入饱和NH4HCO3溶液,反应生成MnCO3沉淀。过滤,洗涤,干燥。
(3)①生成MnCO3的离子方程式_____________ 。
②判断沉淀已洗净的操作和现象是___________ 。
步骤三:制备(CH3COO)2Mn·4H2O固体
向11.5 g MnCO3固体中加入醋酸水溶液,反应一段时间后,过滤、洗涤,控制温度不超过55℃干燥,得(CH3COO)2Mn·4H2O固体。探究生成(CH3COO)2Mn·4H2O最佳实验条件的数据如下:
(4)产品干燥温度不宜超过55℃的原因可能是___________ 。
(5)上述实验探究了___________ 和___________ 对产品质量的影响,实验l中(CH3COO)2Mn·4H2O产率为___________ 。
步骤一:以MnO2为原料制备MnSO4

(1)仪器a的名称是
(2)B装置中发生反应的化学方程式是
步骤二:制备MnCO3沉淀
充分反应后将B装置中的混合物过滤,向滤液中加入饱和NH4HCO3溶液,反应生成MnCO3沉淀。过滤,洗涤,干燥。
(3)①生成MnCO3的离子方程式
②判断沉淀已洗净的操作和现象是
步骤三:制备(CH3COO)2Mn·4H2O固体
向11.5 g MnCO3固体中加入醋酸水溶液,反应一段时间后,过滤、洗涤,控制温度不超过55℃干燥,得(CH3COO)2Mn·4H2O固体。探究生成(CH3COO)2Mn·4H2O最佳实验条件的数据如下:
| 实验组别 | 醋酸质量分数 | 温度/℃ | 产品质量/g |
| 1 | 3% | 50 | 22.05 |
| 2 | 3% | 60 | 22.24 |
| 3 | 4% | 50 | 22.13 |
| 4 | 4$ | 60 | 23.27 |
(5)上述实验探究了
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】通过海水晾晒可得粗盐,粗盐除 外,还含有
外,还含有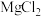 、
、 、
、 以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
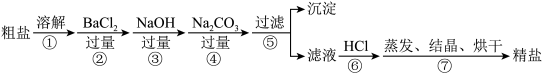
(1)在第 步粗盐溶解操作中要用玻璃棒,作用是
步粗盐溶解操作中要用玻璃棒,作用是______________ 。
(2)第 步操作的目的是除去粗盐中的
步操作的目的是除去粗盐中的_____________  填化学式,下同
填化学式,下同 ,第
,第 步操作的目的是除去滤液中
步操作的目的是除去滤液中_______ 和_________ 。
(3)第 步“过滤”操作中得到沉淀的成分有:泥沙、
步“过滤”操作中得到沉淀的成分有:泥沙、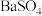 、
、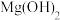 、
、________ 和______ 。
(4)在第 步操作中,选择的除杂的试剂不能用
步操作中,选择的除杂的试剂不能用 代替
代替 ,理由是
,理由是_________________ 。
(5)过量 溶液和过量
溶液和过量 溶液滴加顺序
溶液滴加顺序_____ 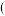 填可以或不可以
填可以或不可以 调换,理由是
调换,理由是______________ 。
(6)写出第 步反应的化学方程式
步反应的化学方程式_______________________________ 。
 外,还含有
外,还含有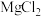 、
、 、
、 以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下: 
(1)在第
 步粗盐溶解操作中要用玻璃棒,作用是
步粗盐溶解操作中要用玻璃棒,作用是(2)第
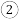 步操作的目的是除去粗盐中的
步操作的目的是除去粗盐中的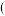 填化学式,下同
填化学式,下同 ,第
,第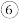 步操作的目的是除去滤液中
步操作的目的是除去滤液中(3)第
 步“过滤”操作中得到沉淀的成分有:泥沙、
步“过滤”操作中得到沉淀的成分有:泥沙、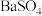 、
、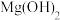 、
、(4)在第
 步操作中,选择的除杂的试剂不能用
步操作中,选择的除杂的试剂不能用 代替
代替 ,理由是
,理由是(5)过量
 溶液和过量
溶液和过量 溶液滴加顺序
溶液滴加顺序 填可以或不可以
填可以或不可以 调换,理由是
调换,理由是(6)写出第
 步反应的化学方程式
步反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某实验室模拟以工业用菱铁矿(FeCO3)含碱式碳酸铜[Cu2(OH)2CO3]为原料制取纯净的FeCO3和氯化铜晶体(CuCl2·2H2O)的生产流程如下:
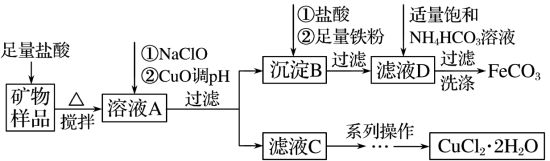
(1)盐酸溶解矿物样品时可能发生的离子方程式______ 。
(2)写出向溶液A中加入NaClO的离子方程式_________ 。
(3)向沉淀B中依次加入盐酸和铁粉时可能发生的离子方程式_________ 。
(4)处理滤液D时,除产生沉淀外,还产生无色气体,写出该反应的离子方程式_________ 。

(1)盐酸溶解矿物样品时可能发生的离子方程式
(2)写出向溶液A中加入NaClO的离子方程式
(3)向沉淀B中依次加入盐酸和铁粉时可能发生的离子方程式
(4)处理滤液D时,除产生沉淀外,还产生无色气体,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】纳米磁性Fe3O4在生物靶向材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性Fe3O4的工艺流程如下
(已知Zn+2NaOH=NaZnO2+H2↑):

(1)将有油污的废旧镀锌铁皮“碱洗”的目的是除去废旧镀锌铁皮表面的油污和___________ 。
(2)“酸溶”的离子方程式为___________ 。
(3)“氧化”时发生的总反应的离子方程式为___________ ,在酸性条件下,FeSO4很容易发生如下反应:4FeSO4+O2+6H2O=4FeOOH+4H2SO4,为避免生成FeOOH影响产品纯度。则“氧化”时应选择的加料方式为___________ 。
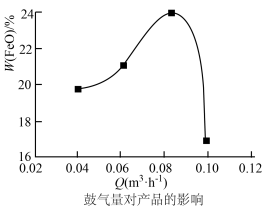
(4)空气的流量影响磁性性能的好环。由图可知,空气的最佳鼓入量为0.08m3/h.此时实际产品中Fe2+与Fe3+的物质的量之比约为___________ 。(保留二位小数)
(已知Zn+2NaOH=NaZnO2+H2↑):

(1)将有油污的废旧镀锌铁皮“碱洗”的目的是除去废旧镀锌铁皮表面的油污和
(2)“酸溶”的离子方程式为
(3)“氧化”时发生的总反应的离子方程式为
(4)空气的流量影响磁性性能的好环。由图可知,空气的最佳鼓入量为0.08m3/h.此时实际产品中Fe2+与Fe3+的物质的量之比约为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇。它是一种食品添加剂,我们所食用的部分食盐中就添加了亚铁氰化钾作为抗结剂。如果食用过量,易引起胃肠不适。同学们可以观察一下家中食盐的配料表,尽量选用不含抗结剂的食盐。亚铁氰化钾可用如下方法进行制备。
已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:
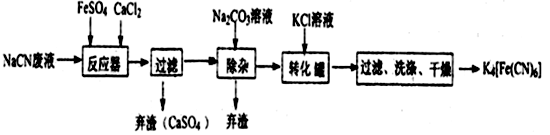
(1)常温下,NaCN水溶液的pH_______ 7(填“>”、“<”、“ = ”)。
(2)反应器中发生的主要反应的化学方程式为_____________________________ 。
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、______________ 。
(4)转化器中生成K4[Fe(CN)6]的反应类型是_______________ ,相同温度下,溶解度:K4[Fe(CN)6]___________ Na4[Fe(CN)6](填“>”“ = ”“<”)。
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为_____________________________ 。
Ⅱ亚铁氰化钾也可以用硫酸亚铁铵为原料制备。可以用氧化还原滴定法测定晶体中Fe2+的含量。称取一份质量为20.0g 的硫酸亚铁铵晶体样品,制成溶液。用0.5 mol/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO4- 被还原成Mn2+时,耗KMnO4 溶液体积20.00mL。
滴定时,将KMnO4 溶液装在____ (酸式或碱式) 滴定管中,判断反应到达滴定终点的现象为__________ ;晶体中FeSO4的质量分数为____________ 。
已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:

(1)常温下,NaCN水溶液的pH
(2)反应器中发生的主要反应的化学方程式为
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、
(4)转化器中生成K4[Fe(CN)6]的反应类型是
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为
Ⅱ亚铁氰化钾也可以用硫酸亚铁铵为原料制备。可以用氧化还原滴定法测定晶体中Fe2+的含量。称取一份质量为20.0g 的硫酸亚铁铵晶体样品,制成溶液。用0.5 mol/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO4- 被还原成Mn2+时,耗KMnO4 溶液体积20.00mL。
滴定时,将KMnO4 溶液装在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.5%的ZnS和12.8%的CuS。某同学用15.0 g该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下:
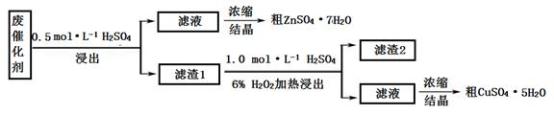
回答下列问题:
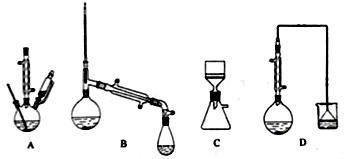
(1)在下列装置中,第一次浸出必须用_____ ,第二次浸出应选用________ 。(填标号)
(2)第二次浸出时,向盛有滤液1的反应器中加入稀硫酸,后滴入过氧化氢溶液。若顺序相反,会造成___________ 。滤渣2的主要成分是____________________ 。
(3)浓缩硫酸锌、硫酸铜溶液使用的器皿名称是________________ 。
(4)某同学在实验完成之后,得到1.5gCuSO4﹒5H2O,则铜的回收率为______________ 。

回答下列问题:
(1)在下列装置中,第一次浸出必须用

(2)第二次浸出时,向盛有滤液1的反应器中加入稀硫酸,后滴入过氧化氢溶液。若顺序相反,会造成
(3)浓缩硫酸锌、硫酸铜溶液使用的器皿名称是
(4)某同学在实验完成之后,得到1.5gCuSO4﹒5H2O,则铜的回收率为
您最近一年使用:0次



