KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为:
________ KClO3+________ HCl(浓) ===________ KCl+________ ClO2↑+________ Cl2↑+________ H2O
(1)配平以上化学方程式(写出各物质的化学计量数)。
(2)ClO2是反应的_________ (填“氧化”或“还原”)产物。浓盐酸在反应中显示出来的性质是________ (填字母)。
a.还原性 b.氧化性 c.酸性 d.碱性
(3)反应产生0.1 mol Cl2,则转移的电子的物质的量为________ mol。
(4)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl−,则其消毒的效率(以单位质量得到电子数表示)是Cl2的________ 倍(保留2位小数)。
(1)配平以上化学方程式(写出各物质的化学计量数)。
(2)ClO2是反应的
a.还原性 b.氧化性 c.酸性 d.碱性
(3)反应产生0.1 mol Cl2,则转移的电子的物质的量为
(4)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl−,则其消毒的效率(以单位质量得到电子数表示)是Cl2的
更新时间:2019-12-09 18:48:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)高锰酸钾是常见的氧化剂,也是氧化还原滴定中的常用试剂。酸性KMnO4与蒽( 分子式C14H10)反应生成蒽醌(
分子式C14H10)反应生成蒽醌(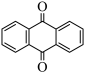 分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是
分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是_____ (填写化学式),发生氧化反应的原子是________ (在图中将相关位置的原子“○”涂黑,○表示碳原子, 表示氢原子);
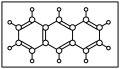
(2)实验室盛放高锰酸钾溶液的试剂瓶常有黑色沉积物,是因KMnO4发生分解生成的MnO2所至,同时有KOH生成,另一反应产物是_______ (填写化学式),判断的理由是_____ 。
(3)在酸性条件下高锰酸钾与硫酸铬能发生反应,请配平该反应方程式:
____ Cr2(SO4)3+____ KMnO4+____ H2O→____ CrO3+____ K2SO4+____ MnSO4+____ H2SO4
(4)实验室称取0.867 g草酸钠(Na2C2O4,式量为134),溶解于水,加入一定量硫酸,用未知浓度的KMnO4溶液滴定,用去KMnO4溶液22.50 mL,反应式如下(未配平):MnO4+C2O42+H+→Mn2++CO2+H2O。则KMnO4溶液的浓度是________ mol/L。
 分子式C14H10)反应生成蒽醌(
分子式C14H10)反应生成蒽醌( 分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是
分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是
(2)实验室盛放高锰酸钾溶液的试剂瓶常有黑色沉积物,是因KMnO4发生分解生成的MnO2所至,同时有KOH生成,另一反应产物是
(3)在酸性条件下高锰酸钾与硫酸铬能发生反应,请配平该反应方程式:
(4)实验室称取0.867 g草酸钠(Na2C2O4,式量为134),溶解于水,加入一定量硫酸,用未知浓度的KMnO4溶液滴定,用去KMnO4溶液22.50 mL,反应式如下(未配平):MnO4+C2O42+H+→Mn2++CO2+H2O。则KMnO4溶液的浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硼酸( )为一元弱酸,广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:
)为一元弱酸,广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:
(1) 中B元素的化合价为
中B元素的化合价为______ 。
(2)已知: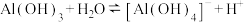 ,
, 的电离方程式为
的电离方程式为____ ,酸性:
___ (填“>”或“<”) 。
。
(3) 受热分解得到
受热分解得到 ,
, 和镁粉混合点燃可得单质B,写出生成单质B的化学方程式
和镁粉混合点燃可得单质B,写出生成单质B的化学方程式________ ,该反应中氧化剂和还原剂物质的量之比为______ 。
(4) 可用于生产储氢材料NaBH4。涉及的主要反应为:
可用于生产储氢材料NaBH4。涉及的主要反应为:
Ⅰ.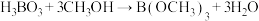
Ⅱ.
①“反应Ⅰ”的类型为______ (填标号)。
a.取代反应 b.加成反应 c.加聚反应 d.氧化反应
②NaH的电子式为____________ 。
③在碱性条件下,NaBH4与CuSO4溶液反应可得Cu和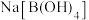 ,其中H元素由
,其中H元素由 价升高为
价升高为 价,该反应的离子方程式为
价,该反应的离子方程式为______ 。
 )为一元弱酸,广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:
)为一元弱酸,广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:(1)
 中B元素的化合价为
中B元素的化合价为(2)已知:
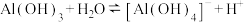 ,
, 的电离方程式为
的电离方程式为
 。
。(3)
 受热分解得到
受热分解得到 ,
, 和镁粉混合点燃可得单质B,写出生成单质B的化学方程式
和镁粉混合点燃可得单质B,写出生成单质B的化学方程式(4)
 可用于生产储氢材料NaBH4。涉及的主要反应为:
可用于生产储氢材料NaBH4。涉及的主要反应为:Ⅰ.
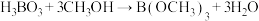
Ⅱ.

①“反应Ⅰ”的类型为
a.取代反应 b.加成反应 c.加聚反应 d.氧化反应
②NaH的电子式为
③在碱性条件下,NaBH4与CuSO4溶液反应可得Cu和
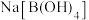 ,其中H元素由
,其中H元素由 价升高为
价升高为 价,该反应的离子方程式为
价,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硒和硫是同一主族元素,二氧化硒(SeO2))是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1 :1,写出Se和浓HNO3的反应方程式_______________ 。
(2)已知:Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O===Se+2SO42-+4H+,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是______________ 。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①__ SeO2+__ KI+__ HNO3―→__ Se+__ I2+__ KNO3+__ H2O
②I2+2Na2S2O3===Na2S4O6+2NaI
配平方程式①,用单线桥标出电子转移的方向和数目。__________________
(4)实验中,准确称量SeO2样品0.1500 g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为________ 。
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1 :1,写出Se和浓HNO3的反应方程式
(2)已知:Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O===Se+2SO42-+4H+,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①
②I2+2Na2S2O3===Na2S4O6+2NaI
配平方程式①,用单线桥标出电子转移的方向和数目。
(4)实验中,准确称量SeO2样品0.1500 g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。CaO2和Na2O2在结构和性质上有很多相似的地方。请完成下列问题:
(1)CaO2属于____ (填“离子化合物”或“共价化合物”),其电子式为_____ ,其阴、阳离子个数比为______ 。
(2)CaO2与水反应的化学方程式为______ ,生成1mol单质气体,转移的电子数为__________ 。(用NA代表阿伏伽德罗常数)
(3)CaO2与二氧化碳反应的化学方程式为_________ ,该反应属于____________ 。
A.置换反应 B.氧化还原反应 C.复分解反应
(1)CaO2属于
(2)CaO2与水反应的化学方程式为
(3)CaO2与二氧化碳反应的化学方程式为
A.置换反应 B.氧化还原反应 C.复分解反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,且无二次污染。K2FeO4中Fe为___ 价,盐酸中加入少量K2FeO4固体,产生黄绿色气体Cl2,K2FeO4被还原成FeCl3,该反应的化学方程式是___ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
①用单线桥标出电子转移的方向和数目___ 。
②此反应中氧化剂与还原剂的质量之比为___ 。
(3)已知常温下在溶液中可发生如下反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___ 。
(1)高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,且无二次污染。K2FeO4中Fe为
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
①用单线桥标出电子转移的方向和数目
②此反应中氧化剂与还原剂的质量之比为
(3)已知常温下在溶液中可发生如下反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原料,实验室常用2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数约为_______ 个,此时被氧化的物质为_______ mol。
(2)。“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ ,若有2mol氯气参与该反应,则此时转移的电子数为_______ NA。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为_______ 。
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为_______ g(请保留两位小数)。
(1)氯气是重要的化工原料,实验室常用2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应制备氯气,该反应的氧化剂是
(2)。“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为
| 9 | 白球比 | 1.6 | |
| 10 | 乳酸脱氢酶 | 161 | U/L |
| 11 | 磷酸肌酸激酶 | 56 | U/L |
| 12 | 甘油三酯 | 0.52 | mmol/L |
| 13 | 总胆固醇 | 4.27 | mmol/L |
| 14 | 高密度脂蛋白胆固醇 | 1.57 | mmol/L |
| 15 | 低密度脂蛋白胆固醇 | 1.40 | mmol/L |
| 16 | 葡萄糖 | 4.94 | mmol/L |
您最近一年使用:0次
【推荐1】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:______________ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式:_____________________ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为
②配平该反应的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫有多种化合物,如 、
、 等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(1)有学者提出利用 、
、 等离子的作用,在常温下将
等离子的作用,在常温下将 氧化成
氧化成 而实现
而实现 的回收利用,写出
的回收利用,写出 将
将 氧化成
氧化成 反应的离子方程式
反应的离子方程式___________ 。
(2)含有 、
、 的硫酸盐混合溶液可用于吸收
的硫酸盐混合溶液可用于吸收 回收硫单质,其转化关系如图所示。其中反应①中作氧化剂的是
回收硫单质,其转化关系如图所示。其中反应①中作氧化剂的是___________ (填离子符号或化学式),该图示中总反应的化学方程式为___________ 。
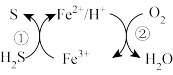
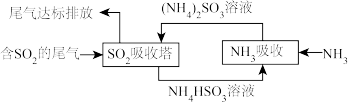
(3)某企业利用下列流程综合处理工厂排放的含 的烟气,以减少其对环境造成的污染。“
的烟气,以减少其对环境造成的污染。“ 吸收塔”中发生反应的化学方程式为
吸收塔”中发生反应的化学方程式为___________ ,该流程中可循环利用的物质为___________ (填化学式)。
(4)生产过程中的尾气需要测定 的含量符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量
的含量符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量 溶液吸收再加入足量
溶液吸收再加入足量 溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到bg沉淀。 溶液的作用是
溶液的作用是___________ ;尾气中 含量(体积分数)的计算式是
含量(体积分数)的计算式是___________ (用含V、b的代数式表示)。
 、
、 等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。(1)有学者提出利用
 、
、 等离子的作用,在常温下将
等离子的作用,在常温下将 氧化成
氧化成 而实现
而实现 的回收利用,写出
的回收利用,写出 将
将 氧化成
氧化成 反应的离子方程式
反应的离子方程式(2)含有
 、
、 的硫酸盐混合溶液可用于吸收
的硫酸盐混合溶液可用于吸收 回收硫单质,其转化关系如图所示。其中反应①中作氧化剂的是
回收硫单质,其转化关系如图所示。其中反应①中作氧化剂的是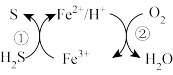
(3)某企业利用下列流程综合处理工厂排放的含
 的烟气,以减少其对环境造成的污染。“
的烟气,以减少其对环境造成的污染。“ 吸收塔”中发生反应的化学方程式为
吸收塔”中发生反应的化学方程式为
(4)生产过程中的尾气需要测定
 的含量符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量
的含量符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量 溶液吸收再加入足量
溶液吸收再加入足量 溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到bg沉淀。 溶液的作用是
溶液的作用是 含量(体积分数)的计算式是
含量(体积分数)的计算式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为________ 和________ 。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2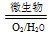 Fe2++SO42—
Fe2++SO42—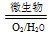 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_______________________ ,第二步反应的离子方程式为________________ 。
(3)工业煤干馏得到的产品有焦炭、________ 。
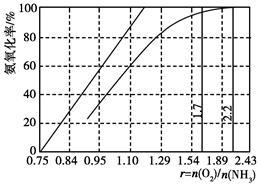
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________ ,实际生产要将r值维持在1.7~2.2之间,原因是__________________________________________ 。
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2
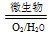 Fe2++SO42—
Fe2++SO42—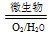 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为(3)工业煤干馏得到的产品有焦炭、
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2022年9月14号台风梅花过后,对环境进行消毒杀菌、获取洁净的饮用水都需要大量消毒剂,开发具有广谱、高效、低毒的杀菌、消毒剂是今后发展的趋势。
(1) 、
、 、
、 (还原产物为
(还原产物为 )、
)、 (1mol
(1mol  转化为1mol
转化为1mol  和1mol
和1mol  )等物质常被用作消毒剂。等物质的量的上述物质中消毒效率最高的是_______(填序号)。
)等物质常被用作消毒剂。等物质的量的上述物质中消毒效率最高的是_______(填序号)。
(2)过氧乙酸(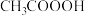 )是一种多用途的新型液体消毒杀菌剂,它具有
)是一种多用途的新型液体消毒杀菌剂,它具有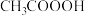 和
和 的双重性质。下列物质与过氧乙酸混合,不会使过氧乙酸失效的是_______(填序号)。
的双重性质。下列物质与过氧乙酸混合,不会使过氧乙酸失效的是_______(填序号)。
(3)消毒试剂亚氯酸钠( )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为:
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为: (未配平)。在该反应中,当有1mol
(未配平)。在该反应中,当有1mol  生成时,转移的电子数是
生成时,转移的电子数是_______ 。
(4)氯氨(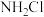 )可作杀菌剂,请用化学方程式表示氯氨在水中的杀菌机理:
)可作杀菌剂,请用化学方程式表示氯氨在水中的杀菌机理:_______ 。
(5)将NO转化为无毒气体,可选用天然气代替 来处理硝酸尾气(用
来处理硝酸尾气(用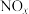 表示),请写出用天然气处理尾气的化学反应方程式:
表示),请写出用天然气处理尾气的化学反应方程式:_______ 。
(1)
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 (1mol
(1mol  转化为1mol
转化为1mol  和1mol
和1mol  )等物质常被用作消毒剂。等物质的量的上述物质中消毒效率最高的是_______(填序号)。
)等物质常被用作消毒剂。等物质的量的上述物质中消毒效率最高的是_______(填序号)。A. | B. | C. | D. |
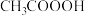 )是一种多用途的新型液体消毒杀菌剂,它具有
)是一种多用途的新型液体消毒杀菌剂,它具有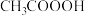 和
和 的双重性质。下列物质与过氧乙酸混合,不会使过氧乙酸失效的是_______(填序号)。
的双重性质。下列物质与过氧乙酸混合,不会使过氧乙酸失效的是_______(填序号)。A. | B. 溶液 溶液 | C.稀盐酸 | D. 溶液 溶液 |
 )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为:
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为: (未配平)。在该反应中,当有1mol
(未配平)。在该反应中,当有1mol  生成时,转移的电子数是
生成时,转移的电子数是(4)氯氨(
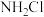 )可作杀菌剂,请用化学方程式表示氯氨在水中的杀菌机理:
)可作杀菌剂,请用化学方程式表示氯氨在水中的杀菌机理:(5)将NO转化为无毒气体,可选用天然气代替
 来处理硝酸尾气(用
来处理硝酸尾气(用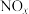 表示),请写出用天然气处理尾气的化学反应方程式:
表示),请写出用天然气处理尾气的化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】过氧化氢(H2O2)可作为采矿业的废液消毒剂,如消除采矿废液中有剧毒的氰化钾(KCN,其中N元素为-3价),化学方程式为KCN+H2O2+H2O=A+NH3↑(已配平),请回答下列问题:
(1)KCN中碳元素的化合价为_______ ,生成物A的化学式是_______ 。
(2)该反应是否是氧化还原反应?_______ (填“是”或“不是”)。若是,请指出被还原的元素;若不是,请说明理由:_______ 。
(3)若将KCN改为HCN也类似上述反应,则该反应的化学方程式为_______ 。
(1)KCN中碳元素的化合价为
(2)该反应是否是氧化还原反应?
(3)若将KCN改为HCN也类似上述反应,则该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,且无二次污染。K2FeO4中Fe为___ 价,盐酸中加入少量K2FeO4固体,产生黄绿色气体Cl2,K2FeO4被还原成FeCl3,该反应的化学方程式是___ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
①用单线桥标出电子转移的方向和数目___ 。
②此反应中氧化剂与还原剂的质量之比为___ 。
(3)已知常温下在溶液中可发生如下反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___ 。
(1)高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,且无二次污染。K2FeO4中Fe为
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
①用单线桥标出电子转移的方向和数目
②此反应中氧化剂与还原剂的质量之比为
(3)已知常温下在溶液中可发生如下反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
您最近一年使用:0次



