到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式___ 。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol, E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=___ 。
(3)①如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为:___ ;
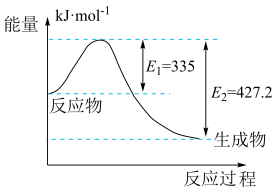
②若起始时向容器内放入1molN2和3molH2,达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为___ ;
(4)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=akJ·mol-1;
CO(g)+ O2(g)=CO2(g) ΔH=bkJ·mol-1;
O2(g)=CO2(g) ΔH=bkJ·mol-1;
C(石墨)+O2(g)=CO2(g) ΔH=ckJ·mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变ΔH=___ kJ·mol-1。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol, E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=
(3)①如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为:

②若起始时向容器内放入1molN2和3molH2,达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为
(4)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=akJ·mol-1;
CO(g)+
 O2(g)=CO2(g) ΔH=bkJ·mol-1;
O2(g)=CO2(g) ΔH=bkJ·mol-1;C(石墨)+O2(g)=CO2(g) ΔH=ckJ·mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变ΔH=
更新时间:2019-12-24 13:02:05
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。
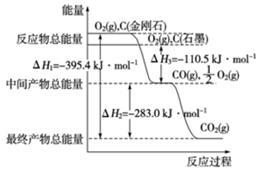
(1)在通常状况下,金刚石和石墨_______ (填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式____________ 。
(2)12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量______ 。
(3)已知在常温常压下:
①CH3OH(l)+O2(g)=CO(g)+2H2O(g) △H=-359.8kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-556.0kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0kJ·mol-1
写出体现甲醇燃烧热的热化学方程式_______________ 。

(1)在通常状况下,金刚石和石墨
(2)12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量
(3)已知在常温常压下:
①CH3OH(l)+O2(g)=CO(g)+2H2O(g) △H=-359.8kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-556.0kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0kJ·mol-1
写出体现甲醇燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】国家主席习近平在2017年新年祝词上表示,我国将实行“河长制”。水体污染的治理再次成为议的焦点。游离氨或氨盐是水体的常见污染物。
(1)氨氮的处理方法之一是用次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,反应如下:
① 配平该反应方程式:___ NH3(aq) +HClO(aq)= N2(g)+ H2O(I)+ HCl (aq),每生成lmol氧化产物,转移的电子数个数为________ 。
② 已知:NH3(aq)+HClO (aq)=NH2Cl (aq)+H2O (l)△H1=akJ·mol-1
NH2Cl(aq)+HCO(aq) = NHCl2(aq)+H2O(l)△H2=bkJ·mol-1
2NHCl2(aq) + H2O(l)= N2(g)+HClO(aq)+3HCl (aq)△H3=ckJ·mol-1
则上述次氯酸处理水中氨氮反应的△H=_______ 。(用a、b、c表示)
(2)吹脱法是处理氨氮的另一方法。其原理是利用气体,将反应NH4+ +OH- NH3+H2O中的氨气吹出。
NH3+H2O中的氨气吹出。
① 下列因素,不会影响吹脱法处理效果的是__________ (填序号)。
A.温度 B.溶液的pH
C.通入气体的速率和物质的量 D.通入气体的摩尔质量
② 25℃时,向25.00mL 0.1000mol/L (NH4)2SO4溶液中滴加0.1000mol/L NaOH 溶液所得的滴定曲线如图。(不考虑NH3逸出及溶液混合对体积的影响), 则a点的c(NH4+)=____ mol/L,b点的c (NH4+) + c ( NH3·H2O) =____ mol/L,下列关于c点的叙述正确的是_____ (填序号)。
A. pH = 13
B. c (NH4+) + c(NH3·H2O)=c(Na+)
C. c (NH4+) + c(Na+) + c(H+) =c(SO42-)+ c (OH-)
(3)如图所示,利用电解法产生的Cl2也可氧化除去水中的氨氮,实验室用石墨电极电解一定浓度的(NH4)2SO4 与NaCl 混合溶液来模拟。电解时,b为电源____ 极,阳极的电极反应式为___________
(1)氨氮的处理方法之一是用次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,反应如下:
① 配平该反应方程式:
② 已知:NH3(aq)+HClO (aq)=NH2Cl (aq)+H2O (l)△H1=akJ·mol-1
NH2Cl(aq)+HCO(aq) = NHCl2(aq)+H2O(l)△H2=bkJ·mol-1
2NHCl2(aq) + H2O(l)= N2(g)+HClO(aq)+3HCl (aq)△H3=ckJ·mol-1
则上述次氯酸处理水中氨氮反应的△H=
(2)吹脱法是处理氨氮的另一方法。其原理是利用气体,将反应NH4+ +OH-
 NH3+H2O中的氨气吹出。
NH3+H2O中的氨气吹出。① 下列因素,不会影响吹脱法处理效果的是
A.温度 B.溶液的pH
C.通入气体的速率和物质的量 D.通入气体的摩尔质量
② 25℃时,向25.00mL 0.1000mol/L (NH4)2SO4溶液中滴加0.1000mol/L NaOH 溶液所得的滴定曲线如图。(不考虑NH3逸出及溶液混合对体积的影响), 则a点的c(NH4+)=

A. pH = 13
B. c (NH4+) + c(NH3·H2O)=c(Na+)
C. c (NH4+) + c(Na+) + c(H+) =c(SO42-)+ c (OH-)
(3)如图所示,利用电解法产生的Cl2也可氧化除去水中的氨氮,实验室用石墨电极电解一定浓度的(NH4)2SO4 与NaCl 混合溶液来模拟。电解时,b为电源

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)已知:2N2O5(g)=2N2O4(g)+O2(g) △H1=-4.4kJ·mol-1
2NO2(g)=N2O4(g) △H2=-55.3kJ·mol-1
则反应N2O5(g)=2NO2(g)+ O2(g)的△H=
O2(g)的△H=____ kJ·mol-1。
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g) △H1=48kJ·mol-1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) △H2=-30kJ·mol-1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的△H为____ kJ·mol-1。
(3)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+ Cl2(g) △H1=83kJ·mol-1
Cl2(g) △H1=83kJ·mol-1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20kJ·mol-1
Cl2(g) △H2=-20kJ·mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H3=-121kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的△H=____ kJ·mol-1。
(1)已知:2N2O5(g)=2N2O4(g)+O2(g) △H1=-4.4kJ·mol-1
2NO2(g)=N2O4(g) △H2=-55.3kJ·mol-1
则反应N2O5(g)=2NO2(g)+
 O2(g)的△H=
O2(g)的△H=(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g) △H1=48kJ·mol-1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) △H2=-30kJ·mol-1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的△H为
(3)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+
 Cl2(g) △H1=83kJ·mol-1
Cl2(g) △H1=83kJ·mol-1CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20kJ·mol-1
Cl2(g) △H2=-20kJ·mol-1CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H3=-121kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)25℃下,纯水中c(H+)=1×10-7 mol·L-1,则此时c(OH-)=______________ ,该温度下向纯水中加盐酸,使溶液中的c(H+)=1×10-3 mol·L-1,则此时溶液的pH=_______________ 。若25℃下,向纯水中加入NaOH固体,使溶液的pH=13,此时溶液中c(OH-)=___________ 。 与纯水的电离相似,液氨中也存在着微弱的电离:2NH3  NH4++NH2-,请写出液氨的电离平衡常数表达式K =
NH4++NH2-,请写出液氨的电离平衡常数表达式K =____________________________ 。
(2)同素异形体相互转化的反应热相当少而转化速率慢,有时还很不完全,测定时很 困难,现可依据盖斯定律进行计算。已知:
P4 (白磷,s) + 5O2 (g) = 2P2O5 (s); △H1 =-283.2 kJ·mol-1 ①
4P (红磷,s) + 5O2 (g) = 2P2O5 (s); △H2 =-184.0kJ·mol-1 ②
由热化学方程式看来,更稳定的磷的同素异形体是______ (填“白磷”或“红磷”) ,试写出白磷转化成红磷的热化学方程式______________________________________ 。
 NH4++NH2-,请写出液氨的电离平衡常数表达式K =
NH4++NH2-,请写出液氨的电离平衡常数表达式K =(2)同素异形体相互转化的反应热相当少而转化速率慢,有时还很不完全,测定时很 困难,现可依据盖斯定律进行计算。已知:
P4 (白磷,s) + 5O2 (g) = 2P2O5 (s); △H1 =-283.2 kJ·mol-1 ①
4P (红磷,s) + 5O2 (g) = 2P2O5 (s); △H2 =-184.0kJ·mol-1 ②
由热化学方程式看来,更稳定的磷的同素异形体是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+ O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;
O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;
C(s)+ O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;
2Cu(s)+O2(g)=2CuO(s) ΔH=-314 kJ·mol-1。
工业上用木炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为_______ 。
(2)某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中电解质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。
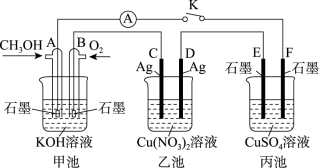
请回答下列问题:
①甲池为_______ (填“原电池”“电解池”或“电镀池”),A极的电极反应式为_______ 。
②丙池中F极为_______ (填“正极”“负极”“阴极”或“阳极”),该池的总反应式为_______ 。
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况)。
(1)纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+
 O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;
O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;C(s)+
 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;2Cu(s)+O2(g)=2CuO(s) ΔH=-314 kJ·mol-1。
工业上用木炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
(2)某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中电解质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。

请回答下列问题:
①甲池为
②丙池中F极为
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)已知:N N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式
N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式_______________________________ ;该反应的熵变△S___ 0(填“>”、“<”或“=”)。
(2)将1 mol N2与3 mol H2混合置于容积为10 L的密闭容器中。
①温度为T1时,混合气体中氨的物质的量分数为25%,则N2的转化率为_________ 。
②当温度由T1变化到T2(T2>T1)时(如图),平衡常数KA_________ KB(填“>”、“<”或“=”)。
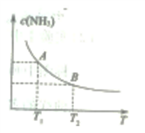
③温度在T1时,若起始时向10L密闭容器中加入N2 0.5 mol、H2 1.5 mol、NH3 1mol。当反应达到平衡时,与起始时比较,___________________ (填化学式)的物质的量增加。
 N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式
N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式(2)将1 mol N2与3 mol H2混合置于容积为10 L的密闭容器中。
①温度为T1时,混合气体中氨的物质的量分数为25%,则N2的转化率为
②当温度由T1变化到T2(T2>T1)时(如图),平衡常数KA

③温度在T1时,若起始时向10L密闭容器中加入N2 0.5 mol、H2 1.5 mol、NH3 1mol。当反应达到平衡时,与起始时比较,
您最近一年使用:0次
【推荐2】化学能与热能在生产生活中扮演者重要的角色,按照要求回答下列各题。
(1)对烟道气中的 进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由
进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,每生成
的能量变化如图所示,每生成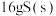 ,该反应
,该反应___________ (填“放出”或“吸收”)的热量为___________ kJ。

(2) 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 ),还对温室气体的减排具有重要意义。
),还对温室气体的减排具有重要意义。 催化重整反应为:
催化重整反应为: 。
。
已知:
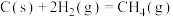
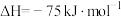
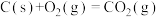
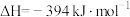
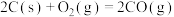
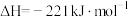
该催化重整反应的 =
=___________  。
。
(3)利用 可制备乙烯及合成气(CO、
可制备乙烯及合成气(CO、 )。有关化学键键能(E)的数据如下表:
)。有关化学键键能(E)的数据如下表:
①已知
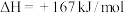 ,则a=
,则a=___________ 。
②已知 的燃烧热是890.31kJ/mol,表示
的燃烧热是890.31kJ/mol,表示 燃烧热的热化学方程式
燃烧热的热化学方程式___________ 。
③制备合成气反应历程分两步,
步骤I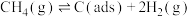 ;
;
步骤Ⅱ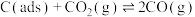 。
。
上述反应中(ads)吸附性活性炭,反应历程的能量变化如图:

决定制备合成气反应速率的是___________ (填“步骤I”或“步骤Ⅱ”),反应I的活化能___________ 反应Ⅱ的活化能(填“>”“=”或“<”)。
(1)对烟道气中的
 进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由
进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,每生成
的能量变化如图所示,每生成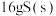 ,该反应
,该反应
(2)
 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 ),还对温室气体的减排具有重要意义。
),还对温室气体的减排具有重要意义。 催化重整反应为:
催化重整反应为: 。
。已知:
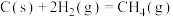
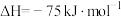
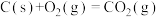
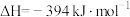
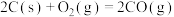
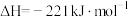
该催化重整反应的
 =
= 。
。(3)利用
 可制备乙烯及合成气(CO、
可制备乙烯及合成气(CO、 )。有关化学键键能(E)的数据如下表:
)。有关化学键键能(E)的数据如下表:| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |

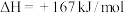 ,则a=
,则a=②已知
 的燃烧热是890.31kJ/mol,表示
的燃烧热是890.31kJ/mol,表示 燃烧热的热化学方程式
燃烧热的热化学方程式③制备合成气反应历程分两步,
步骤I
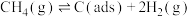 ;
;步骤Ⅱ
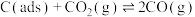 。
。上述反应中(ads)吸附性活性炭,反应历程的能量变化如图:

决定制备合成气反应速率的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)键能是表征化学键强度的物理量,可以用键断裂时所需能量的大小来衡量。从断键和成键的角度分析反应2H2(g)+O2(g) 2H2O(g)中能量的变化,化学键的键能如表所示:
2H2O(g)中能量的变化,化学键的键能如表所示:
则生成1molH2O(g)可以放出____ kJ热量。
(2)下列反应中,属于放热反应的是____ (填字母,下同),属于吸热反应的是____ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向____ (填“A”或“B”)极。
②装置乙中正极的电极反应式为____ 。
③四种金属活动性由强到弱的顺序是____ 。
(1)键能是表征化学键强度的物理量,可以用键断裂时所需能量的大小来衡量。从断键和成键的角度分析反应2H2(g)+O2(g)
 2H2O(g)中能量的变化,化学键的键能如表所示:
2H2O(g)中能量的变化,化学键的键能如表所示:| 化学键 | H—H | O=O | H—O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 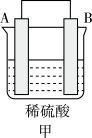 |  | 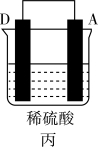 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
您最近一年使用:0次



