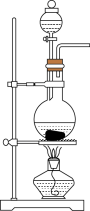
实验室用如图所示装置制备氯气并进行一系列相关实验(夹持设备及必要的加热装置已省略)。
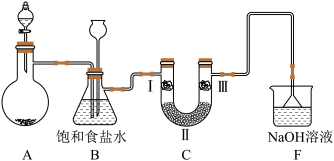
(1)整套装置装配完毕后,首先进行的操作是___ ,再添加试剂。
(2)实验室常用MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O制取氯气:
MnCl2+Cl2↑+2H2O制取氯气:
①实验时,通常采用密度为1.19g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为____ 。
②标准状况下,上述反应每生成4.48L氯气,转移电子的物质的量为___ mol。
(3)洗气装置B的作用是除去Cl2中的HCl气体,同时用作安全瓶(监测实验时装置 C 中是否发生堵塞 )。若装置C发生堵塞,装置B中将观察到的现象是___ 。
(4)装置C的作用是验证氯气是否具有漂白性。为此,实验时装置C中I、II、III处依次放入的物质是____ (填字母)。
(5)向品红溶液中同时通入氯气和二氧化硫(按物质的量之比1:1),观察到的现象是___ 。用化学方程式解释一下原因___ 。
(6)F为尾气吸收装置。实验时,该装置中反应的离子方程式___ 。

(1)整套装置装配完毕后,首先进行的操作是
(2)实验室常用MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O制取氯气:
MnCl2+Cl2↑+2H2O制取氯气:①实验时,通常采用密度为1.19g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为
②标准状况下,上述反应每生成4.48L氯气,转移电子的物质的量为
(3)洗气装置B的作用是除去Cl2中的HCl气体,同时用作安全瓶(
(4)装置C的作用是验证氯气是否具有漂白性。为此,实验时装置C中I、II、III处依次放入的物质是
| A | B | C | D | |
| I | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 无水氯化钙 | 无水氯化钙 | 浓硫酸 |
| III | 湿润的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 |
(6)F为尾气吸收装置。实验时,该装置中反应的离子方程式
更新时间:2019-12-25 12:25:31
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
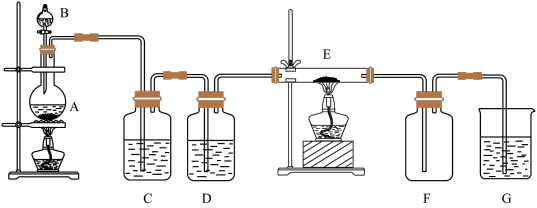
【推荐1】如下图所示的装置中,A是氯气发生装置,C、D 为气体净化装置(C中装有饱和食盐水;D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液。
试回答:
(1)仪器A的名称是__________ ;
(2)C装置的作用是__________ ;
(3)D 装置的作用是__________ ;
(4)E中发生化学反应的方程式为:_____________________________ ;
(5)烧杯G 中发生反应的化学方程式为:_______________________________________ 。

试回答:
(1)仪器A的名称是
(2)C装置的作用是
(3)D 装置的作用是
(4)E中发生化学反应的方程式为:
(5)烧杯G 中发生反应的化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。
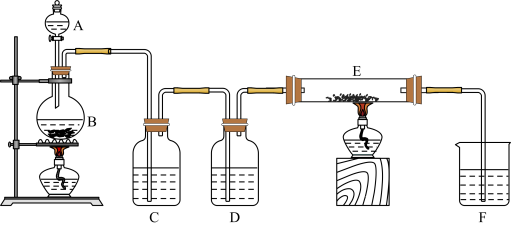
试回答:
①B中发生反应的化学方程式为_______ ;反应中氧化剂为_______ (填化学式)。
②为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是_______ ;D装置中的试剂是_______ 。
③E中发生的化学反应方程式为_______ 。
④F是尾气处理装置,反应离子方程式为_______ 。
⑤实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式_______ 。(已知 被还原为Mn2+)
被还原为Mn2+)
(2)Cl2是一种重要的化工原料,下图是一些含氯产品。
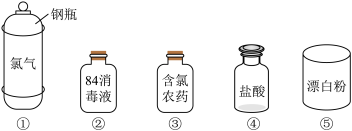
①中钢瓶上应贴的标签为_______ 。
A.腐蚀品 B.有毒品 C.易燃品
②漂白粉可用于游泳池及环境消毒剂,制漂白粉的反应原理为_______ 。
(3)2016年10月20日生活日报讯,一位温州小伙将84消毒液与洁厕灵共用来刷洗厕所时,突然瘫坐在地,无力挪步,呼吸急促。经医生诊断,小伙子为轻度氯气中毒。某大学化工系教授,该教授表示洁厕灵含有盐酸,84消毒液含有NaClO(次氯酸钠),二者不可混用,一旦混合会产生有毒的氯气,如果不慎发生事故,应立即开窗通风,用湿毛巾捂住口鼻向高处转移,事后要多喝水,并及时就医。
①请用离子方程式分析小伙子中毒的原因_______ 。
②发生事故后,要用湿毛巾捂住口鼻向高处转移,事后还要多喝水,用化学方程式表示用湿毛巾捂住口鼻,事后多喝水的原因:_______
(1)如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。

试回答:
①B中发生反应的化学方程式为
②为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是
③E中发生的化学反应方程式为
④F是尾气处理装置,反应离子方程式为
⑤实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式
 被还原为Mn2+)
被还原为Mn2+)(2)Cl2是一种重要的化工原料,下图是一些含氯产品。

①中钢瓶上应贴的标签为
A.腐蚀品 B.有毒品 C.易燃品
②漂白粉可用于游泳池及环境消毒剂,制漂白粉的反应原理为
(3)2016年10月20日生活日报讯,一位温州小伙将84消毒液与洁厕灵共用来刷洗厕所时,突然瘫坐在地,无力挪步,呼吸急促。经医生诊断,小伙子为轻度氯气中毒。某大学化工系教授,该教授表示洁厕灵含有盐酸,84消毒液含有NaClO(次氯酸钠),二者不可混用,一旦混合会产生有毒的氯气,如果不慎发生事故,应立即开窗通风,用湿毛巾捂住口鼻向高处转移,事后要多喝水,并及时就医。
①请用离子方程式分析小伙子中毒的原因
②发生事故后,要用湿毛巾捂住口鼻向高处转移,事后还要多喝水,用化学方程式表示用湿毛巾捂住口鼻,事后多喝水的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。高铁酸钾(K2FeO4,极易溶于水)是常见的水处理剂,其原理如图所示。完成下列问题:
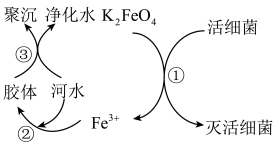
(1)K2FeO4的电离方程式______ 。过程①中K2FeO4表现了______ (填“氧化”或“还原”)性。
(2)根据上述原理分析,作水处理剂时,K2FeO4的作用有______ 、______ (填两个)。
(3)制备高铁酸钾常用的反应原理为:Fe(OH)3+KClO+KOH→K2FeO4+KCl+H2O(反应未配平)。
①通过该反应说明:在碱性条件下,氧化性KClO______ K2FeO4。
A.大于 B.小于 C.等于 D.无法比较
②配平该反应的化学方程式,并用单线桥法 表示电子转移的方向和数目说明______ ;
世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂
已知:NaCl+3H2O NaClO3+3H2↑
NaClO3+3H2↑
发生器:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
ClO2的生产流程示意图如图:
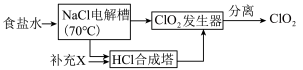
(4)该工艺中,需要补充的物质X为______ (填化学式,下同)。
(5)能参与循环的物质是______ 。
已知:ClO2是极易溶于水的气体,具有强氧化性。用如图装置探究ClO2性质。回答下列问题:
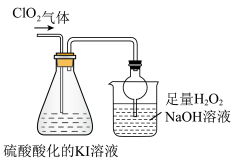
(6)锥形瓶内ClO2进气导管不伸入液面以下,原因是______ 。
(7)烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2:1,则还原产物的化学式是______ 。
反应后向锥形瓶中加入少量四氯化碳,溶液上下分层,下层为紫红色
已知:I2+Na2S=2NaI+S
(8)若将锥形瓶内溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:______ 。
②请设计实验证明你的假设(仅用离子方程式表示):______ 。

(1)K2FeO4的电离方程式
(2)根据上述原理分析,作水处理剂时,K2FeO4的作用有
(3)制备高铁酸钾常用的反应原理为:Fe(OH)3+KClO+KOH→K2FeO4+KCl+H2O(反应未配平)。
①通过该反应说明:在碱性条件下,氧化性KClO
A.大于 B.小于 C.等于 D.无法比较
②配平该反应的化学方程式,并用
世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂
已知:NaCl+3H2O
 NaClO3+3H2↑
NaClO3+3H2↑发生器:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
ClO2的生产流程示意图如图:

(4)该工艺中,需要补充的物质X为
(5)能参与循环的物质是
已知:ClO2是极易溶于水的气体,具有强氧化性。用如图装置探究ClO2性质。回答下列问题:

(6)锥形瓶内ClO2进气导管不伸入液面以下,原因是
(7)烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2:1,则还原产物的化学式是
反应后向锥形瓶中加入少量四氯化碳,溶液上下分层,下层为紫红色
已知:I2+Na2S=2NaI+S
(8)若将锥形瓶内溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:
②请设计实验证明你的假设(仅用离子方程式表示):
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾。实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al + 6HCl(g) → 2AlCl3+ 3H2。完成下列填空:
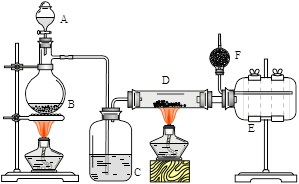
(1)写出B处烧瓶中发生反应的化学方程式:_______________________________________ 。
(2)C中盛有的试剂为__________ 。进行实验时应先点燃_____ (选填“B”或“D”)处酒精灯。
(3) 用粗短导管连接D、E的目的是_________ (选填序号)。
a. 防堵塞 b. 防倒吸 c. 平衡气压 d. 冷凝回流
E瓶的作用是_______________________________________________________ 。
(4)F中盛有碱石灰,其目的是_________ (选填序号)。
a. 吸收HCl b. 吸收Cl2c. 吸收CO2d. 吸收H2O
(5)①将D中固体改为市售氯化铝(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是_____________________________________________ 。
②若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原市售氯化铝的40%,则可推算n的值为_______ 。
(6)有人建议将上述装置A、B中的试剂改为浓盐酸和二氧化锰,其余装置和试剂均不变,也能制备无水AlCl3。事实证明这样做比较危险,请简述理由_________________________ 。

(1)写出B处烧瓶中发生反应的化学方程式:
(2)C中盛有的试剂为
(3) 用粗短导管连接D、E的目的是
a. 防堵塞 b. 防倒吸 c. 平衡气压 d. 冷凝回流
E瓶的作用是
(4)F中盛有碱石灰,其目的是
a. 吸收HCl b. 吸收Cl2c. 吸收CO2d. 吸收H2O
(5)①将D中固体改为市售氯化铝(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是
②若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原市售氯化铝的40%,则可推算n的值为
(6)有人建议将上述装置A、B中的试剂改为浓盐酸和二氧化锰,其余装置和试剂均不变,也能制备无水AlCl3。事实证明这样做比较危险,请简述理由
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
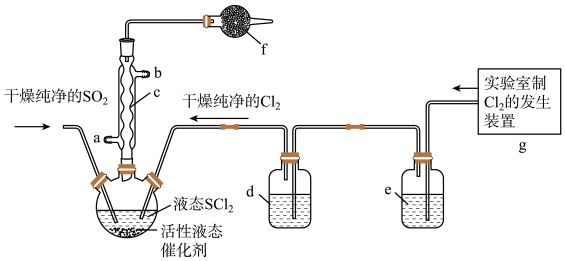
【推荐2】氯化亚砜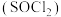 在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备
在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备 。
。
已知:① 是一种液态化合物,沸点为77℃
是一种液态化合物,沸点为77℃
② 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
③实验室合成 原理:
原理:
请回答以下问题:
(1)仪器c的名称是_______ ,f中的最佳试剂是_______ (填字母符号)。
A.碱石灰 B.浓硫酸 C. 溶液 D.无水氯化钙
溶液 D.无水氯化钙
(2)实验室用浓盐酸与 粉末反应制
粉末反应制 的化学方程式为
的化学方程式为________ 。
(3) 与水反应的化学方程式为
与水反应的化学方程式为_______ 。
(4)下列三种制备 的方案中最佳选择是
的方案中最佳选择是_________ .
(5)装置g中产生的 经过e、d后进入三颈烧瓶,e中的试剂为
经过e、d后进入三颈烧瓶,e中的试剂为_____ 。
(6)实验结束后,将三颈烧瓶中混合物分离开的实验操作是_____ (已知 的沸点为50℃);若反应中消耗
的沸点为50℃);若反应中消耗 的体积为
的体积为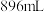 (已转化为标准状况,
(已转化为标准状况, 足量),最后得到
足量),最后得到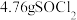 ,则
,则 的产率为
的产率为_______ (已知产率=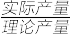 ×100%)。
×100%)。
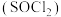 在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备
在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备 。
。
已知:①
 是一种液态化合物,沸点为77℃
是一种液态化合物,沸点为77℃②
 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生③实验室合成
 原理:
原理:
请回答以下问题:
(1)仪器c的名称是
A.碱石灰 B.浓硫酸 C.
 溶液 D.无水氯化钙
溶液 D.无水氯化钙(2)实验室用浓盐酸与
 粉末反应制
粉末反应制 的化学方程式为
的化学方程式为(3)
 与水反应的化学方程式为
与水反应的化学方程式为(4)下列三种制备
 的方案中最佳选择是
的方案中最佳选择是方案 | 甲 | 乙 | 丙 |
| 发生装置 |
|
|
|
| 所选试剂 | 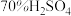 和 和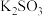 粉末 粉末 | 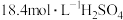 铜片 铜片 | 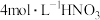 和 和 粉末 粉末 |
 经过e、d后进入三颈烧瓶,e中的试剂为
经过e、d后进入三颈烧瓶,e中的试剂为(6)实验结束后,将三颈烧瓶中混合物分离开的实验操作是
 的沸点为50℃);若反应中消耗
的沸点为50℃);若反应中消耗 的体积为
的体积为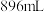 (已转化为标准状况,
(已转化为标准状况, 足量),最后得到
足量),最后得到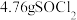 ,则
,则 的产率为
的产率为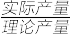 ×100%)。
×100%)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯气是一种重要的化工原料,广泛应用于制备含氯化合物。现用如图装置(夹持装置省略)制备少量漂白粉。

已知:在温度较高时,将氯气通入石灰乳中会发生反应: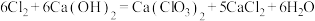 。
。
(1)采用装置①也可以制备Cl2,发生的反应为: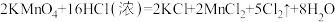 ,若生成标准状况下224LCl2,则被还原的物质的物质的量为
,若生成标准状况下224LCl2,则被还原的物质的物质的量为______ 。
(2)漂白粉长期露置空气中会变质失效,主要发生反应的化学方程式为:_______ 。
(3)若无装置②,可能产生的影响是_______ 。
(4)装置③中用了多孔球泡,其目的是______ ;由于装置③中发生的反应会放出热量,因此为防止副反应的发生,装置③应如何改进?______ 。
(5)装置④中盛装的溶液为_____ (填试剂名称),发生反应的离子方程式为:_______ 。

已知:在温度较高时,将氯气通入石灰乳中会发生反应:
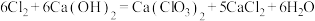 。
。(1)采用装置①也可以制备Cl2,发生的反应为:
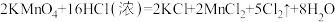 ,若生成标准状况下224LCl2,则被还原的物质的物质的量为
,若生成标准状况下224LCl2,则被还原的物质的物质的量为(2)漂白粉长期露置空气中会变质失效,主要发生反应的化学方程式为:
(3)若无装置②,可能产生的影响是
(4)装置③中用了多孔球泡,其目的是
(5)装置④中盛装的溶液为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二氯乙烷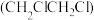 是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点
是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点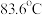 ,碱性条件下水解程度较大。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理为
,碱性条件下水解程度较大。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理为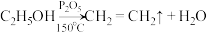
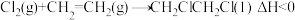
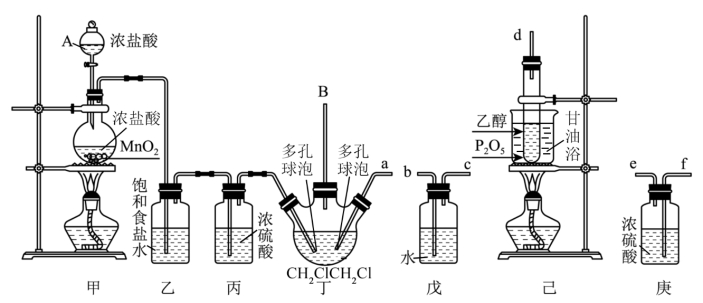
实验装置如图:
请回答下列问题:
(1)写出甲装置发生反应的化学方程式___________ 。
(2)按实验原理将装置戊、己、庚连接起来,d→___________ →___________ →___________ →___________ a(按接口顺序连接)
(3)丁装置中长玻璃导管B的作用是___________ ,先装入1,2-二氯乙烷液体,其作用是___________ 以促进气体间的接触,更容易使物质发生反应。
(4)制乙烯采用甘油浴加热,该加热方式的优点是___________ 。
(5)制得的1,2-二氯乙烷中溶解有 、乙烯,逐出其中的
、乙烯,逐出其中的 和乙烯采用的方法是
和乙烯采用的方法是___________ 。
(6)有同学提出该装置存在缺陷,你认为是___________ 。
(7)产品纯度的测定:量取 逐出
逐出 和乙烯后的产品,产品密度为
和乙烯后的产品,产品密度为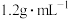 ,加足量稀
,加足量稀 溶液,加热充分反应:
溶液,加热充分反应: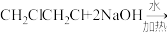
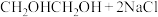 。所得溶液先用稀硝酸中和至酸性,然后加入
。所得溶液先用稀硝酸中和至酸性,然后加入 的
的 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为___________ 。
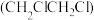 是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点
是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点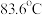 ,碱性条件下水解程度较大。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理为
,碱性条件下水解程度较大。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理为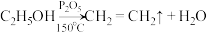
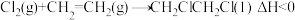
实验装置如图:

请回答下列问题:
(1)写出甲装置发生反应的化学方程式
(2)按实验原理将装置戊、己、庚连接起来,d→
(3)丁装置中长玻璃导管B的作用是
(4)制乙烯采用甘油浴加热,该加热方式的优点是
(5)制得的1,2-二氯乙烷中溶解有
 、乙烯,逐出其中的
、乙烯,逐出其中的 和乙烯采用的方法是
和乙烯采用的方法是(6)有同学提出该装置存在缺陷,你认为是
(7)产品纯度的测定:量取
 逐出
逐出 和乙烯后的产品,产品密度为
和乙烯后的产品,产品密度为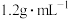 ,加足量稀
,加足量稀 溶液,加热充分反应:
溶液,加热充分反应: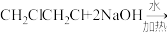
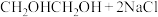 。所得溶液先用稀硝酸中和至酸性,然后加入
。所得溶液先用稀硝酸中和至酸性,然后加入 的
的 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】云南是我国的矿产资源大省,被誉为“有色金属王国”。利用某冶炼废渣(主要成分为二氧化硅和锡、铜、铅、铁的氧化物)回收锡、铜、铅的工艺流程如图所示:
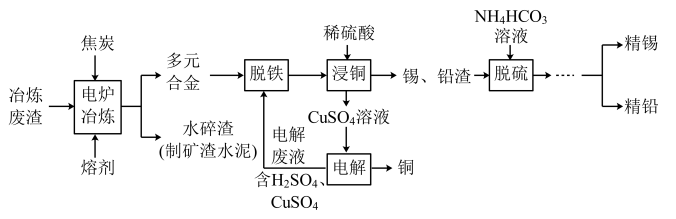
回答下列问题:
(1)电炉冶炼时,焦炭的作用是____ (填“氧化剂”或“还原剂”),将焦炭粉碎的目的是_____ 。熔剂的主要成分是氟石(CaF2),高温下能与 SiO2反应生成两种钙,其中之一为 CaSiF6,该反应的化学方程式为____ 。
(2)脱铁后的溶液中含有少量的 Sn2+,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为____ 。
(3)已知 SnO2不溶于稀硫酸。脱铁后氧化焙烧的目的是____ 。
(4)电解 CuSO4溶液时,阳极的电极反应式为____ 。
(5)锡、铅渣中的铅主要以 PbSO4存在,脱硫时发生的反应为PbSO4+HCO (aq)
(aq) PbCO3 (s)+H+(aq)+SO
PbCO3 (s)+H+(aq)+SO (aq)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是
(aq)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是___ 。
(6)若该冶炼废渣中锡的质量分数为 5%,30t 废渣制得精锡 lt,则锡的回收率为_____ 。

回答下列问题:
(1)电炉冶炼时,焦炭的作用是
(2)脱铁后的溶液中含有少量的 Sn2+,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为
(3)已知 SnO2不溶于稀硫酸。脱铁后氧化焙烧的目的是
(4)电解 CuSO4溶液时,阳极的电极反应式为
(5)锡、铅渣中的铅主要以 PbSO4存在,脱硫时发生的反应为PbSO4+HCO
 (aq)
(aq) PbCO3 (s)+H+(aq)+SO
PbCO3 (s)+H+(aq)+SO (aq)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是
(aq)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是(6)若该冶炼废渣中锡的质量分数为 5%,30t 废渣制得精锡 lt,则锡的回收率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】过氧化钙是重要的化工原料,易溶于酸、难溶于水、乙醇等溶剂,温度在350℃以上容易分解。其主要用作杀菌剂、防腐剂、解酸剂、油类漂白剂等。农业上用作种子及谷物的无毒性消毒剂及鱼池的增氧剂。
(1)过氧化钙工业上常用以下合成路线进行合成。
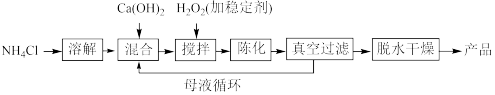
已知:氯化铵的作用是提高Ca2+的浓度。
①反应温度需要控制在常温下产率最高,温度过高或过低都会使产率降低的原因是___________________ ,母液的主要溶质是__________ 。
②整个过程的总化学方程式为_____________________________________________ 。
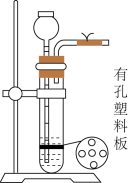
(2)实验室也可利用反应Ca(s)+O2(g) CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
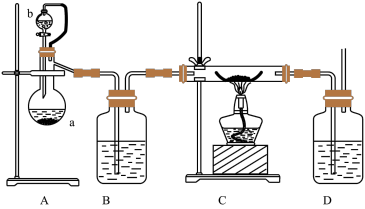
请回答下列问题:
①仪器a的名称为________ ,仪器a上方橡皮管的作用是______________ ,D装置中的试剂为________ 。
②根据完整的实验装置进行实验,实验步骤如下:检验装置的气密性后,装入药品;打开分液漏斗活塞,通入一段时间气体,加热药品;待反应结束后,操作顺序为____________ (填序号);拆除装置,取出产物。
a 停止通入氧气并关闭分液漏斗的活塞 b 熄灭酒精灯 c 反应管冷却至室温
(3)利用如图装置测定反应2CaO2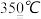 2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是
2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是___________ ,若B装置直接读数确定25℃、1个标准大气压下气体的体积,则测量结果_______ (填“偏大”、“偏小”或“无影响”)。
(1)过氧化钙工业上常用以下合成路线进行合成。

已知:氯化铵的作用是提高Ca2+的浓度。
①反应温度需要控制在常温下产率最高,温度过高或过低都会使产率降低的原因是
②整个过程的总化学方程式为
(2)实验室也可利用反应Ca(s)+O2(g)
 CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
请回答下列问题:
①仪器a的名称为
②根据完整的实验装置进行实验,实验步骤如下:检验装置的气密性后,装入药品;打开分液漏斗活塞,通入一段时间气体,加热药品;待反应结束后,操作顺序为
a 停止通入氧气并关闭分液漏斗的活塞 b 熄灭酒精灯 c 反应管冷却至室温
(3)利用如图装置测定反应2CaO2
 2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是
2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2 和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品。
(1)写出氯碱工业中电解饱和食盐水的离子方程式:________________ ;某学习小组为了测定电解后所得溶液NaOH的浓度,设计了如下实验操作步骤:
①取电解后的溶液10.00mL,加水稀释至100mL;
②量取20.00mL于洁净的锥形瓶,滴加2~3滴酚酞试剂;
③用浓度为0.1010mo/L的标准HCl滴定至终点并记录滴定管的读数为25.00mL
请回答有关问题
①步骤①可能用到的仪器除移液管外,还有_______________
②滴定终点的现象是____________ ,此溶液中c(Na+)______ c(Cl-)(填“<”、“>”或“=”)
③下列操作可能导致所得浓度偏大的是______________
a. 锥形瓶用待测溶液润洗 b.碱式滴定管用待测液润洗
c. 滴定管滴定前有气泡,滴定后无气泡 d. 滴定终点俯视读数
④该实验设计存在的明显不足的是____________
(2)已知:H2SO3的Ka1=1.54×10–2,Ka2=1.02×10–7;HClO的Ka=2.95×10–8
①室温下,0.1 mol·L–1 NaClO溶液的pH_____ 0.1 mol·L–1 Na2SO3溶液的pH。(填“大于”、“小于”或“等于”)
②写出一种可以证明NaHSO3溶液中HSO3–的电离程度大于HSO3–水解程度的方法:_____
(3)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
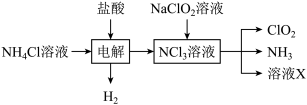
电解时发生反应的化学方程式为_______________________ ,溶液X的溶质主要是__________
(1)写出氯碱工业中电解饱和食盐水的离子方程式:
①取电解后的溶液10.00mL,加水稀释至100mL;
②量取20.00mL于洁净的锥形瓶,滴加2~3滴酚酞试剂;
③用浓度为0.1010mo/L的标准HCl滴定至终点并记录滴定管的读数为25.00mL
请回答有关问题
①步骤①可能用到的仪器除移液管外,还有
②滴定终点的现象是
③下列操作可能导致所得浓度偏大的是
a. 锥形瓶用待测溶液润洗 b.碱式滴定管用待测液润洗
c. 滴定管滴定前有气泡,滴定后无气泡 d. 滴定终点俯视读数
④该实验设计存在的明显不足的是
(2)已知:H2SO3的Ka1=1.54×10–2,Ka2=1.02×10–7;HClO的Ka=2.95×10–8
①室温下,0.1 mol·L–1 NaClO溶液的pH
②写出一种可以证明NaHSO3溶液中HSO3–的电离程度大于HSO3–水解程度的方法:
(3)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

电解时发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组同学设计了如图所示的实验装置来进行实验探究:
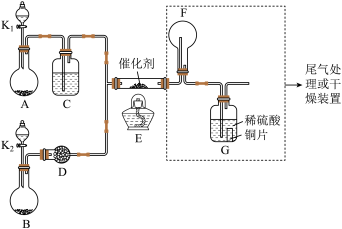
I.氨的催化氧化(4NH3+5O2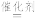 4NO+6H2O):
4NO+6H2O):
(1)A中加入的是一种黑色的固体,B装置是制备___________ 的装置,D中装的试剂为___________ 。
(2)甲、乙同学分别按图示装置进行实验,一段时间后,装置G中的溶液都变成蓝色,甲观察到装置F中有红棕色气体,乙观察到装置F中有白烟生成。G中溶液变蓝的原因是(用离子方程式表示)______________________ ,白烟的成分为___________ 。甲、乙两同学分析了F装置现象不同的原因,乙同学通过改变实验操作:______________________ ,也在F中看到了红棕色气体生成。
Ⅱ.测定SO2转化为SO3的转化率:
已知:SO3的熔点是16.8℃,沸点是44.8℃。
(3)根据实验需要,应将F、G处替换成图中的装置(填序号)F.___________ G._________ 。

(4)在A中加入 a mol Na2SO3粉末与足量浓硫酸反应,当反应结束时,让B装置继续再反应一段时间,最后测得G处装置增重bg,则此时SO2的转化率为___________ (用含a、b的代数式表示)。
(5)丙同学观察整套装置后,推断该实验结果必定偏高,他更换了一个三孔橡皮塞,改动装置后重新实验,获得了更符合实际的转化率。请推断他对装置的改动是___________ 。

I.氨的催化氧化(4NH3+5O2
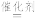 4NO+6H2O):
4NO+6H2O):(1)A中加入的是一种黑色的固体,B装置是制备
(2)甲、乙同学分别按图示装置进行实验,一段时间后,装置G中的溶液都变成蓝色,甲观察到装置F中有红棕色气体,乙观察到装置F中有白烟生成。G中溶液变蓝的原因是(用离子方程式表示)
Ⅱ.测定SO2转化为SO3的转化率:
已知:SO3的熔点是16.8℃,沸点是44.8℃。
(3)根据实验需要,应将F、G处替换成图中的装置(填序号)F.

(4)在A中加入 a mol Na2SO3粉末与足量浓硫酸反应,当反应结束时,让B装置继续再反应一段时间,最后测得G处装置增重bg,则此时SO2的转化率为
(5)丙同学观察整套装置后,推断该实验结果必定偏高,他更换了一个三孔橡皮塞,改动装置后重新实验,获得了更符合实际的转化率。请推断他对装置的改动是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】绿矾(FeSO4·7H2O) 是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质) 为原料生产纯净绿矾的一种方法:
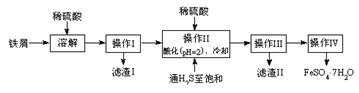
查询资料,得有关物质的数据如下表:
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为____________________ 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是(写两点)___________ 、____________ 。
(3)操作IV的顺序依次为________ 、冷却结晶、过滤。
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取3.72g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为_________ (填仪器名称)。
②计算上述样品中FeSO4•7H2O的质量分数为__________ 。
③上述测定中,若滴定管规格为50mL,则步骤a中称取样品的质量不能超过______ g。(保留4位小数)

查询资料,得有关物质的数据如下表:
| 25℃时 | 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是(写两点)
(3)操作IV的顺序依次为
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取3.72g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为
②计算上述样品中FeSO4•7H2O的质量分数为
③上述测定中,若滴定管规格为50mL,则步骤a中称取样品的质量不能超过
您最近一年使用:0次