将5.6g铁投入200mL某浓度的稀盐酸中,铁和稀盐酸恰好完全反应。试求:
(1)5.6g铁的物质的量。________
(2)所用稀盐酸的物质的量浓度。________
(3)生成H2的体积(标准状况).______________
(1)5.6g铁的物质的量。
(2)所用稀盐酸的物质的量浓度。
(3)生成H2的体积(标准状况).
更新时间:2020-01-14 10:18:05
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】1)22.0g K2R中含有0.4mol钾离子,则该物质的摩尔质量为________ ,R的相对原子质量为________ 。
(2)在恒温条件下的密闭容器中,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当在左边充入1 mol N2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置。

①隔板左右两边气体的气体的分子数之比为______ 。
②右边混合气体中CO和CO2物质的量分别为________ 、________ ,该混合气体平均相对分子质量为______ 。
(3)现有20°C的饱和硫酸铜溶液,其质量分数为16%、密度为1.25g/cm3。则:
①20°C时,硫酸铜的溶解度为________ ;
②该饱和硫酸铜溶液的物质的量浓度为____ ;
③实验室需要250mL 0.5mol/LCuSO4溶液。在配制该溶液时需要称取胆矾(CuSO4·5H2O)的质量为____ ;
④取20mL 0.5mol/LCuSO4溶液恰好与50mLNaOH溶液反应,使Cu2+完全转化为沉淀。请计算氢氧化钠溶液的物质的量浓度(写出过程)____ 。
(2)在恒温条件下的密闭容器中,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当在左边充入1 mol N2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置。

①隔板左右两边气体的气体的分子数之比为
②右边混合气体中CO和CO2物质的量分别为
(3)现有20°C的饱和硫酸铜溶液,其质量分数为16%、密度为1.25g/cm3。则:
①20°C时,硫酸铜的溶解度为
②该饱和硫酸铜溶液的物质的量浓度为
③实验室需要250mL 0.5mol/LCuSO4溶液。在配制该溶液时需要称取胆矾(CuSO4·5H2O)的质量为
④取20mL 0.5mol/LCuSO4溶液恰好与50mLNaOH溶液反应,使Cu2+完全转化为沉淀。请计算氢氧化钠溶液的物质的量浓度(写出过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】已知: 2NH4Cl(s)+ Ca(OH)2(s) CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
(1)产生的氨气在标准状况时的体积为多少?
(2)将所得氨气全部溶于200mL水中,若所得氨水的密度为0.936 g·cm-3,则该氨水的物质的量浓度为多少?
 CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:(1)产生的氨气在标准状况时的体积为多少?
(2)将所得氨气全部溶于200mL水中,若所得氨水的密度为0.936 g·cm-3,则该氨水的物质的量浓度为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】计算:
(1)3.6 g H2O的物质的量是_______ mol,含有_______ mol质子。
(2)22 g CO2在标准状况下的体积是_______ L。
(3)10.6 g Na2CO3固体溶于水配成100 mL溶液,其物质的量浓度为_______ mol/L。将其稀释至1000 mL,其物质的量浓度为_______ mol/L。
(4)现有200 mL0.27 kg的质量分数为10%的CuCl2溶液。计算:溶液中CuCl2物质的量浓度为_______ 。
(1)3.6 g H2O的物质的量是
(2)22 g CO2在标准状况下的体积是
(3)10.6 g Na2CO3固体溶于水配成100 mL溶液,其物质的量浓度为
(4)现有200 mL0.27 kg的质量分数为10%的CuCl2溶液。计算:溶液中CuCl2物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】已知丁烷在催化剂、加热、加压的条件下会以如下两种方式发生裂解:

现有1mol丁烷,其中有36%以方式①裂解,有24%以方式②裂解,还有40%没有裂解,则最终所得混合气体的平均摩尔质量是______________________ 。

现有1mol丁烷,其中有36%以方式①裂解,有24%以方式②裂解,还有40%没有裂解,则最终所得混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知实验室制氯气的化学方程式为:MnO2 + 4HCl (浓) 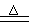 MnCl2 + Cl2↑+2H2O,现用足量浓盐酸在加热条件下跟二氧化锰反应制取氯气。若标准状况下制得Cl22.24L求:
MnCl2 + Cl2↑+2H2O,现用足量浓盐酸在加热条件下跟二氧化锰反应制取氯气。若标准状况下制得Cl22.24L求:
(1)二氧化锰的质量;
(2)把(1)中反应后的溶液稀释到50 mL,从中取出10.0 mL,加入10.0 mL 0.600 mol / L的硝酸银溶液,恰好将氯离子完全沉淀。求(1)中反应后溶液稀释到50 mL时氯离子的物质的量浓度是多少?
 MnCl2 + Cl2↑+2H2O,现用足量浓盐酸在加热条件下跟二氧化锰反应制取氯气。若标准状况下制得Cl22.24L求:
MnCl2 + Cl2↑+2H2O,现用足量浓盐酸在加热条件下跟二氧化锰反应制取氯气。若标准状况下制得Cl22.24L求:(1)二氧化锰的质量;
(2)把(1)中反应后的溶液稀释到50 mL,从中取出10.0 mL,加入10.0 mL 0.600 mol / L的硝酸银溶液,恰好将氯离子完全沉淀。求(1)中反应后溶液稀释到50 mL时氯离子的物质的量浓度是多少?
您最近一年使用:0次
【推荐3】将32.0 g铜与150 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
(1)NO的体积为___________ L(标准状况);
(2)铜完全溶解后,消耗的硝酸的物质的量为___________ mol;
(3)待产生的气体全部逸出后,向溶液中加入200 mL 5.00 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸的物质的量浓度为___________ mol·L-1。
(1)NO的体积为
(2)铜完全溶解后,消耗的硝酸的物质的量为
(3)待产生的气体全部逸出后,向溶液中加入200 mL 5.00 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸的物质的量浓度为
您最近一年使用:0次



