碳是形成化合物种类最多的元素,其单质和化合物是人类生活的主要能源物质。
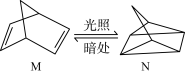
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH =+88.6 kJ·mol-1,则M、N相比,较稳定的是__________
(2)根据下列热化学方程式分析,C(s)的燃烧热△H等于_____________ (用△H1 、△H2、△H3表示)
C(s)+H2O(l)=CO(g)+H2(g); △H1
2CO(g)+O2(g)=2CO2(g); △H2
2H2(g)+O2(g)=2H2O(l); △H3
(3)根据键能数据估算CH4(g)+4F2(g)= CF4(g)+4HF(g)的反应热ΔH=________
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________________
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH =+88.6 kJ·mol-1,则M、N相比,较稳定的是

(2)根据下列热化学方程式分析,C(s)的燃烧热△H等于
C(s)+H2O(l)=CO(g)+H2(g); △H1
2CO(g)+O2(g)=2CO2(g); △H2
2H2(g)+O2(g)=2H2O(l); △H3
(3)根据键能数据估算CH4(g)+4F2(g)= CF4(g)+4HF(g)的反应热ΔH=
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
更新时间:2020-01-14 23:37:45
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】I.已知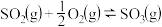 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
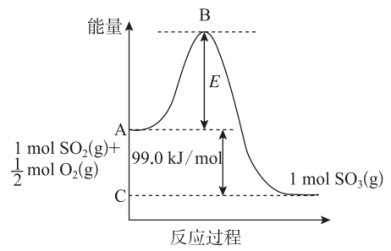
(1)图中C点表示_______ ,E所代表的能量是_______ ,E的大小对该反应的反应热_______ (填“有”或“无”)影响。
(2)请求出反应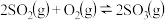

_______ 。
(3)又知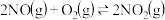
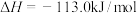 ,请根据题给条件求出反应
,请根据题给条件求出反应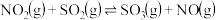 的焓变
的焓变
_______ 。
II.
(4)0.5mol (g)在
(g)在 中完全燃烧生成
中完全燃烧生成 和液态水,放出649.8kJ的热量,写出燃烧热的热反应方程式
和液态水,放出649.8kJ的热量,写出燃烧热的热反应方程式_______ 。
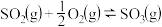 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
(1)图中C点表示
(2)请求出反应
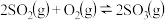

(3)又知
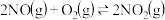
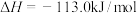 ,请根据题给条件求出反应
,请根据题给条件求出反应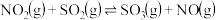 的焓变
的焓变
II.
(4)0.5mol
 (g)在
(g)在 中完全燃烧生成
中完全燃烧生成 和液态水,放出649.8kJ的热量,写出燃烧热的热反应方程式
和液态水,放出649.8kJ的热量,写出燃烧热的热反应方程式
您最近一年使用:0次
【推荐2】I. 某可逆反应在某体积为2L的密闭容器中进行,在从0~3min各物质的量的变化情况如图所示(A、B、C均为气体)。
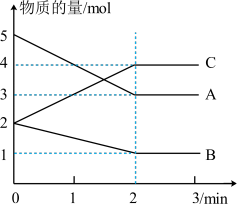
(1)该反应的化学方程式为______ 。
(2)反应开始至2min时,B的平均反应速率为______ 。
(3)能说明该反应已达到平衡状态的是______ 。
A. c(A)= c(B)= c(C) B.容器内压强保持不变
C .v逆(A)= v正(C) D. c(C)不再变化
(4)由图求得A的平衡时的转化率为______ 。
Ⅱ.(5)已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表
则合成氨反应:N2(g) + 3H2 (g)= 2NH3(g)  H =
H = ______ kJ·mol-1

(1)该反应的化学方程式为
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
A. c(A)= c(B)= c(C) B.容器内压强保持不变
C .v逆(A)= v正(C) D. c(C)不再变化
(4)由图求得A的平衡时的转化率为
Ⅱ.(5)已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表
| 共价键 | H—H | N—H | N≡N |
| 能量变化/kJ·mol-1 | a | b | c |
 H =
H =
您最近一年使用:0次
【推荐3】燃料和能源是化学知识与社会生活联系极为密切的内容,我们要关注矿物能源的合理利用,积极研究、开发新能源。
(1)新能源应该具有原材料易得、燃烧时产生的热量多且不会污染环境的特点,在煤炭、石油、煤气、氢气中,前途广阔的能源是_____ 。
(2)近年来,我国煤矿事故大多是瓦斯爆炸所致。瓦斯中含有甲烷和一氧化碳等气体,当矿井中瓦斯浓度达到一定范围时遇明火即燃烧爆炸。为避免灾难的发生应采取的切实可行的措施有_____ (填序号)。
①加强安全管理,杜绝明火源 ②降低瓦斯气体的着火点 ③提高通风能力 ④将矿井中的氧气抽去
(3)水煤气的主要成分是一氧化碳和氢气,它是由煤炭和水蒸气反应制得的,已知C(石墨)、CO、H2燃烧的热化学方程式为:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1
请回答下列问题:
①根据上述提供的热化学方程式计算,36g水由液态变成气态的热量变化是_____ (填“吸收”或“放出”)_____ 热量。
②写出C(石墨,s)与水蒸气反应生成一氧化碳和氢气的热化学方程式:_____ 。
③作为燃料,水煤气和煤相比有什么优点_____ (任答一点)。
(1)新能源应该具有原材料易得、燃烧时产生的热量多且不会污染环境的特点,在煤炭、石油、煤气、氢气中,前途广阔的能源是
(2)近年来,我国煤矿事故大多是瓦斯爆炸所致。瓦斯中含有甲烷和一氧化碳等气体,当矿井中瓦斯浓度达到一定范围时遇明火即燃烧爆炸。为避免灾难的发生应采取的切实可行的措施有
①加强安全管理,杜绝明火源 ②降低瓦斯气体的着火点 ③提高通风能力 ④将矿井中的氧气抽去
(3)水煤气的主要成分是一氧化碳和氢气,它是由煤炭和水蒸气反应制得的,已知C(石墨)、CO、H2燃烧的热化学方程式为:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
H2(g)+
 O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1CO(g)+
 O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1H2(g)+
 O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1请回答下列问题:
①根据上述提供的热化学方程式计算,36g水由液态变成气态的热量变化是
②写出C(石墨,s)与水蒸气反应生成一氧化碳和氢气的热化学方程式:
③作为燃料,水煤气和煤相比有什么优点
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】生产生活中的化学反应都伴随能量的变化,请根据有关知识回答下列问题:
(1)制作有降温、保鲜和镇痛的冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”可利用下面_______ (填字母序号)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)沼气是一种能源,它的主要成分是 ,常温下1g
,常温下1g 完全燃烧生成
完全燃烧生成 和水时,放出55.625kJ热量,则其热化学方程式是
和水时,放出55.625kJ热量,则其热化学方程式是_______ 。
(4)共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。工业合成氨是人类科学技术的一项重大突破,其反应如下:
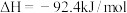 ,若断裂
,若断裂 和
和 需要吸收的能量分别为436kJ和391kJ,则断裂
需要吸收的能量分别为436kJ和391kJ,则断裂 需要吸收的能量为
需要吸收的能量为_______ kJ。
(5)参考下表中的数据,判断下列分子受热时最稳定的是_______。(填字母)
(1)制作有降温、保鲜和镇痛的冷敷袋可以利用
(2)“即热饭盒”可利用下面
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)沼气是一种能源,它的主要成分是
 ,常温下1g
,常温下1g 完全燃烧生成
完全燃烧生成 和水时,放出55.625kJ热量,则其热化学方程式是
和水时,放出55.625kJ热量,则其热化学方程式是(4)共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。工业合成氨是人类科学技术的一项重大突破,其反应如下:

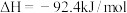 ,若断裂
,若断裂 和
和 需要吸收的能量分别为436kJ和391kJ,则断裂
需要吸收的能量分别为436kJ和391kJ,则断裂 需要吸收的能量为
需要吸收的能量为(5)参考下表中的数据,判断下列分子受热时最稳定的是_______。(填字母)
| 化学键 |  |  |  |  |
键能 | 436 | 565 | 431 | 368 |
A. | B.HF | C.HCl | D.HBr |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答问题:
(1)已知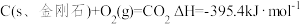 ,
,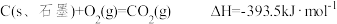 。
。
①石墨中 键键能
键键能___________ (填“大于”“小于”或“等于”)金刚石中 键键能。
键键能。
②由石墨转化为金刚石的热化学方程式为___________ 。
(2)将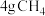 完全燃烧生成气态
完全燃烧生成气态 和液态水,放出热量
和液态水,放出热量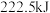 ,其热化学反应方程式为:
,其热化学反应方程式为:___________ 。
(3) 的气态高能燃料乙硼烷
的气态高能燃料乙硼烷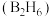 在氧气中燃烧,生成固态三氧化二硼和液态水,放出
在氧气中燃烧,生成固态三氧化二硼和液态水,放出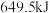 热量,其热化学反应方程式为:
热量,其热化学反应方程式为:___________ 。
(4)已知下列反应的反应热:
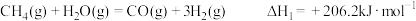
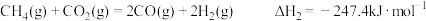
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(1)已知
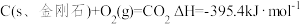 ,
,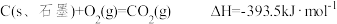 。
。①石墨中
 键键能
键键能 键键能。
键键能。②由石墨转化为金刚石的热化学方程式为
(2)将
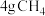 完全燃烧生成气态
完全燃烧生成气态 和液态水,放出热量
和液态水,放出热量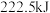 ,其热化学反应方程式为:
,其热化学反应方程式为:(3)
 的气态高能燃料乙硼烷
的气态高能燃料乙硼烷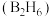 在氧气中燃烧,生成固态三氧化二硼和液态水,放出
在氧气中燃烧,生成固态三氧化二硼和液态水,放出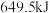 热量,其热化学反应方程式为:
热量,其热化学反应方程式为:(4)已知下列反应的反应热:
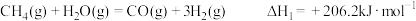
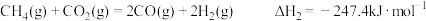
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
【推荐3】能源危机当前是一个全球性问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是__ (填字母)。
A.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
B.大力开采煤、石油和天然气以满足人们日益增长的能源需求
C.开发太阳能、水能、风能、地热能等新能源,不使用煤、石油等化石燃料
D.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
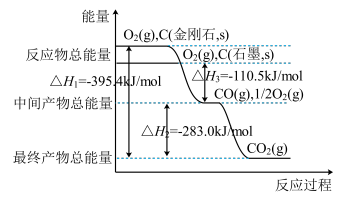
①在通常状况下,金刚石和石墨相比较,__ (填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH=___ 。
②12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为__ kJ。
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1。N2(g)+O2(g)=2NO(g)ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为__ 。
(4)综合上述有关信息,请写出用CO除去NO的热化学方程式:__ 。
(1)下列做法有助于能源“开源节流”的是
A.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
B.大力开采煤、石油和天然气以满足人们日益增长的能源需求
C.开发太阳能、水能、风能、地热能等新能源,不使用煤、石油等化石燃料
D.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
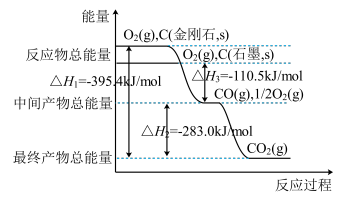
①在通常状况下,金刚石和石墨相比较,
②12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1。N2(g)+O2(g)=2NO(g)ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为
(4)综合上述有关信息,请写出用CO除去NO的热化学方程式:
您最近一年使用:0次
【推荐1】回答下列问题
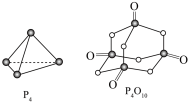
(1)白磷与氧可发生如下反应: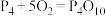 ,已知断裂下列化学键需要吸收的能量分别为:P—P
,已知断裂下列化学键需要吸收的能量分别为:P—P 、P—O
、P—O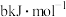 、P=O
、P=O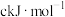 、O=O
、O=O 根据图示的分子结构和有关数据计算该反应的反应热为
根据图示的分子结构和有关数据计算该反应的反应热为_______ 。
(2)写出下列热化学方程式,在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫燃烧热的热化学方程式为_______ 。
(3)氮氧化物能破坏臭氧层: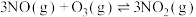

_______ 。
已知:反应Ⅰ: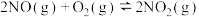
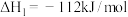
反应Ⅱ: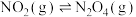
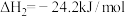
反应Ⅲ: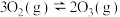
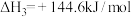
(4)碳氧化物的转化有重大用途,请回答下列问题,已知:
①

②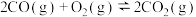

③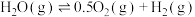

则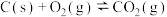

_______ ( 、
、 、
、 表示)。
表示)。
(1)白磷与氧可发生如下反应:
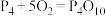 ,已知断裂下列化学键需要吸收的能量分别为:P—P
,已知断裂下列化学键需要吸收的能量分别为:P—P 、P—O
、P—O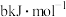 、P=O
、P=O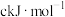 、O=O
、O=O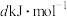 根据图示的分子结构和有关数据计算该反应的反应热为
根据图示的分子结构和有关数据计算该反应的反应热为
(2)写出下列热化学方程式,在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫燃烧热的热化学方程式为
(3)氮氧化物能破坏臭氧层:
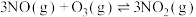

已知:反应Ⅰ:
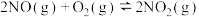
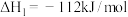
反应Ⅱ:
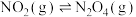
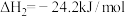
反应Ⅲ:
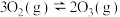
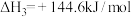
(4)碳氧化物的转化有重大用途,请回答下列问题,已知:
①


②
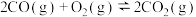

③
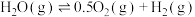

则
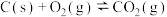

 、
、 、
、 表示)。
表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:
(i)直接氯化: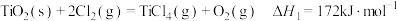 ,
,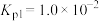 。
。
(ii)碳氯化: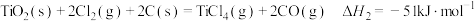 ,
,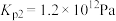 。则反应
。则反应 的
的 为
为____________  ,
,
________  ;对于碳氯化反应,温度升高,平衡转化率
;对于碳氯化反应,温度升高,平衡转化率____________ (填“变大”“变小”或“不变”)。
 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:(i)直接氯化:
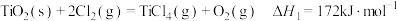 ,
,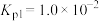 。
。(ii)碳氯化:
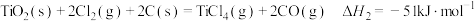 ,
,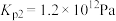 。则反应
。则反应 的
的 为
为 ,
,
 ;对于碳氯化反应,温度升高,平衡转化率
;对于碳氯化反应,温度升高,平衡转化率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
(1)H2的燃烧热ΔH=_________ 。
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为_________ g。
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________ 。
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1(1)H2的燃烧热ΔH=
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次



