NaNO2(亚硝酸钠)常用作肉类食品的防腐剂,若添加过量,易导致人体中毒。亚硝酸盐经消化道吸收进入血液,使血液中的正常携氧的亚铁血红蛋白转化成三价铁血红蛋白,失去携氧能力引起组织缺氧,导致中毒。成人摄入0.2~0.5g就会引起中毒,摄入3g即可致死。
(1)NaNO2的毒性源于NaNO2具有________ 性。
(2)设计实验验证NaNO2确实具有该性质(已知: NaNO2与HI反应生成I2和NO),将离子方程式配平:
____ NO2-+_____ H+ + _____ I -=_____ I2 + _____ NO↑ + _____
(3)请从两个不同的角度进一步预测NaNO2还可能 具有的化学性质,并说明预测的依据 (已知:HNO2是一种弱酸)。按照因为…所以…进行表述___________________ ;__________________ 。
(4)救治NaNO2中毒病人的方法是静脉注射亚甲蓝(一种有机物),其解毒原理是__________ 。
(1)NaNO2的毒性源于NaNO2具有
(2)设计实验验证NaNO2确实具有该性质(已知: NaNO2与HI反应生成I2和NO),将离子方程式配平:
(3)请从两个不同的角度进一步预测NaNO2
(4)救治NaNO2中毒病人的方法是静脉注射亚甲蓝(一种有机物),其解毒原理是
更新时间:2020-01-17 20:40:33
|
相似题推荐
【推荐1】自舍勒发现氯气可以作为消毒剂以来,人们陆续发现和使用了形形色色的消毒剂。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移_______ 。反应中盐酸表现出的性质有_______ 。
(2)根据世界环保联盟的要求,二氧化氯(ClO2)消毒剂将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 (已知
(已知 具有很强的还原性,易被氧化成
具有很强的还原性,易被氧化成 )溶液混合并加入稀
)溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:_______ 。
(3)高铁酸钾 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。
①湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式_______ 。
②如下图所示,用 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: 。
。
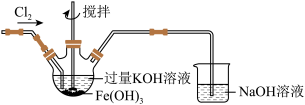
反应后取出三口瓶中的溶液于试管中,加入稀 ,后产生黄绿色气体
,后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 ;制备高铁酸钾的实验中,氧化性:
;制备高铁酸钾的实验中,氧化性:
_______  (填“>”、“<”或“=”),试管中发生反应再次产生
(填“>”、“<”或“=”),试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
_______  (填“>”“<”或“=”),试说明影响
(填“>”“<”或“=”),试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素_______ 。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用
 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移(2)根据世界环保联盟的要求,二氧化氯(ClO2)消毒剂将逐渐取代
 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 (已知
(已知 具有很强的还原性,易被氧化成
具有很强的还原性,易被氧化成 )溶液混合并加入稀
)溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:(3)高铁酸钾
 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。①湿法制备高铁酸钾的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式②如下图所示,用
 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: 。
。
反应后取出三口瓶中的溶液于试管中,加入稀
 ,后产生黄绿色气体
,后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 ;制备高铁酸钾的实验中,氧化性:
;制备高铁酸钾的实验中,氧化性:
 (填“>”、“<”或“=”),试管中发生反应再次产生
(填“>”、“<”或“=”),试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
 (填“>”“<”或“=”),试说明影响
(填“>”“<”或“=”),试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:
H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O____________ 。
(2)如消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:
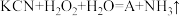 (已配平)试指出A的化学式
(已配平)试指出A的化学式______ ,如此反应中有6.72L(标准状况)气体生成,转移电子数目为______ (用 表示)。
表示)。
(3)高锰酸钾也可用于医学杀菌消毒。根据反应条件可判断氧化剂的氧化能力的强弱:例如: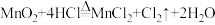 ;
; 。
。
则氧化性
______  (填“强于”或“弱于”或“等于”。)
(填“强于”或“弱于”或“等于”。)
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:
H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(2)如消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:
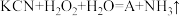 (已配平)试指出A的化学式
(已配平)试指出A的化学式 表示)。
表示)。(3)高锰酸钾也可用于医学杀菌消毒。根据反应条件可判断氧化剂的氧化能力的强弱:例如:
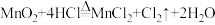 ;
; 。
。则氧化性

 (填“强于”或“弱于”或“等于”。)
(填“强于”或“弱于”或“等于”。)
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】(1)通常状况下,已知X、Y两种气体,其质量分别为a、b时,体积之比为2:3。 两种气体X、Y的相对分子质量之比为________ ;相同条件下的X、Y两种气体,体积相同时,则X、Y的密度之比为__________ ;相同条件下,同质量的两种气体,X与Y的分子数之比为________ 。
(2)已知下列反应能发生:
2A3+ + 2B - = 2A2+ + B2;
C2 + 2B- = 2C- + B2;
2A2+ + C2 = 2A3++ 2C-
上述三个反应中氧化剂的氧化性强弱顺序为___________ ;还原剂的还原性强弱顺序为___________ 。
(3)一定条件下硝酸铵受热分解的化学方程式为: NH4NO3→HNO3+N2↑+H2O(未配平),写出配平后的化学方程式:________________________ 。在反应中被氧化与被还原的氮原子数之比为___________
(4)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。
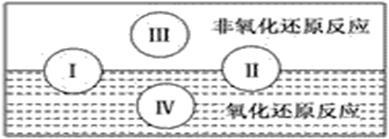
试写出有水参加的符合反应类型Ⅳ的一个化学方程式___________________________
(2)已知下列反应能发生:
2A3+ + 2B - = 2A2+ + B2;
C2 + 2B- = 2C- + B2;
2A2+ + C2 = 2A3++ 2C-
上述三个反应中氧化剂的氧化性强弱顺序为
(3)一定条件下硝酸铵受热分解的化学方程式为: NH4NO3→HNO3+N2↑+H2O(未配平),写出配平后的化学方程式:
(4)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是
| A.野火烧不尽,春风吹又生 |
| B.春蚕到死丝方尽,蜡炬成灰泪始干 |
| C.粉身碎骨浑不怕,要留清白在人间 |
| D.爆竹声中一岁除,春风送暖入屠苏 |
水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式
您最近一年使用:0次
【推荐1】氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+2H2O;已知KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该反应的离子方程式;用“单线桥法”标出电子转移的方向和数目:_______________ 。
(2)反应中硝酸体现了_________ 、_________ 性质。
(3)反应中若转移3mol电子,则在标况下产生的气体体积是________ L。
(1)写出并配平该反应的离子方程式;用“单线桥法”标出电子转移的方向和数目:
(2)反应中硝酸体现了
(3)反应中若转移3mol电子,则在标况下产生的气体体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】汽车尾气中主要含有 、CO、NO等物质,治理方法之一是在汽车的排气管上安装“催化转化器”,其中CO和NO可以转化为两种无毒的气体,如图所示。
、CO、NO等物质,治理方法之一是在汽车的排气管上安装“催化转化器”,其中CO和NO可以转化为两种无毒的气体,如图所示。
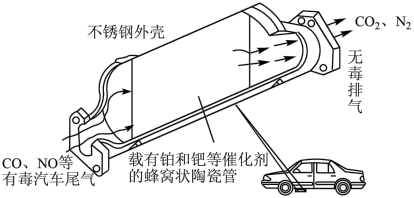
(1)下列关于汽车尾气处理的说法正确的是___________
(2)汽车尾气中的NO来源不合理的是___________ 。
A.氨和氧气在催化剂的作用下转化而成
B.氮气和氧气在火花塞放电时反应生成
C.氮气和氧气在高温条件下转化而成
(3)尽管催化转化器可以处理CO、NO,但是催化剂也容易将 转化为
转化为 ,从而引起酸雨问题。
,从而引起酸雨问题。 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
 、CO、NO等物质,治理方法之一是在汽车的排气管上安装“催化转化器”,其中CO和NO可以转化为两种无毒的气体,如图所示。
、CO、NO等物质,治理方法之一是在汽车的排气管上安装“催化转化器”,其中CO和NO可以转化为两种无毒的气体,如图所示。
(1)下列关于汽车尾气处理的说法正确的是___________
A.这是一个产生 的置换反应 的置换反应 |
B.汽车尾气的主要污染成分包括CO、NO和 |
| C.尾气进入催化转化器前,必须有措施控制NO和CO的排出比例 |
| D.铂和钯等催化剂能够催化所有气体之间的反应 |
(2)汽车尾气中的NO来源不合理的是
A.氨和氧气在催化剂的作用下转化而成
B.氮气和氧气在火花塞放电时反应生成
C.氮气和氧气在高温条件下转化而成
(3)尽管催化转化器可以处理CO、NO,但是催化剂也容易将
 转化为
转化为 ,从而引起酸雨问题。
,从而引起酸雨问题。 转化为
转化为 的化学方程式为
的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
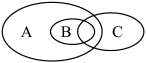
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母)
(2)有同学认为所有酸碱中和反应均可表示为 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)_______ 。
(3)下列反应属于分类中的氧化还原反应。
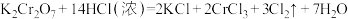
在参加反应的HCl中,起还原剂作用的HCl与起酸性作用的HCl的质量比为_______ ,每生成一个 转移的电子数为
转移的电子数为_______ 。
(4)配平化学方程式,并标出电子转移方向和数目。_______
_______ _______
_______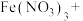 _______
_______ _______
_______ _______
_______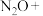 _______
_______
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)有同学认为所有酸碱中和反应均可表示为
 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)(3)下列反应属于分类中的氧化还原反应。
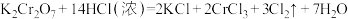
在参加反应的HCl中,起还原剂作用的HCl与起酸性作用的HCl的质量比为
 转移的电子数为
转移的电子数为(4)配平化学方程式,并标出电子转移方向和数目。
_______
 _______
_______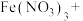 _______
_______ _______
_______ _______
_______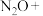 _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】工业制硝酸的尾气中含有N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
I.工业制硝酸:
(1)氨催化氧化法是工业制硝酸的基础反应,写出氨催化氧化的化学方程式为___ 。
II.含氮氧化物的尾气处理:
(2)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解,N2O分解的化学方程式为___ 。
(3)NO和NO2的处理。已知NO、NO2在碱溶液中可以发生如下反应:NO+NO2+2OH-=2NO2-+H2O,2NO2+2OH-=NO2-+NO3-+H2O
①下列措施能提高尾气中NO和NO2去除率的有___ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入空气可以提高尾气的吸收率
② 含NO和NO2的尾气可用NaOH溶液吸收,吸收后的溶液经___ 、过滤,得到NaNO2晶体。
③ 吸收后排放的尾气中含量较高的氮氧化物是___ (填化学式)。
(4)用NaClO溶液吸收尾气。用NaClO溶液代替NaOH溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO3-的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
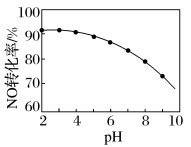
①在酸性NaClO溶液中,HClO氧化NO生成NO3-时发生反应的离子方程式为___ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___ 。
I.工业制硝酸:
(1)氨催化氧化法是工业制硝酸的基础反应,写出氨催化氧化的化学方程式为
II.含氮氧化物的尾气处理:
(2)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解,N2O分解的化学方程式为
(3)NO和NO2的处理。已知NO、NO2在碱溶液中可以发生如下反应:NO+NO2+2OH-=2NO2-+H2O,2NO2+2OH-=NO2-+NO3-+H2O
①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入空气可以提高尾气的吸收率
② 含NO和NO2的尾气可用NaOH溶液吸收,吸收后的溶液经
③ 吸收后排放的尾气中含量较高的氮氧化物是
(4)用NaClO溶液吸收尾气。用NaClO溶液代替NaOH溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO3-的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。

①在酸性NaClO溶液中,HClO氧化NO生成NO3-时发生反应的离子方程式为
②NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近一年使用:0次
【推荐2】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它是一种还原剂,能被常见的强氧化剂氧化,但在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C可解毒。下列叙述不正确的是___________ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是___________ (填序号)。
A.加入稀盐酸,观察是否有气泡产生 B.加入AgNO3,观察是否有沉淀产生 C.在酸性条件下加入KI-淀粉溶液,观察溶液颜色(I2遇淀粉呈蓝色)
(3)某同学把氯气通入到NaNO2溶液中,生成NaNO3和HCl,请写出反应的离子方程式:___________ 。
(4)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
___________Fe(OH)3 +___________ClO-+___________OH- =___________FeO +___________Cl-+___________ ___________
+___________Cl-+___________ ___________
___________
(5)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________ 。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.加入稀盐酸,观察是否有气泡产生 B.加入AgNO3,观察是否有沉淀产生 C.在酸性条件下加入KI-淀粉溶液,观察溶液颜色(I2遇淀粉呈蓝色)
(3)某同学把氯气通入到NaNO2溶液中,生成NaNO3和HCl,请写出反应的离子方程式:
(4)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
___________Fe(OH)3 +___________ClO-+___________OH- =___________FeO
 +___________Cl-+___________ ___________
+___________Cl-+___________ ___________(5)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是
您最近一年使用:0次



