在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)⇌2NH3(g) △H<0,其平衡常数K与温度T的关系如表:
①试判断K1_____ K2(填写“>”,“=”或“<”)。
②下列各项能说明该反应已达到平衡状态的是__ (填字母)。
a.单位时间内,消耗1molN2的同时生成2molNH3
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
①试判断K1
②下列各项能说明该反应已达到平衡状态的是
a.单位时间内,消耗1molN2的同时生成2molNH3
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
更新时间:2020-02-11 19:42:04
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】用活性炭还原法处理氮氧化物,有关反应为:C(s)+ 2NO(g) N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
(1) 10 min~20 min的时间段内,以CO2表示的反应速率为____ ;
(2)计算出该反应的平衡常数的值K=________ ;
(3) 下列各项能作为判断该反应达到平衡状态的是____ (填序号字母);
A.容器内压强保持不变 B.2v正(NO)= v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是_____________ ;
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率__________ (填“增大”、 “不变”或“减小”)。
 N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:| 时间min/ 浓度mol·L-1 | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
(1) 10 min~20 min的时间段内,以CO2表示的反应速率为
(2)计算出该反应的平衡常数的值K=
(3) 下列各项能作为判断该反应达到平衡状态的是
A.容器内压强保持不变 B.2v正(NO)= v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题
(1)在2L的密闭容器中放入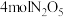 ,发生如下反应:2N2O5(g)
,发生如下反应:2N2O5(g)  4NO2(g)+O2(g)。反应至
4NO2(g)+O2(g)。反应至 时,测得
时,测得 转化了20%,则
转化了20%,则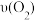 为
为_______ ; 时,
时, 混合气体中的体积分数是
混合气体中的体积分数是_______
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
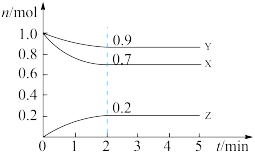
①该反应的化学方程式为_______ 。
②若X、Y、Z均为气体, 时反应达到平衡,开始时的压强与平衡时的压强之比为
时反应达到平衡,开始时的压强与平衡时的压强之比为_______ ,X的转化率为_______ 。若X、Y、Z均为气体,则以下情况可判断达平衡状态的有_______ (填序号)
A.容器内混合气体的平均相对分子质量不变
B.容器内混合气体的密度不变
C.容器内混合气体的总压强不变
D.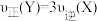
(3)将一定质量的 粉投入到
粉投入到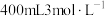 的稀硝酸中,待
的稀硝酸中,待 粉完全溶解时,收集到标准状况下的NO气体
粉完全溶解时,收集到标准状况下的NO气体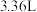 (假设硝酸的还原产物只有NO且气体全部逸出),再向反应后的溶液中缓慢加入
(假设硝酸的还原产物只有NO且气体全部逸出),再向反应后的溶液中缓慢加入 粉,充分反应后溶液只含一种溶质。试计算:
粉,充分反应后溶液只含一种溶质。试计算:
①最初加入的铜粉质量为_______
②至少需要加入铁粉的质量为_______
(1)在2L的密闭容器中放入
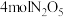 ,发生如下反应:2N2O5(g)
,发生如下反应:2N2O5(g)  4NO2(g)+O2(g)。反应至
4NO2(g)+O2(g)。反应至 时,测得
时,测得 转化了20%,则
转化了20%,则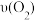 为
为 时,
时, 混合气体中的体积分数是
混合气体中的体积分数是(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
②若X、Y、Z均为气体,
 时反应达到平衡,开始时的压强与平衡时的压强之比为
时反应达到平衡,开始时的压强与平衡时的压强之比为A.容器内混合气体的平均相对分子质量不变
B.容器内混合气体的密度不变
C.容器内混合气体的总压强不变
D.
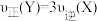
(3)将一定质量的
 粉投入到
粉投入到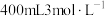 的稀硝酸中,待
的稀硝酸中,待 粉完全溶解时,收集到标准状况下的NO气体
粉完全溶解时,收集到标准状况下的NO气体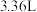 (假设硝酸的还原产物只有NO且气体全部逸出),再向反应后的溶液中缓慢加入
(假设硝酸的还原产物只有NO且气体全部逸出),再向反应后的溶液中缓慢加入 粉,充分反应后溶液只含一种溶质。试计算:
粉,充分反应后溶液只含一种溶质。试计算:①最初加入的铜粉质量为
②至少需要加入铁粉的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=a kJ/mol1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ/mol1,平衡常数为K;
(1)若500℃时进行上述反应,CO2起始浓度为2 mol/L,CO的平衡浓度为________ 。
(2)上述反应中的a________ 0(填“大于”“小于”或“等于”)。
(3)700℃上述反应达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有______ (填序号)。
A.缩小反应器体积 B.通入CO2
C.升高温度到900℃ D.使用合适的催化剂
 FeO(s)+CO(g) ΔH=a kJ/mol1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ/mol1,平衡常数为K;| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(1)若500℃时进行上述反应,CO2起始浓度为2 mol/L,CO的平衡浓度为
(2)上述反应中的a
(3)700℃上述反应达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有
A.缩小反应器体积 B.通入CO2
C.升高温度到900℃ D.使用合适的催化剂
您最近一年使用:0次
【推荐2】完成下列问题。
I.
(1)已知在448℃时,反应H2(g)+I2(g)⇌2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)⇌H2(g)+I2(g)的平衡常数K2为____ ;反应 H2(g)+
H2(g)+ I2(g)⇌HI(g)的平衡常数K3为
I2(g)⇌HI(g)的平衡常数K3为_____ 。
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(2)该反应的化学平衡常数表达式为K=_______ 。
(3)该反应为_______ 反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是_______。
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_______ ℃。
(6)为了减少CO的排放,某环境研究小组以CO和 为原料合成清洁能源二甲醚(
为原料合成清洁能源二甲醚( ),反应如下:
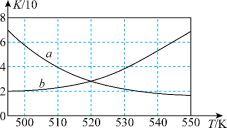
),反应如下: 。如图所示能正确反映平衡常数K随温度变化关系的曲线为
。如图所示能正确反映平衡常数K随温度变化关系的曲线为_______ (填曲线标记字母),其判断理由是_______ 。
I.
(1)已知在448℃时,反应H2(g)+I2(g)⇌2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)⇌H2(g)+I2(g)的平衡常数K2为
 H2(g)+
H2(g)+ I2(g)⇌HI(g)的平衡常数K3为
I2(g)⇌HI(g)的平衡常数K3为Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)该反应的化学平衡常数表达式为K=
(3)该反应为
(4)能判断该反应达到化学平衡状态的依据是_______。
| A.容器中压强不变 | B.混合气体中c(CO)不变 |
| C.v(H2)正=v(H2O)逆 | D.c(CO2)=c(CO) |
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(6)为了减少CO的排放,某环境研究小组以CO和
 为原料合成清洁能源二甲醚(
为原料合成清洁能源二甲醚( ),反应如下:
),反应如下: 。如图所示能正确反映平衡常数K随温度变化关系的曲线为
。如图所示能正确反映平衡常数K随温度变化关系的曲线为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某研究小组向2 L密闭容器中加入过量的活性炭和0.2 mol NO,恒温(T1℃)下发生反应:C(s)+2NO(g) N2(g)+CO2(g)+Q(Q>0)。30 min后达到平衡,测得NO浓度为0.04 mol/L。回答下列问题:
N2(g)+CO2(g)+Q(Q>0)。30 min后达到平衡,测得NO浓度为0.04 mol/L。回答下列问题:
(1)该反应的平衡常数表达式K=______ ;T1℃达到平衡时,N2的平均反应速率=_______ 。
(2)30 min后,若改变某一条件提高NO的转化率,则可以改变的条件是______________ 。
(3)30 min后,升高温度至T2℃,达到平衡后,容器内NO、N2、CO2的关系不可能是____ 。
a.5:3:3 b.1:1:1 c.4:3:3 d.2:1:1
(4)若开始时密闭容器的体积为1 L,其它条件不变,达到平衡后,与原平衡相比,下列说法正确的是_________ 。
a.NO的转化率不变 b.N2的浓度是原来的2倍
c.反应放出的热量为0.1Q d.达到平衡的时间是原来的一半
 N2(g)+CO2(g)+Q(Q>0)。30 min后达到平衡,测得NO浓度为0.04 mol/L。回答下列问题:
N2(g)+CO2(g)+Q(Q>0)。30 min后达到平衡,测得NO浓度为0.04 mol/L。回答下列问题:(1)该反应的平衡常数表达式K=
(2)30 min后,若改变某一条件提高NO的转化率,则可以改变的条件是
(3)30 min后,升高温度至T2℃,达到平衡后,容器内NO、N2、CO2的关系不可能是
a.5:3:3 b.1:1:1 c.4:3:3 d.2:1:1
(4)若开始时密闭容器的体积为1 L,其它条件不变,达到平衡后,与原平衡相比,下列说法正确的是
a.NO的转化率不变 b.N2的浓度是原来的2倍
c.反应放出的热量为0.1Q d.达到平衡的时间是原来的一半
您最近一年使用:0次

 在一定条件下可发生反应
在一定条件下可发生反应 ,一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
,一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和