为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
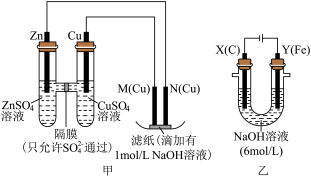
Ⅰ.用甲装置进行第一组实验:
(1)Zn电极上的电极反应式为___________________ ,在保证电极反应不变的情况下,下列材料不能代替左侧Cu电极(虚线方框内)的是________ (填序号)。
A.石墨 B.镁 C.银 D.铂
(2)实验过程中,SO42-________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________________________________
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(FeO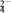 )在溶液中呈紫红色。根据实验现象及所查信息,填写下列空白:
)在溶液中呈紫红色。根据实验现象及所查信息,填写下列空白:
(3)电解过程中,X极溶液的pH________ (填“增大”、“减小”或“不变”)。
(4)电解过程中,Y极发生的电极反应为4OH--4e-===2H2O+O2↑和______________ 。
(5)已知K2FeO4和Zn可以构成碱性电池,其中K2FeO4在电池中作正极材料,电池总反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2,则该电池正极发生的电极反应为_____________ 。

Ⅰ.用甲装置进行第一组实验:
(1)Zn电极上的电极反应式为
A.石墨 B.镁 C.银 D.铂
(2)实验过程中,SO42-
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(FeO
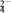 )在溶液中呈紫红色。根据实验现象及所查信息,填写下列空白:
)在溶液中呈紫红色。根据实验现象及所查信息,填写下列空白:(3)电解过程中,X极溶液的pH
(4)电解过程中,Y极发生的电极反应为4OH--4e-===2H2O+O2↑和
(5)已知K2FeO4和Zn可以构成碱性电池,其中K2FeO4在电池中作正极材料,电池总反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2,则该电池正极发生的电极反应为
更新时间:2020-02-15 11:13:04
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据以上表中记录的实验现象,回答下列问题:
(1)实验1、4中A1电极分别作_______ 、_______ 。(填“正极”或“负极”)
(2)实验2中负极的电极反应式为_______ 。
(3)根据以上实验结果,在原电池中相对活泼的金属做正极还是做负极,除了受金属本身的性质影响外,还受_______ 因素的影响。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
(1)实验1、4中A1电极分别作
(2)实验2中负极的电极反应式为
(3)根据以上实验结果,在原电池中相对活泼的金属做正极还是做负极,除了受金属本身的性质影响外,还受
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某学习小组用如图所示A、B装置分别探究金属锌与稀硫酸的反应,实验过程中A装置烧杯内的溶液温度升高,B装置的电流计指针发生偏转。

(1)A装置的烧杯中发生反应的离子方程式为______________ 。
(2)B装置中Zn板是________ 极;Cu板上的现象是________ ,其发生的电极反应式是_____ 。若有1 mol电子流过导线,则正极生成的产物的物质的量为_______ 。
(3)从能量转化的角度看,A、B中反应物的总能量________ (填“大于”“小于”或“等于”)生成物的总能量,A中主要是将化学能转化为__________ ,B中主要是将化学能转化为___________ 。
(4)该小组同学反思原电池的原理,其中观点正确的是___________ (填字母)。
A 原电池反应的过程中可能没有电子发生转移 B 原电池装置需要2个电极
C 电极一定不能参加反应 D 氧化反应和还原反应可以拆开在两极发生
(5)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则该原电池的正极发生的电极反应为___________ 。

(1)A装置的烧杯中发生反应的离子方程式为
(2)B装置中Zn板是
(3)从能量转化的角度看,A、B中反应物的总能量
(4)该小组同学反思原电池的原理,其中观点正确的是
A 原电池反应的过程中可能没有电子发生转移 B 原电池装置需要2个电极
C 电极一定不能参加反应 D 氧化反应和还原反应可以拆开在两极发生
(5)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则该原电池的正极发生的电极反应为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:
已知:相关物质的溶解度(20℃) Ag2SO4:0.796 g
(1)甲同学的实验如表:
注:经检验黑色固体为Ag。
①白色沉淀的化学式是__________________ 。
②甲同学得出Ag+氧化了Fe2+的依据是_____________________________________ 。
(2)乙同学为探究Ag+和Fe2+的反应,进行实验II。

a.按如图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
①盐桥中盛有饱和KNO3溶液,此盐桥中钾离子向________ (填“甲”或“乙”)池移动;
②若该电池能维持稳定电流强度为1 A,工作600s,理论上Ag电极的质量会________ (填“增重”或“溶解”) ________ g(已知F=96500 C·mol-1,电量(C)=电流(A)×时间(s) )。
b.随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
③a中甲烧杯里的电极反应式是______________ 。
④b中电压表指针逆向偏移后,银为_______ (填“正”或“负”)极。
(3)由上述实验得出的结论为_________________________________________________ 。
已知:相关物质的溶解度(20℃) Ag2SO4:0.796 g
(1)甲同学的实验如表:
序号 | 操作 | 现象 |
实验Ⅰ | 将2mL 1 mol•L-1 AgNO3溶液加入到1mL 1 mol•L-1 FeSO4溶液中 | 产生白色沉淀,随后又有黑色固体产生 |
取上层清液,滴加KSCN溶液 | 溶液变红 |
①白色沉淀的化学式是
②甲同学得出Ag+氧化了Fe2+的依据是
(2)乙同学为探究Ag+和Fe2+的反应,进行实验II。

a.按如图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
①盐桥中盛有饱和KNO3溶液,此盐桥中钾离子向
②若该电池能维持稳定电流强度为1 A,工作600s,理论上Ag电极的质量会
b.随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
③a中甲烧杯里的电极反应式是
④b中电压表指针逆向偏移后,银为
(3)由上述实验得出的结论为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】SCR催化剂广泛应用于燃煤烟气的处理,其主要成分为 、
、 、
、 ,还含有少量CaO、
,还含有少量CaO、 、
、 等。一种从废SCR催化剂中回收钨的工艺如下:
等。一种从废SCR催化剂中回收钨的工艺如下:

(1)“酸浸还原”中 转化成可溶于水的
转化成可溶于水的 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(2)“碱浸”时 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
(3)“滤渣”的主要成分是_______ 。
(4)常温下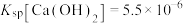 ,
,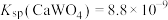 。“沉钨”过程中不断加入石灰乳,当“滤液”的
。“沉钨”过程中不断加入石灰乳,当“滤液”的 时,
时,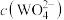 为
为_______  。
。
(5)“熔融电解”过程中阴极反应为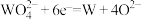 。电解过程中作阳极的石墨易消耗,原因是
。电解过程中作阳极的石墨易消耗,原因是_______ 。
(6)钛渣经处理可得到粗 。将
。将 氯化为
氯化为 是冶炼金属钛的主要反应之一、工业上常采用“加碳氯化”的方法生产
是冶炼金属钛的主要反应之一、工业上常采用“加碳氯化”的方法生产 ,同时得到CO,相应的化学方程式为
,同时得到CO,相应的化学方程式为
①
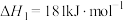
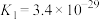
②
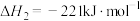
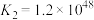
结合数据说明氯化过程中加碳的理由_______ 。
 、
、 、
、 ,还含有少量CaO、
,还含有少量CaO、 、
、 等。一种从废SCR催化剂中回收钨的工艺如下:
等。一种从废SCR催化剂中回收钨的工艺如下:
(1)“酸浸还原”中
 转化成可溶于水的
转化成可溶于水的 ,该反应的化学方程式为
,该反应的化学方程式为(2)“碱浸”时
 转化为
转化为 的离子方程式为
的离子方程式为(3)“滤渣”的主要成分是
(4)常温下
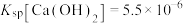 ,
,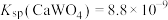 。“沉钨”过程中不断加入石灰乳,当“滤液”的
。“沉钨”过程中不断加入石灰乳,当“滤液”的 时,
时,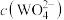 为
为 。
。(5)“熔融电解”过程中阴极反应为
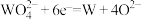 。电解过程中作阳极的石墨易消耗,原因是
。电解过程中作阳极的石墨易消耗,原因是(6)钛渣经处理可得到粗
 。将
。将 氯化为
氯化为 是冶炼金属钛的主要反应之一、工业上常采用“加碳氯化”的方法生产
是冶炼金属钛的主要反应之一、工业上常采用“加碳氯化”的方法生产 ,同时得到CO,相应的化学方程式为
,同时得到CO,相应的化学方程式为①

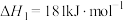
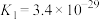
②

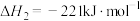
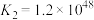
结合数据说明氯化过程中加碳的理由
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】电化学原理在污染治理方面有着重要的作用。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和 :
: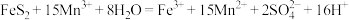
已知:两电极为完全相同的惰性电极。
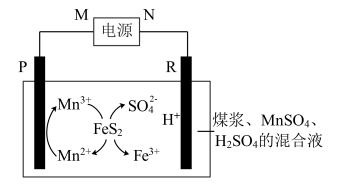
回答下列问题:
(1)N为电源的_______ (填“正极”或“负极”)。
(2)P上的电极反应为_______ 。
(3)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式_______ 。
(4)电解池工作时, 往
往_______ (填“P”或“R”)极移动,一段时间后,混合液中 的物质的量
的物质的量_______ (填“变大”、“变小”或“不变”)。
(5)电解过程中,混合溶液中的pH将_______ (填“变大”、“变小”或“不变”),理由是_______ 。
Ⅱ.微生物电池可用来处理废水中的对氯苯酚,原理如图所示。
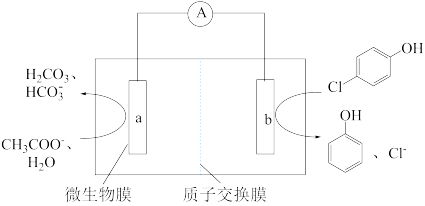
(6)该电池放电时,电子从_______ (填“b→a”或“a→b”)。
(7)a极上生成H2CO3的电极反应为_______ 。
(8)已知b极的电极反应为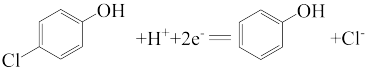 ,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为_______ mol(溶液体积变化忽略不计)。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和
 :
: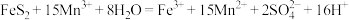
已知:两电极为完全相同的惰性电极。

回答下列问题:
(1)N为电源的
(2)P上的电极反应为
(3)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(4)电解池工作时,
 往
往 的物质的量
的物质的量(5)电解过程中,混合溶液中的pH将
Ⅱ.微生物电池可用来处理废水中的对氯苯酚,原理如图所示。

(6)该电池放电时,电子从
(7)a极上生成H2CO3的电极反应为
(8)已知b极的电极反应为
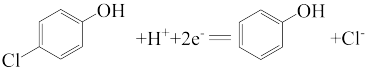 ,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】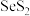 (二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含
(二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含 、
、 及少量
及少量 )制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:
)制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:

已知: 可溶于水
可溶于水 和
和 都是酸性氧化物。
都是酸性氧化物。
(1)“焙烧”时, 与
与 反应生成
反应生成 、
、 、
、 和
和 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)硒与硝酸反应产生的尾气可以用_______ (填化学式)溶液吸收。
(3) 是弱酸,
是弱酸, ,
, 和
和 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(4)分离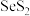 的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是
的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是_______ ,洗涤产品的操作是_______ 。
已知:布氏漏斗是漏斗上面板上有很多小孔,上面板上放滤纸。抽滤的原理是水龙头冲水排气,使瓶内压强小于外界大气压,从而在漏斗上方形成压力加快抽滤速率。
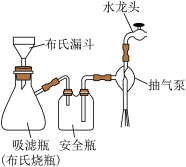
(5)以石墨为阳极,“电解”时阴极的电极反应式为_______ ,阳极产生的气体是_______ (填化学式)。
(6)已知阳极泥中Se的质量分数为2%,100t该阳极泥在上述转化中硒的总提取率为80%,得到的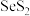 的质量为
的质量为_______ kg(结果保留1位小数)。
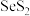 (二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含
(二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含 、
、 及少量
及少量 )制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:
)制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:
已知:
 可溶于水
可溶于水 和
和 都是酸性氧化物。
都是酸性氧化物。(1)“焙烧”时,
 与
与 反应生成
反应生成 、
、 、
、 和
和 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(2)硒与硝酸反应产生的尾气可以用
(3)
 是弱酸,
是弱酸, ,
, 和
和 溶液反应的离子方程式为
溶液反应的离子方程式为(4)分离
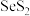 的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是
的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是已知:布氏漏斗是漏斗上面板上有很多小孔,上面板上放滤纸。抽滤的原理是水龙头冲水排气,使瓶内压强小于外界大气压,从而在漏斗上方形成压力加快抽滤速率。

(5)以石墨为阳极,“电解”时阴极的电极反应式为
(6)已知阳极泥中Se的质量分数为2%,100t该阳极泥在上述转化中硒的总提取率为80%,得到的
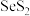 的质量为
的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】本次亚运会火炬燃料甲醇是利用焦炉气中的氢气(H2)与从工业尾气中捕集的二氧化碳(CO2)合成,并由远程甲醇动力重卡提供运输保障。
Ⅰ.二氧化碳加氢制甲醇的总反应可表示为:CO2(g) + 3H2(g)=CH2OH(g) + H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g) +H2(g)=CO(g) + H2O(g) ΔH1 = +41 kJ·mol-1
②CO (g) + 2H2(g)=CH3OH(g) ΔH2 = -90 kJ·mol-1
(1)总反应的 ΔH=___________ kJ·mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
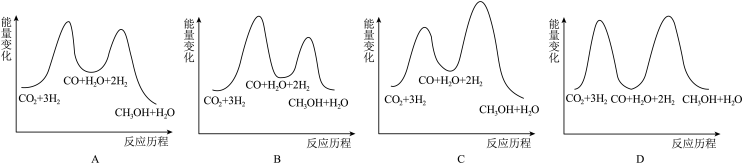
(2)甲醇可作为燃料使用,也可用CH3OH 和O2组合形成质子交换膜燃料电池,其结构示意图如图所示:
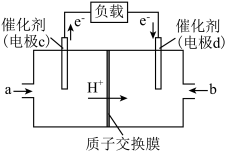
①电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极的反应方程式___________
②下图是一个电化学过程的装置示意图。 已知甲池的总反应式为 2CH3OH+3O2+4KOH=2K2CO3+6H2O
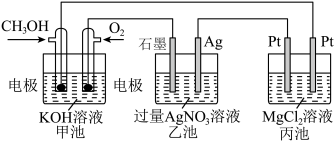
a.甲池是___________ (填“原电池”或“电解池”),通入O2的电极作___________ 极;
b.乙池是___________ (填“原电池”或“电解池”),石墨电极为___________ 极, 电极反应式为___________ 。乙池中总反应的离子方程式为___________ 。一段时间后丙池___________ 极(填“阴极”或“阳极”)附近有白色浑浊出现。
c. 当乙池中Ag极的质量增加5.40 g时, 甲池中理论上消耗O₂___________ mL(标准状况)。
(3)回收并利用CO₂一直是科研人员研究的热点。2021年,中科院天津工业生物技术研究所成果“无细胞化学酶系统催化CO₂合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设NA为阿伏加德罗常数的值。下列说法错误的是

(4)利用两种金属催化剂,在水溶液体系中将CO2分别转化为CO和 HCOOH的反应过程示意图如图:

下列说法正确的是___________
(5)CO用于处理大气污染物 N2O 的反应为 CO(g)+N2O(g)=CO2(g)+N2(g)。在Zn⁺作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。


总反应:CO(g)+N2O(g)=CO2(g)+N2(g) ΔH=______ kJ/mol;该总反应的决速步是反应___________ (填“①”或“②”)。
Ⅰ.二氧化碳加氢制甲醇的总反应可表示为:CO2(g) + 3H2(g)=CH2OH(g) + H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g) +H2(g)=CO(g) + H2O(g) ΔH1 = +41 kJ·mol-1
②CO (g) + 2H2(g)=CH3OH(g) ΔH2 = -90 kJ·mol-1
(1)总反应的 ΔH=

(2)甲醇可作为燃料使用,也可用CH3OH 和O2组合形成质子交换膜燃料电池,其结构示意图如图所示:

①电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极的反应方程式
②下图是一个电化学过程的装置示意图。 已知甲池的总反应式为 2CH3OH+3O2+4KOH=2K2CO3+6H2O

a.甲池是
b.乙池是
c. 当乙池中Ag极的质量增加5.40 g时, 甲池中理论上消耗O₂
(3)回收并利用CO₂一直是科研人员研究的热点。2021年,中科院天津工业生物技术研究所成果“无细胞化学酶系统催化CO₂合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设NA为阿伏加德罗常数的值。下列说法错误的是

| A.反应①中消耗44gCO2, 转移电子数为6NA |
| B.反应③中 cat为催化剂,实验室常用MnO2催化该反应 |
| C.30g HCHO与DHA 的混合物中所含氧原子数为2 NA |
| D.淀粉与纤维素的分子式相同,但不互为同分异构体 |

下列说法正确的是___________
| A.在转化为CO 的路径中,只涉及碳氧键的断裂和氧氢键的形成 |
| B.在转化为HCOOH的路径中,CO2被氧化为HCOOH |
| C.两个转化路径均有非极性键的形成 |
| D.上述反应过程说明催化剂具有选择性 |


总反应:CO(g)+N2O(g)=CO2(g)+N2(g) ΔH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】I.某实验小组同学利用如图装置对电化学原理进行了一系列探究活动。
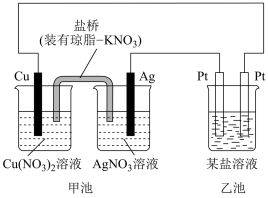
(1)甲池装置为_______ (填“原电池”或“电解池”)。
(2)甲池反应前两电极质量相等,一段时间后,两电极质量相差14g,导线中通过_______ mol电子。
(3)实验过程中,甲池左侧烧杯中 的浓度
的浓度_______ (填“增大”、“减小”或“不变”)。
(4)若乙池中溶液为足量的硝酸银溶液,工作一段时间后,若要使乙池中溶液恢复原浓度,可向溶液中加入_______ 。(填化学式)
(5)若把乙池改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),电解质溶液为 溶液,则下列说法正确的是_______。
溶液,则下列说法正确的是_______。
II.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。

(6)电解池A中发生的电解化学方程式是_______ 。
(7)图中Y是_______ (填化学式),若电解产生11.2L(标准状况)该物质,则至少转移电子_______ mol;
(8)分析图可知:氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

(1)甲池装置为
(2)甲池反应前两电极质量相等,一段时间后,两电极质量相差14g,导线中通过
(3)实验过程中,甲池左侧烧杯中
 的浓度
的浓度(4)若乙池中溶液为足量的硝酸银溶液,工作一段时间后,若要使乙池中溶液恢复原浓度,可向溶液中加入
(5)若把乙池改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),电解质溶液为
 溶液,则下列说法正确的是_______。
溶液,则下列说法正确的是_______。| A.电解过程中,阳极减少的质量与阴极增加的质量相等 |
| B.乙池左侧电极为粗铜,发生氧化反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 |
| D.杂质都将以单质的形式沉淀到池底 |
II.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。

(6)电解池A中发生的电解化学方程式是
(7)图中Y是
(8)分析图可知:氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.车用燃料技术的研究受到广泛关注,目前利用氢能的氢氧燃料电池技术较成熟。某兴趣小组想探究氢氧燃料电池反应的工作原理,设计如图(a)所示的实验装置。实验前,U 型管中装满溶液,电极均为铂电极。

(1)I池为 1 (填“原电池”、“电解池”),判断A、B的电极名称的依据是: 2 B极的电极反应式: 3
(2)通电一段时间后,滤纸上发生明显颜色变化,则发生反应的化学方程式为 4
(3)Ⅱ池中电极具有导电和 5 的作用,写出D的电极反应式: 6
Ⅱ.该兴趣小组查阅资料发现,现有的技术在原料氢气的储存和运输方面都存在安全隐患.2017年3月大连理工大学研究以“铂一碳化钼催化甲醇和水液化重组制备氢气”的新方法获得重大突破,并在美国《自然》杂志发表,具体原理如上图(b)所示:

(4)过程Ⅱ属于 7 (填“吸热”或“放热)过程。
(5)依据下表完成总反应的热化学方程式: 8
(6)天然气是一种清洁的化石燃料,也可以在一定的条件下与水反应产生CO2和H2,若生产等量氢气,则消耗甲醇和甲烷的质量比为: 9 。

(1)I池为
(2)通电一段时间后,滤纸上发生明显颜色变化,则发生反应的化学方程式为
(3)Ⅱ池中电极具有导电和
Ⅱ.该兴趣小组查阅资料发现,现有的技术在原料氢气的储存和运输方面都存在安全隐患.2017年3月大连理工大学研究以“铂一碳化钼催化甲醇和水液化重组制备氢气”的新方法获得重大突破,并在美国《自然》杂志发表,具体原理如上图(b)所示:

(4)过程Ⅱ属于
(5)依据下表完成总反应的热化学方程式:
| 化学键 | C=O | H-H | C-O | H-O | C-H |
| E/(kJ/mol) | 803 | 436 | 326 | 464 | 414 |
(6)天然气是一种清洁的化石燃料,也可以在一定的条件下与水反应产生CO2和H2,若生产等量氢气,则消耗甲醇和甲烷的质量比为:
您最近一年使用:0次



