(1)84消毒液的有效成分是_____ 。
(2)O2F2为共价化合物,各原子均满足8电子稳定结构,写出O2F2的电子式_____ 。
(3)NaOH的碱性比Mg(OH)2强,主要原因是_____ 。
(2)O2F2为共价化合物,各原子均满足8电子稳定结构,写出O2F2的电子式
(3)NaOH的碱性比Mg(OH)2强,主要原因是
19-20高三下·浙江温州·阶段练习 查看更多[2]
更新时间:2020-03-11 11:49:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】我国空间站“天和”核心舱太阳翼电池采用自主研发的砷化镓器件,能量转化效率大大提高。已知:砷( )与镓(
)与镓( )同位于第四周期;
)同位于第四周期; 与
与 同主族,
同主族, 与P同主族。
与P同主族。
(1)P在元素周期表中的位置是___________ ,镓的原子结构示意图为___________ 。
(2)非金属性强弱S___________ P(填“大于”或“小于”),下列表述中能证明这一事实的是___________ (填字母)。
a.S的简单氢化物的水溶液比P的简单氢化物的水溶液酸性强
b.S最高价氧化物对应的水化物的酸性强于P最高价氧化物对应的水化物的酸性
c.在反应中,P原子得电子数比S原子得电子数多
d.S的简单阴离子的还原性比P的简单阴离子的还原性弱
(3)下列关于 的推断正确的是
的推断正确的是___________ (填序号)。
① 的最高正价为+5;②原子半径:
的最高正价为+5;②原子半径: ;③元素的金属性:
;③元素的金属性:
(4) ,的酸性由强到弱的关系是
,的酸性由强到弱的关系是___________ 。
(5) 与
与 在一定条件下化合为
在一定条件下化合为 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:___________ 。
 )与镓(
)与镓( )同位于第四周期;
)同位于第四周期; 与
与 同主族,
同主族, 与P同主族。
与P同主族。(1)P在元素周期表中的位置是
(2)非金属性强弱S
a.S的简单氢化物的水溶液比P的简单氢化物的水溶液酸性强
b.S最高价氧化物对应的水化物的酸性强于P最高价氧化物对应的水化物的酸性
c.在反应中,P原子得电子数比S原子得电子数多
d.S的简单阴离子的还原性比P的简单阴离子的还原性弱
(3)下列关于
 的推断正确的是
的推断正确的是①
 的最高正价为+5;②原子半径:
的最高正价为+5;②原子半径: ;③元素的金属性:
;③元素的金属性:
(4)
 ,的酸性由强到弱的关系是
,的酸性由强到弱的关系是(5)
 与
与 在一定条件下化合为
在一定条件下化合为 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)氟原子激发态的电子排布式有______ ,其中能量较高的是______ 。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的______ 区,写出该基态原子电子排布式为______ 。
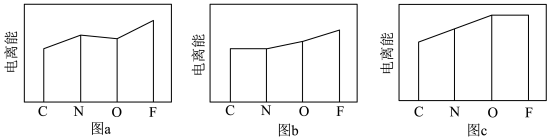
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是______ (填标号),判断的根据是______ ;第三电离能的变化图是______ (填标号)。
(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
①元素的电负性:Z______ W(填“大于”“小于”或“等于”)。
②简单离子半径:W______ Y(填“大于”“小于”或“等于”)。
③氢化物的稳定性:X______ Z(填“大于”“小于”或“等于”)。
(1)氟原子激发态的电子排布式有
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | H3ZO4 | |||
| 0.1 mol∙L−1溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】钛和钛的合金已广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
①Ti 元素在元素周期表中的位置是第_____ 周期,第_____ 族;基态原子的电子排布式为_____ ;按电子排布Ti 元素在元素周期表分区中_____ 区
②现有 Ti3+的配合物化学式为[TiCl(H2O)5 ]Cl2H2O。配离子[TiCl(H2O)5]2+ 中含有的化学键类型是_____ ,_____ 。该配合物的配体是_____ 、_____
①Ti 元素在元素周期表中的位置是第
②现有 Ti3+的配合物化学式为[TiCl(H2O)5 ]Cl2H2O。配离子[TiCl(H2O)5]2+ 中含有的化学键类型是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如表为元素周期表的一部分。
(1)表中元素___ 的非金属性最强;元素___ 的金属性最强;元素___ 的单质在室温下呈液态(填写元素符号)。
(2)表中元素③的原子结构示意图是___ 。
(3)表中元素⑥、⑦氢化物的稳定性顺序为___ >___ (填写化学式,下同)。
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是___ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ⑤ | |||||
| 3 | ③ | ⑥ | |||||
| 4 | ④ | ⑦ | |||||
(1)表中元素
(2)表中元素③的原子结构示意图是
(3)表中元素⑥、⑦氢化物的稳定性顺序为
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表列出了①~⑥六种元素在周期表中的位置。
请按要求回答下列问题:
(1)写出①的元素符号___________________ 。
(2)⑥的原子结构示意图是_______________ 。
(3)写出③与⑤的单质反应的化学方程式__________________________ 。
(4)③和④中金属性较弱的是_______________ (填化学式)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(1)写出①的元素符号
(2)⑥的原子结构示意图是
(3)写出③与⑤的单质反应的化学方程式
(4)③和④中金属性较弱的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)元素周期表有______ 个横行、________________ 个周期,每一周期中元素原子的_________ 相同,从左到右原子半径依次___________________ (填“增大”或“减小”)、核对外层电子的引力逐渐________ (填“增强”或“减弱”) 、元素失电子能力逐渐________ (填“增强”或“减弱”)、元素的非金属性________ (填“增强”或“减弱”)、阴离子的还原性_________ (填“增强”或“减弱”)、最高价氧化物对应水化物酸性________ (填“增强”或“减弱”)、气态氢化物的稳定性________ (填“增强”或“减弱”);
(2)元素周期表有____ 纵列、_______________ 个族,第ⅥA族处在第_______ 列,同一主族从上到下,元素的金属性依次_________ (填“增强”或“减弱”)、元素失电子的能力________ (填“增强”或“减弱”)、阳离子的氧化性________ (填“增强”或“减弱”)、最高价氧化物对应水化物酸性________ (填“增强”或“减弱”)。
(2)元素周期表有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】一定条件下,氨与氟气发生反应: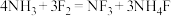 。其中
。其中 空间结构与
空间结构与 相似。
相似。
(1)写出反应物生成物中共价化合物的化学式___________ 。
(2)反应物、生成物中各原子均满足8电子稳定结构的是___________ 。
(3)书写 的电子式
的电子式___________ 。
(4) 所含的化学键为
所含的化学键为___________ 。
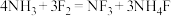 。其中
。其中 空间结构与
空间结构与 相似。
相似。(1)写出反应物生成物中共价化合物的化学式
(2)反应物、生成物中各原子均满足8电子稳定结构的是
(3)书写
 的电子式
的电子式(4)
 所含的化学键为
所含的化学键为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】NH3是制备氮肥的原料之一。
(1)写出NH3的电子式。___________
(2)下列关于NH3的说法错误的是___________。
(1)写出NH3的电子式。
(2)下列关于NH3的说法错误的是___________。
| A.极易溶于水 | B.可用作制冷剂 | C.属于电解质 | D.属于共价化合物 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】I.有以下6种物质:①Ne;②HCl;③P4;④H2O2;⑤Na2S;⑥NaOH,请用物质的序号填空:
(1)不存在化学键的是___________ ;
(2)只存在极性共价键的是___________ ;
(3)只存在非极性共价键的是___________ ;
(4)既存在非极性共价键又存在极性共价键的是___________ ;
(5)只存在离子键的是___________ ;
(6)既存在离子键又存在共价键的是___________ 。
Ⅱ.在下列变化中:①I2升华②烧碱熔化③NaCl溶于水④HCl溶于水⑤O2溶于水⑥Na2O2溶于水。
(1)未破坏化学键的是___________ (填序号,下同);
(2)仅离子键被破坏的是___________ ;
(3)仅共价键被破坏的是___________ ;
(4)离子键和共价键同时被破坏的是___________ 。
(1)不存在化学键的是
(2)只存在极性共价键的是
(3)只存在非极性共价键的是
(4)既存在非极性共价键又存在极性共价键的是
(5)只存在离子键的是
(6)既存在离子键又存在共价键的是
Ⅱ.在下列变化中:①I2升华②烧碱熔化③NaCl溶于水④HCl溶于水⑤O2溶于水⑥Na2O2溶于水。
(1)未破坏化学键的是
(2)仅离子键被破坏的是
(3)仅共价键被破坏的是
(4)离子键和共价键同时被破坏的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】用序号按要求回答问题:
下列物质:①N2②CO2③NH3④氩气⑤Na2O2⑥NaOH⑦CaBr2⑧H2O2⑨NH4Cl⑩HBr。
(1)只含非极性键的是______ 。
(2)含有极性键和非极性键的是______ 。
(3)含有极性键的离子化合物是______ 。
(4)不含离子键和共价键的是______ 。
下列物质:①N2②CO2③NH3④氩气⑤Na2O2⑥NaOH⑦CaBr2⑧H2O2⑨NH4Cl⑩HBr。
(1)只含非极性键的是
(2)含有极性键和非极性键的是
(3)含有极性键的离子化合物是
(4)不含离子键和共价键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】实验室有如下物质:①熔融的氢氧化钠② 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体
(1)上述状态下可导电的是______ ;
(2)属于电解质的是______ ;
(3)属于非电解质的是______ ;
(4)上述状态下的电解质不能导电的是______ 。
 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)上述状态下的电解质不能导电的是
您最近一年使用:0次

 ②
② ③
③ ⑤
⑤ ⑥
⑥ ⑦乙烯⑧
⑦乙烯⑧
 融化③
融化③ 溶于水④
溶于水④ 溶于水⑤氢气在氧气中燃烧⑥
溶于水⑤氢气在氧气中燃烧⑥

