铁及其化合物与生产、生活关系密切
(1)生铁是通过高炉冶炼而得,用化学方程式表示其原理为______________________ 。冶炼过程中,即被氧化又被还原的元素是(填元素符号)____________ ;
(2)铁在一定条件下可与多种非金属单质反应,铁与氯气反应的化学方程式为___________________ ,铁与硫反应的化学方程式为__________________________ 。
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
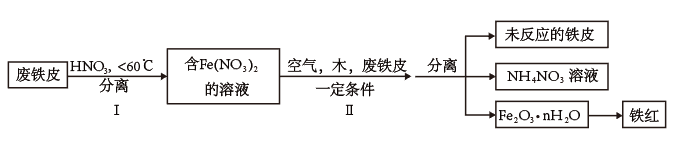
①步骤I若要检验是否有Fe3+生成,方法是____________ ,离子方程式为_________ 。
②步骤II中发生反应:4Fe(NO3)2+O2+(2n+4)H2O→2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为________________ 。
③上述生产流程中,能体现“绿色化学”思想的是_____________________ (任写一项)。
(1)生铁是通过高炉冶炼而得,用化学方程式表示其原理为
(2)铁在一定条件下可与多种非金属单质反应,铁与氯气反应的化学方程式为
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤I若要检验是否有Fe3+生成,方法是
②步骤II中发生反应:4Fe(NO3)2+O2+(2n+4)H2O→2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为
③上述生产流程中,能体现“绿色化学”思想的是
14-15高二上·上海闵行·期中 查看更多[1]
(已下线)上海市七宝中学2014-2015学年高二上学期期中考试化学试题
更新时间:2020-03-22 15:38:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学在研究Fe与H2SO4的反应时,进行了如下实验。

(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为______ 。
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是______ 。
(3)实验Ⅲ中,加热后产生大量气体,B试管中溶液的红色褪去,D处始终未检测到可燃性气体。C试管中反应的离子方程式是______ 。
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同。浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于______ 。
②造成反应多样性的主要因素有______ 。

(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是
(3)实验Ⅲ中,加热后产生大量气体,B试管中溶液的红色褪去,D处始终未检测到可燃性气体。C试管中反应的离子方程式是
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同。浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于
②造成反应多样性的主要因素有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:

(1)若A为淡黄色固体,物质A和D的摩尔质量相等,请写出B和F溶液反应生成C的离子方程式:_____ 。
(2)若物质A中一种元素原子的最外层电子数为其电子总数的 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O 反应的化学方程式:
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O 反应的化学方程式:________ 。
(3)若常温下A为有色气体,F是一种金属单质。请写出B和适量F反应生成C与气体E的离子方程式:_______ ;简述D溶液中的金属阳离子的检验方法______ 。

(1)若A为淡黄色固体,物质A和D的摩尔质量相等,请写出B和F溶液反应生成C的离子方程式:
(2)若物质A中一种元素原子的最外层电子数为其电子总数的
 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O 反应的化学方程式:
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O 反应的化学方程式:(3)若常温下A为有色气体,F是一种金属单质。请写出B和适量F反应生成C与气体E的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学在实验室研究Fe与H2SO4的反应

【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为___ 。
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,这一现象被称为___ 。
(3)实验Ⅲ,加热试管A,生成硫酸铁和SO2气体,写出化学方程式___ 。
B中可用于检验产生气体为SO2的试剂有___ 。
A.BaCl2溶液 B.品红溶液 C.酸性高锰酸钾溶液 D.饱和NaHSO3溶液
(4)实验Ⅲ过程中,D处始终未检测到可燃性气体;结束后,经检验A中既有Fe3+又有大量Fe2+,产生Fe2+的原因可能是___ (写离子方程式);检验反应后溶液中含有Fe2+的具体操作方法是___ 。
【实验反思】
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:影响反应产物的可能因素有___ 。

【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,这一现象被称为
(3)实验Ⅲ,加热试管A,生成硫酸铁和SO2气体,写出化学方程式
B中可用于检验产生气体为SO2的试剂有
A.BaCl2溶液 B.品红溶液 C.酸性高锰酸钾溶液 D.饱和NaHSO3溶液
(4)实验Ⅲ过程中,D处始终未检测到可燃性气体;结束后,经检验A中既有Fe3+又有大量Fe2+,产生Fe2+的原因可能是
【实验反思】
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:影响反应产物的可能因素有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A一J是中学化学中常见的物质,其相互转化关系如下图所示,反应条件均已略去。A、B常温下均为无色液体,且均由两种相同的元素组成;C、F、G均为非金属单质,常温下C、F为无色气体,G可用于制取“84”消毒液;D是应用最广泛的金属;J溶液中滴入KSCN 溶液显红色。

回答下列问题:
(1)A的化学式是_________ 。
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是______ 。
(3)B和G能发生反应,写出反应的离子方程式______ 。
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:______ 。

回答下列问题:
(1)A的化学式是
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是
(3)B和G能发生反应,写出反应的离子方程式
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】铝热反应的本质是利用铝的还原性,将难熔金属从其氧化物中置换出来,关于铝热反应解答下列问题:
(1)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有________ 。
A.KCl B.KClO3 C.MnO2 D.Mg
(2)用等物质的量的MgO和Fe2O3组成的混合物在一定条件下与Al粉进行铝热反应。
①引发铝热反应的操作是__________________________________ 。
②产物中单质是________ (写名称)。
(3)取少量(1)中铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,________ (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是______ (用离子方程式说明)。
(1)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
A.KCl B.KClO3 C.MnO2 D.Mg
(2)用等物质的量的MgO和Fe2O3组成的混合物在一定条件下与Al粉进行铝热反应。
①引发铝热反应的操作是
②产物中单质是
(3)取少量(1)中铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】为探索工业含铝、铁、铜合金废料的再利用,某同学设计的回收利用方案如图:

(1)“滤渣B”的主要成分为_____ (填化学式)。
(2)加入NaOH溶液发生反应的化学方程式:_____ 。
(3)检验“滤液D”是否含有Fe3+的方法为_____ 。
(4)从“滤液D”得到绿矾晶体,须进行的操作为_____ 、过滤、洗涤、干燥。
(5)试剂Y最可能为_____ (填标号)
(6)反应①的离子方程式:_____ 。
(7)工业上常用“滤液D”制得净水剂Na2FeO4,流程如图:

测得“滤液D”中c(Fe2+)为0.4mol•L-1,若要处理0.1m3“滤液D”,理论上需要消耗20%的H2O2溶液_____ kg。

(1)“滤渣B”的主要成分为
(2)加入NaOH溶液发生反应的化学方程式:
(3)检验“滤液D”是否含有Fe3+的方法为
(4)从“滤液D”得到绿矾晶体,须进行的操作为
(5)试剂Y最可能为
| A.Cl2 | B.H2 | C.H2O2 | D.SO2 |
(7)工业上常用“滤液D”制得净水剂Na2FeO4,流程如图:

测得“滤液D”中c(Fe2+)为0.4mol•L-1,若要处理0.1m3“滤液D”,理论上需要消耗20%的H2O2溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题:
(1)我国某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。

①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定图中相应工厂的名称: A.___________ ,B.___________ ,C.___________ ,D.___________ ;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式:___________ ;
(2)玻璃钢可由酚醛树脂和玻璃纤维制成。
①酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜___________ 地加入甲醛,且反应釜应装有___________ 装置。
②玻璃钢中玻璃纤维的作用是___________ 。玻璃钢具有___________ 等优异性能(写出两点即可)。
③下列处理废旧热固性酚醛塑料的做法合理的是___________ 。
a.深埋 b.粉碎后用作树脂填料
c.用作燃料 d.用有机溶剂将其溶解,回收树脂
(3)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=___________ ,实际生产要将r值维持在1.7~2.2之间,原因是___________ 。

(1)我国某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。

①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定图中相应工厂的名称: A.
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式:
(2)玻璃钢可由酚醛树脂和玻璃纤维制成。
①酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜
②玻璃钢中玻璃纤维的作用是
③下列处理废旧热固性酚醛塑料的做法合理的是
a.深埋 b.粉碎后用作树脂填料
c.用作燃料 d.用有机溶剂将其溶解,回收树脂
(3)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】除金、铂等极少数金属外,绝大多数金属元素以化合物形式存在于自然界中,将金属元素从其化合物中还原出来的工业工程称为金属的冶炼。下列材料描述了部分常见金属的冶炼方法。
①工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电解熔融的氯化镁;皮江法是硅在高温下还原氧化镁 。
②霍尔-埃鲁铝电解法是以氧化铝为原料、冰晶石(Na3AlF6)为熔剂组成的电解质,在950-970℃的条件下通过电解的方法使电解质熔体中的氧化铝分解为铝和氧气。
③冶炼锰一般用铝热法,即在高温下用铝还原二氧化锰。
④相关各物质熔点见下表:
Ⅰ.根据上述信息回答下列问题:
(1)冶炼镁时电解熔融MgCl2而不电解熔融MgO的原因是_______
(2)将铝和镁作电极插入稀硫酸中,镁、铝分别作_______ 极、_______ 极;写出正极的电极反应式:_______ 。
Ⅱ.下面是皮江法冶炼镁的工业流程示意图:

(3)气体a是_______ 。
(4)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有_______ 、_______ 。
(5)还原炉中抽空气到近似真空的原因是_______ 。
①工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电解熔融的氯化镁;皮江法是
②霍尔-埃鲁铝电解法是以氧化铝为原料、冰晶石(Na3AlF6)为熔剂组成的电解质,在950-970℃的条件下通过电解的方法使电解质熔体中的氧化铝分解为铝和氧气。
③冶炼锰一般用铝热法,即在高温下用铝还原二氧化锰。
④相关各物质熔点见下表:
| 物质 | Al2O3 | AlCl3 | MgO | MgCl2 | Al | Mn | Mg |
| 熔点/℃ | 2303 | 190 | 2800 | 712 | 660 | 1244 | 649 |
Ⅰ.根据上述信息回答下列问题:
(1)冶炼镁时电解熔融MgCl2而不电解熔融MgO的原因是
(2)将铝和镁作电极插入稀硫酸中,镁、铝分别作
Ⅱ.下面是皮江法冶炼镁的工业流程示意图:

(3)气体a是
(4)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有
(5)还原炉中抽空气到近似真空的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图。根据上述产业流程回答下列问题:

(1)从原料、能源、交通角度考虑该企业应建在______
A西部山区 B沿海地区 C发达城市 D东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①______ 、②______ 、③______ 、④______ 、⑤______ 。
(3)沸腾炉发生反应的化学方程式:______ ;磷肥厂的主要产品是普钙,其主要成分是______ (填化学式)。
(4)热电厂的冷却水是______ ,该流程中浓缩盐水除提取盐以外还可提取的物质有______ (写出一种即可)。
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。______ ,______ (写出两点即可)。

(1)从原料、能源、交通角度考虑该企业应建在
A西部山区 B沿海地区 C发达城市 D东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①
(3)沸腾炉发生反应的化学方程式:
(4)热电厂的冷却水是
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】紫菜与海带类似,是一种富含生物碘的海洋植物。商品紫菜轻薄松脆、比海带更易被焙烧成灰实验室里从紫菜中提取碘的流程如下图:
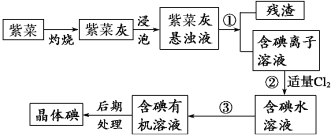
(1)实验室焙烧紫菜,需要下列仪器中的________ (填序号)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①________ ,③______ 。
(3)提取碘的过程中,可选择的有机试剂是( )
A.酒精 B.苯 C.乙酸 D.食盐水
选择该试剂的理由是___________________________________ 。
(4)为使紫菜灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有______________ 、________________ 。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,观察下面实验装置图改正其中的错误之处:

①_________________________________________ ;
②_________________________________________ ;
③_________________________________________ 。
(6)进行上述蒸馏操作时,使用水浴加热,最后晶态碘在____ 里聚集。

(1)实验室焙烧紫菜,需要下列仪器中的
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程中,可选择的有机试剂是
A.酒精 B.苯 C.乙酸 D.食盐水
选择该试剂的理由是
(4)为使紫菜灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,观察下面实验装置图改正其中的错误之处:

①
②
③
(6)进行上述蒸馏操作时,使用水浴加热,最后晶态碘在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】信息时代产生的电子垃圾处理不当会对环境构成威胁。某研究小组将废弃的线路板处理后,得到含Cu、Al及少量Fe的金属混合物,并设计如下流程制备硫酸铜和硫酸铝晶体。

请回答:
(1)步骤①~③所涉及的实验操作方法中,属于过滤的是______ (填序号)。
(2)步骤①中Cu、Al、Fe均能与稀硫酸和浓硝酸的混合物在加热条件下反应,其中氮元素全部转化为NO。该步骤中稀硫酸的作用是______ 。
(3)下列关于步骤②的说法正确的是______ (填字母)。
a 沉淀B为白色固体
b H2O2的作用是将Fe2+氧化为Fe3+
c 可以用Ba(OH)2溶液替换NaOH溶液
(4)已知AlO2-+ 4H+=Al3+ + 2H2O。由沉淀B制取Al2(SO4)3·18H2O的操作是:将沉淀B转移到烧杯中,______ ,将溶液加热蒸发、冷却结晶、过滤得到产品。

请回答:
(1)步骤①~③所涉及的实验操作方法中,属于过滤的是
(2)步骤①中Cu、Al、Fe均能与稀硫酸和浓硝酸的混合物在加热条件下反应,其中氮元素全部转化为NO。该步骤中稀硫酸的作用是
(3)下列关于步骤②的说法正确的是
a 沉淀B为白色固体
b H2O2的作用是将Fe2+氧化为Fe3+
c 可以用Ba(OH)2溶液替换NaOH溶液
(4)已知AlO2-+ 4H+=Al3+ + 2H2O。由沉淀B制取Al2(SO4)3·18H2O的操作是:将沉淀B转移到烧杯中,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化钡是重要的化工原料,是制备其他钡盐的主要中间原料,以毒重石(主要成分为BaCO3,还含有SiO2及含Ca、Mg、Fe、Al的化合物)为原料制备BaCl2·2H2O的工艺流程如下:
回答下列问题:
(1)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
分析表中数据,温度越高钡的浸出率越低的可能原因是___________ ;判断“浸取”的最佳液固比为___________ 。
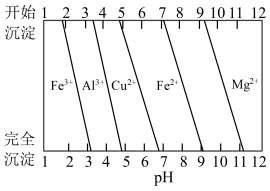
(2)常温时,几种金属离子沉淀的pH如图所示,加H2O2时发生反应的离子方程式为___________ 。“调pH(I)”时,调节溶液pH≈5,则“滤渣II”的主要成分为___________ (填化学式)。
①滴定至终点时的现象为___________ 。
②该溶液中钙离子的浓度为___________ g·mL-1(用含 V1、V2的代数式表示,必须化简)。

回答下列问题:
(1)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
| 改变的条件 | 温度(℃) | 盐酸的浓度(%) | 液固比 | ||||||||
| 30 | 55 | 75 | 10 | 15 | 20 | 25 | 3:1 | 4:1 | 5:1 | 6:1 | |
| 钡的浸出率(%) | 74.3 | 69.6 | 68.4 | 59.2 | 74.3 | 74.2 | 55.3 | 59.8 | 65.1 | 74.3 | 74.4 |
(2)常温时,几种金属离子沉淀的pH如图所示,加H2O2时发生反应的离子方程式为
①滴定至终点时的现象为
②该溶液中钙离子的浓度为
您最近一年使用:0次



