钨在自然界主要以钨(+6价)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4、MnWO4。黑钨矿冶炼金属钨的流程如下图(已知:钨酸是一种难溶性强酸、对热不稳定)。其中A、B、C都是钨的化合物。完成下列填空:
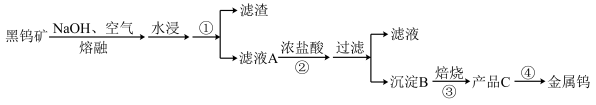
(1)上述从黑钨矿获得单质钨的过程中属于氧化还原反应的是(填数字序号)__________ 。
(2)操作①的名称为__________ ,得到的滤液为钨酸的钠盐,写出反应②的化学方程式______________ 。该过程中产品C为_________ ,从产品C获得纯度较高的钨的另一反应原料应该为___________ 。
(3)若制得的钨中含有少量金属铁,为测定其中金属钨的含量(已知金属钨不溶于盐酸),甲同学用下列装置进行测定:

相关实验步骤:
①加好称量好的样品和盐酸,记录B的液面位置;
②检查气密性。
③待A中不再有气体产生并恢复至室温后,记录B的液面位置;
④将A中盐酸与样品混合;
正确的操作顺序是_________________ (填序号)
(4)若实验用样品的质量为a g,加入20mL盐酸与之充分反应后,测得排出水的体积为VL(标准状况下),测得的H2的体积应为___________ L,样品中的钨的质量分数的计算式为______________ 。
(5)在读取C装置液面数据时,应先____________ ,再平视读数,若样品中含有不溶于酸,也不与酸反应的物质,则测得钨的质量分数将_________ (填“偏大”、“偏小”或“不受影响”)。

(1)上述从黑钨矿获得单质钨的过程中属于氧化还原反应的是(填数字序号)
(2)操作①的名称为
(3)若制得的钨中含有少量金属铁,为测定其中金属钨的含量(已知金属钨不溶于盐酸),甲同学用下列装置进行测定:

相关实验步骤:
①加好称量好的样品和盐酸,记录B的液面位置;
②检查气密性。
③待A中不再有气体产生并恢复至室温后,记录B的液面位置;
④将A中盐酸与样品混合;
正确的操作顺序是
(4)若实验用样品的质量为a g,加入20mL盐酸与之充分反应后,测得排出水的体积为VL(标准状况下),测得的H2的体积应为
(5)在读取C装置液面数据时,应先
更新时间:2020-03-23 09:24:15
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】乙酰水杨酸,俗称阿司匹林(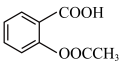 ),是常用的解热镇痛药。合成原理:
),是常用的解热镇痛药。合成原理:
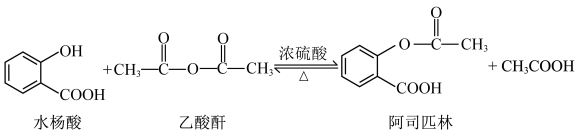
查阅资料:
阿司匹林:相对分子质量为180,分解温度为128~135℃,溶于乙醇、难溶于水;
水杨酸:相对分子质量为138,溶于乙醇、微溶于水;
乙酸酐:相对分子质量为102,无色透明液体,遇水形成乙酸。
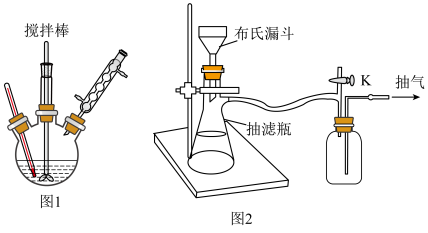
制备过程:
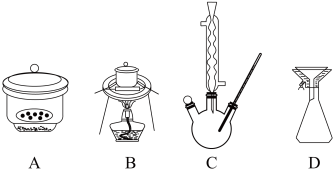
①如图1向三颈烧瓶中加入3.45g水杨酸、新蒸出的乙酸酐20mL(ρ=1.08g·mL-1),再加10滴浓硫酸反复振荡后,连接回流装置,搅拌,70℃加热半小时。
②冷却至室温后,将反应混合液倒入100mL冷水中,并用冰水浴冷却15min,用图2装置减压抽滤,将所有晶体收集到布氏漏斗中。抽滤过程中用少量冷水多次洗涤晶体,继续抽滤,尽量将溶剂抽干,得到乙酰水杨酸粗品。
提纯过程(重结晶法):
③将粗产品转至烧瓶中,装好回流装置,向烧瓶内加入100mL乙酸乙酯和2粒沸石,加热回流,进行热溶解。然后趁热过滤,冷却至室温,抽滤,洗涤,干燥,得无色晶体状乙酰水杨酸。
(1)图1装置中仪器A的名称是___________ 。
(2)步骤①中加热宜采用___________ ,冷凝回流过程中外界的水可能进入三颈烧瓶,导致发生副反应___________ (用化学方程式作答),降低了水杨酸的转化率。
(3)步骤②用冷水洗涤晶体的目的是___________ ,用图2装置减压抽滤后的操作是___________ 。
(4)步骤③中肯定用不到的装置是___________ (填序号)。
重结晶时为了获得较大颗粒的晶体产品,查阅资料得到如下信息:
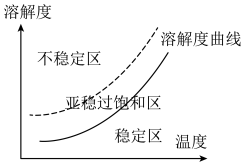
a.不稳定区出现大量微小晶核,产生较多小颗粒的晶体
b.亚稳过饱和区,加入晶种,晶体生长
c.稳定区晶体不可能生长
由信息和已有的知识分析,从温度较高浓溶液中获得较大晶体颗粒的操作为___________ 。
(5)最终称量产品质量为2.61g,则所得乙酰水杨酸的产率为___________ %(精确到0.01)。
 ),是常用的解热镇痛药。合成原理:
),是常用的解热镇痛药。合成原理:
查阅资料:
阿司匹林:相对分子质量为180,分解温度为128~135℃,溶于乙醇、难溶于水;
水杨酸:相对分子质量为138,溶于乙醇、微溶于水;
乙酸酐:相对分子质量为102,无色透明液体,遇水形成乙酸。

制备过程:
①如图1向三颈烧瓶中加入3.45g水杨酸、新蒸出的乙酸酐20mL(ρ=1.08g·mL-1),再加10滴浓硫酸反复振荡后,连接回流装置,搅拌,70℃加热半小时。
②冷却至室温后,将反应混合液倒入100mL冷水中,并用冰水浴冷却15min,用图2装置减压抽滤,将所有晶体收集到布氏漏斗中。抽滤过程中用少量冷水多次洗涤晶体,继续抽滤,尽量将溶剂抽干,得到乙酰水杨酸粗品。
提纯过程(重结晶法):
③将粗产品转至烧瓶中,装好回流装置,向烧瓶内加入100mL乙酸乙酯和2粒沸石,加热回流,进行热溶解。然后趁热过滤,冷却至室温,抽滤,洗涤,干燥,得无色晶体状乙酰水杨酸。
(1)图1装置中仪器A的名称是
(2)步骤①中加热宜采用
(3)步骤②用冷水洗涤晶体的目的是
(4)步骤③中肯定用不到的装置是

重结晶时为了获得较大颗粒的晶体产品,查阅资料得到如下信息:

a.不稳定区出现大量微小晶核,产生较多小颗粒的晶体
b.亚稳过饱和区,加入晶种,晶体生长
c.稳定区晶体不可能生长
由信息和已有的知识分析,从温度较高浓溶液中获得较大晶体颗粒的操作为
(5)最终称量产品质量为2.61g,则所得乙酰水杨酸的产率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】以炼锌厂的烟道灰 主要成分为ZnO,另含少量
主要成分为ZnO,另含少量 、CuO、
、CuO、 、MnO等
、MnO等 为原料可生产草酸锌晶体ZnSO4·2H2O,摩尔质量为189g/mol。
为原料可生产草酸锌晶体ZnSO4·2H2O,摩尔质量为189g/mol。
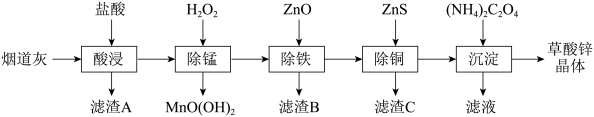
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
请问答下列问题:
(1)滤渣A的主要成分为_________ ,滤渣B的主要成分为_______________ 。
(2)除锰过程中产生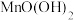 沉淀的离子方程式为
沉淀的离子方程式为_______________________ 。
(3) ①除铁 部分
部分 可能被除去
可能被除去 时加入ZnO控制反应液pH的范围为
时加入ZnO控制反应液pH的范围为______________ 。
②若某溶液中含有 ,可能含有
,可能含有 ,请设计实验证明
,请设计实验证明 的存在。
的存在。________ 。
(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是_______________ 。
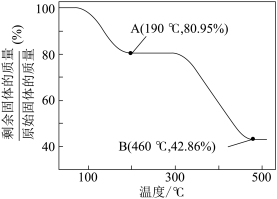
(5)将草酸锌晶体加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化如图所示, 范围内,发生反应的化学方程式为
范围内,发生反应的化学方程式为_________________ 。
 主要成分为ZnO,另含少量
主要成分为ZnO,另含少量 、CuO、
、CuO、 、MnO等
、MnO等 为原料可生产草酸锌晶体ZnSO4·2H2O,摩尔质量为189g/mol。
为原料可生产草酸锌晶体ZnSO4·2H2O,摩尔质量为189g/mol。
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 |  |  |  |  |
| 开始沉淀的pH |  | 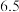 | 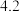 | 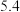 |
| 沉淀完全的pH |  | 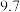 | 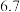 |  |
(1)滤渣A的主要成分为
(2)除锰过程中产生
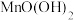 沉淀的离子方程式为
沉淀的离子方程式为(3) ①除铁
 部分
部分 可能被除去
可能被除去 时加入ZnO控制反应液pH的范围为
时加入ZnO控制反应液pH的范围为②若某溶液中含有
 ,可能含有
,可能含有 ,请设计实验证明
,请设计实验证明 的存在。
的存在。(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是
(5)将草酸锌晶体加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化如图所示,
 范围内,发生反应的化学方程式为
范围内,发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 是一种重要的无机功能材料,粗
是一种重要的无机功能材料,粗 的提纯是工业生产的重要环节。某研究性学习小组设计了将粗
的提纯是工业生产的重要环节。某研究性学习小组设计了将粗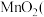 含有较多的MnO和
含有较多的MnO和 样品转化为纯
样品转化为纯 实验,其流程如下:
实验,其流程如下:
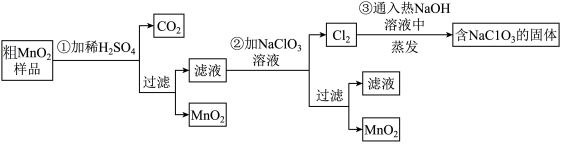
 第
第 步加稀
步加稀 时,粗
时,粗 样品中的
样品中的______  写化学式
写化学式 转化为可溶性物质。
转化为可溶性物质。
 第
第 步反应的离子方程式:
步反应的离子方程式: ______ 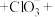
______ 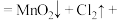
______
 第
第 步蒸发操作必需的仪器有铁架台
步蒸发操作必需的仪器有铁架台 含铁圈
含铁圈 、
、______ 、______ 、______ ,已知蒸发得到的固体中有 和NaOH,则一定还有含有
和NaOH,则一定还有含有______  写化学式
写化学式 。
。
 若粗
若粗 样品的质量为
样品的质量为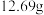 ,第
,第 步反应后,经过滤得到
步反应后,经过滤得到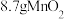 ,并收集到
,并收集到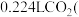 标准状况下
标准状况下 ,则在第
,则在第 步反应中至少需要
步反应中至少需要______ mol  。
。
 是一种重要的无机功能材料,粗
是一种重要的无机功能材料,粗 的提纯是工业生产的重要环节。某研究性学习小组设计了将粗
的提纯是工业生产的重要环节。某研究性学习小组设计了将粗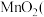 含有较多的MnO和
含有较多的MnO和 样品转化为纯
样品转化为纯 实验,其流程如下:
实验,其流程如下:
 第
第 步加稀
步加稀 时,粗
时,粗 样品中的
样品中的 写化学式
写化学式 转化为可溶性物质。
转化为可溶性物质。 第
第 步反应的离子方程式:
步反应的离子方程式: 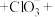
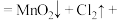
 第
第 步蒸发操作必需的仪器有铁架台
步蒸发操作必需的仪器有铁架台 含铁圈
含铁圈 、
、 和NaOH,则一定还有含有
和NaOH,则一定还有含有 写化学式
写化学式 。
。 若粗
若粗 样品的质量为
样品的质量为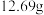 ,第
,第 步反应后,经过滤得到
步反应后,经过滤得到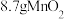 ,并收集到
,并收集到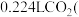 标准状况下
标准状况下 ,则在第
,则在第 步反应中至少需要
步反应中至少需要 。
。
您最近一年使用:0次
【推荐1】镁及其化合物是实验设计的热点载体,查阅资料。
某学习小组设计实验探究镁与二氧化氮反应的产物,提供的实验装置如图所示。
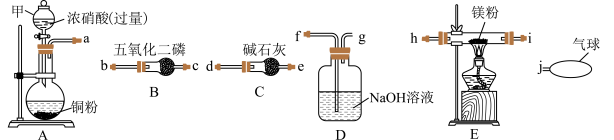
(1)仪器甲名称为_______ ,仪器接口顺序为a→______ ,______ →______ ,______ →______ ,______ →______ ,______ →j。
(2)装置A中的主要现象为_______ ,C装置的作用是_____ 。
(3)确定有N2生成的实验现象是________ 。
(4)经测定,Mg与NO2反应生成MgO、Mg3N2和N2,其中Mg3N2和N2的物质的量相等。E中发生反应的化学方程式为______ 。
(5)实验完毕后,设计实验确认产物中有Mg3N2,取少量C中残留固体于试管中滴加蒸馏水,_________ ,则产物中有氮化镁。
| ⅰ | 2NO2+2NaOH=NaNO2+NaNO3+H2O |
| ⅱ | Mg3N2与水反应 |

(1)仪器甲名称为
(2)装置A中的主要现象为
(3)确定有N2生成的实验现象是
(4)经测定,Mg与NO2反应生成MgO、Mg3N2和N2,其中Mg3N2和N2的物质的量相等。E中发生反应的化学方程式为
(5)实验完毕后,设计实验确认产物中有Mg3N2,取少量C中残留固体于试管中滴加蒸馏水,
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】BaS是一种重要的无机合成中间体,可以通过重晶石(主要成分BaSO4,还含有SiO2等杂质)制备得到。工业常以软锰矿(主要成分MnO2)和BaS为原料制备碳酸锰。
(1)制取BaS溶液
将重晶石与活性炭混合均匀,高温煅烧,冷却后得重晶石熟料。向重晶石熟料中加入热水,充分搅拌后过滤,得BaS溶液。
①SiO2的晶体类型是___ 。
②已知:室温下,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15。测得0.1mol·L-1BaS溶液pH≈13。溶液中OH—、S2—、HS—三种离子浓度由大到小的顺序是___ 。
③通过下列实验方法测定重晶石熟料中BaS的质量分数:
步骤Ⅰ:准确称取10.00g试样,加适量水,待可溶物全部溶解,过滤,并洗涤沉淀,将洗涤液与滤液一并转移至500mL容量瓶中,定容、摇匀。
步骤Ⅱ:取20.00mL醋酸溶液(过量)于锥形瓶中,再加入20.00mL0.08000mol·L-1碘标准溶液,然后再向锥形瓶中加入10.00mL步骤Ⅰ所配的试样溶液,边加边振荡。充分反应后,硫元素完全转化为硫单质。
步骤Ⅲ:以淀粉为指示剂,用0.05000mol·L-1Na2S2O3标准溶液滴定至终点,发生反应:2S2O +I2=S4O
+I2=S4O +2I—。消耗Na2S2O3溶液20.00mL。
+2I—。消耗Na2S2O3溶液20.00mL。
计算试样中BaS的质量分数(写出计算过程)。____ (BaS的相对分子质量为169)
(2)制取高纯碳酸锰
BaS溶液和软锰矿经反应、过滤、酸溶、净化可制得的MnSO4溶液。
①MnSO4溶液和NH4HCO3固体混合后,极速反应生成MnCO3。反应方程式为2HCO +Mn2+=MnCO3↓+H2O+CO2↑。实际制取MnCO3时,一般选择使用氨水—NH4HCO3混合溶液代替NH4HCO3固体,这样改进的优点是
+Mn2+=MnCO3↓+H2O+CO2↑。实际制取MnCO3时,一般选择使用氨水—NH4HCO3混合溶液代替NH4HCO3固体,这样改进的优点是____ 。
②已知:6.5<pH<7.5时,碳酸锰产率较高。pH=8.1时,Mn2+开始形成Mn(OH)2沉淀。请设计以MnSO4溶液、氨水—NH4HCO3混合溶液为原料制备高纯碳酸锰的实验方案:____ 。(实验中须使用的试剂有:稀盐酸、BaCl2溶液、蒸馏水)
(1)制取BaS溶液
将重晶石与活性炭混合均匀,高温煅烧,冷却后得重晶石熟料。向重晶石熟料中加入热水,充分搅拌后过滤,得BaS溶液。
①SiO2的晶体类型是
②已知:室温下,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15。测得0.1mol·L-1BaS溶液pH≈13。溶液中OH—、S2—、HS—三种离子浓度由大到小的顺序是
③通过下列实验方法测定重晶石熟料中BaS的质量分数:
步骤Ⅰ:准确称取10.00g试样,加适量水,待可溶物全部溶解,过滤,并洗涤沉淀,将洗涤液与滤液一并转移至500mL容量瓶中,定容、摇匀。
步骤Ⅱ:取20.00mL醋酸溶液(过量)于锥形瓶中,再加入20.00mL0.08000mol·L-1碘标准溶液,然后再向锥形瓶中加入10.00mL步骤Ⅰ所配的试样溶液,边加边振荡。充分反应后,硫元素完全转化为硫单质。
步骤Ⅲ:以淀粉为指示剂,用0.05000mol·L-1Na2S2O3标准溶液滴定至终点,发生反应:2S2O
 +I2=S4O
+I2=S4O +2I—。消耗Na2S2O3溶液20.00mL。
+2I—。消耗Na2S2O3溶液20.00mL。计算试样中BaS的质量分数(写出计算过程)。
(2)制取高纯碳酸锰
BaS溶液和软锰矿经反应、过滤、酸溶、净化可制得的MnSO4溶液。
①MnSO4溶液和NH4HCO3固体混合后,极速反应生成MnCO3。反应方程式为2HCO
 +Mn2+=MnCO3↓+H2O+CO2↑。实际制取MnCO3时,一般选择使用氨水—NH4HCO3混合溶液代替NH4HCO3固体,这样改进的优点是
+Mn2+=MnCO3↓+H2O+CO2↑。实际制取MnCO3时,一般选择使用氨水—NH4HCO3混合溶液代替NH4HCO3固体,这样改进的优点是②已知:6.5<pH<7.5时,碳酸锰产率较高。pH=8.1时,Mn2+开始形成Mn(OH)2沉淀。请设计以MnSO4溶液、氨水—NH4HCO3混合溶液为原料制备高纯碳酸锰的实验方案:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】牙膏是常见的日用化学品。磨擦剂是牙膏的主体原料,在牙膏中最重要的作用就是去除牙垢,减轻牙结石。
I.完成下列问题。
(1)下表列出了牙膏中常见的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
(2)根据用途推测 在水中的溶解性:
在水中的溶解性:_______ (填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂氢氧化镁可以用菱镁矿(主要成分为 、
、 、
、 、
、 )来制备,按要求回答下列问题。
)来制备,按要求回答下列问题。_______ (填字母)。
A.菱镁矿 B. C.
C. D.
D. E.硫酸钙 F.氨
E.硫酸钙 F.氨
②方案中可循环利用的物质有_______ (填化学式)。
II.某牙膏摩擦剂的成分为 ,为测定其中
,为测定其中 的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):
的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):
①配制 稀盐酸和
稀盐酸和 NaOH溶液;
NaOH溶液;
②称取0.60g该牙膏,溶于水并稀释至20.00mL;
③用 NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
④加入25.00mL 稀盐酸;
稀盐酸;
(4)正确的操作顺序为①_______ (填标号)。
(5)该测定实验共进行了4次,实验室现有50mL、100mL、250mL、500mL4种规格的容量瓶,则配制盐酸应选用的容量瓶规格为_______ 。
(6)某同学4次测定所消耗NaOH溶液的体积如下:
则该牙膏中碳酸钙的质量分数约为_______ (保留三位有效数字)%。
I.完成下列问题。
(1)下表列出了牙膏中常见的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
| 摩擦剂成分 | 氢氧化镁 | 碳酸钙 | 二氧化硅 |
| 物质类别 | ① | ② |
 在水中的溶解性:
在水中的溶解性:(3)牙膏中的摩擦剂氢氧化镁可以用菱镁矿(主要成分为
 、
、 、
、 、
、 )来制备,按要求回答下列问题。
)来制备,按要求回答下列问题。
A.菱镁矿 B.
 C.
C. D.
D. E.硫酸钙 F.氨
E.硫酸钙 F.氨②方案中可循环利用的物质有
II.某牙膏摩擦剂的成分为
 ,为测定其中
,为测定其中 的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):
的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):①配制
 稀盐酸和
稀盐酸和 NaOH溶液;
NaOH溶液;②称取0.60g该牙膏,溶于水并稀释至20.00mL;
③用
 NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;④加入25.00mL
 稀盐酸;
稀盐酸;(4)正确的操作顺序为①
(5)该测定实验共进行了4次,实验室现有50mL、100mL、250mL、500mL4种规格的容量瓶,则配制盐酸应选用的容量瓶规格为
(6)某同学4次测定所消耗NaOH溶液的体积如下:
| 实验标号 | 1 | 2 | 3 | 4 |
| V(NaOH)/mL | 10.10 | 9.90 | 10.20 | 9.80 |
您最近一年使用:0次



