以氮化镓(GaN)、碳化硅、金刚石等为代表的第三代半导体材料具有高发光效率、抗腐蚀、化学稳定性好、高强度等特性,是目前最先进的半导体材料。完成下列填空:
(1)组成上述三种半导体材料的各种元素中,原子半径最小的元素在周期表中的位置是_______ 。原子序数最小的元素原子的核外电子排布式是___________ 。
(2)镓元素的相对原子质量为69.72,自然界中的镓共有两种稳定的同位素,其中69Ga的原子个数百分含量为60.1%,则另一种镓的同位素可表示为______ 。
(3)镓、铝为同族元素,性质相似。下表是两种两性氢氧化物的电离常数。
①写出氢氧化镓的电离方程式:______________ 。
②将一块镓铝合金完全溶于烧碱溶液,再往反应后的溶液中缓缓通入CO2,最先析出的氢氧化物是___________ 。
(4)碳化硅单晶是目前技术最成熟的第三代半导体材料。下列能说明碳的非金属性强于硅的反应(或反应组)是_____ (选填编号)
a.SiO32- + 2CO2 + 2H2O → H2SiO3 + 2HCO3—
b.SiO2 + 2C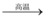 Si + 2CO↑
Si + 2CO↑
c.SiH4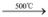 Si + 2H2;CH4
Si + 2H2;CH4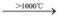 C + 2H2
C + 2H2
d.Si + O2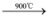 SiO2;C + O2
SiO2;C + O2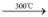 CO2
CO2
(1)组成上述三种半导体材料的各种元素中,原子半径最小的元素在周期表中的位置是
(2)镓元素的相对原子质量为69.72,自然界中的镓共有两种稳定的同位素,其中69Ga的原子个数百分含量为60.1%,则另一种镓的同位素可表示为
(3)镓、铝为同族元素,性质相似。下表是两种两性氢氧化物的电离常数。
| 两性氢氧化物 | Al(OH)3 | Ga(OH)3 |
| 酸式电离常数Kia | 2×10-11 | 1×10-7 |
| 碱式电离常数Kib | 1.3×10-33 | 1.4×10-34 |
①写出氢氧化镓的电离方程式:
②将一块镓铝合金完全溶于烧碱溶液,再往反应后的溶液中缓缓通入CO2,最先析出的氢氧化物是
(4)碳化硅单晶是目前技术最成熟的第三代半导体材料。下列能说明碳的非金属性强于硅的反应(或反应组)是
a.SiO32- + 2CO2 + 2H2O → H2SiO3 + 2HCO3—
b.SiO2 + 2C
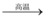 Si + 2CO↑
Si + 2CO↑c.SiH4
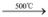 Si + 2H2;CH4
Si + 2H2;CH4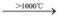 C + 2H2
C + 2H2d.Si + O2
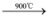 SiO2;C + O2
SiO2;C + O2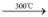 CO2
CO2
2013·上海·零模 查看更多[1]
(已下线)上海市八校2013届高三下学期联合调研考试化学试题
更新时间:2020-03-29 11:05:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
I.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨。
(1)以上物质中属于电解质的是________ (填序号,下同);属于非电解质的是_______ 。
(2)以上物质属于纯净物且能导电的是________ 。
II.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:

(3)加水的烧杯为________ 。
(4)向烧杯A滴入Ba(OH)2溶液,溶液导电性________ 。
(5)H3PO4是三元酸,能生成NaH2PO4、Na2HPO4两种酸式盐和Na3PO4一种正盐。磷还有一种含氧酸叫亚磷酸(H3PO3)。已知:H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。那么Na2HPO3为________ (填“正盐”或“酸式盐”);写出H3PO3与少量NaOH溶液反应的离子方程式________ 。
I.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨。
(1)以上物质中属于电解质的是
(2)以上物质属于纯净物且能导电的是
II.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:

(3)加水的烧杯为
(4)向烧杯A滴入Ba(OH)2溶液,溶液导电性
| A.变强 | B.变弱 | C.先变弱后变强 | D.先变强后变弱 |
(5)H3PO4是三元酸,能生成NaH2PO4、Na2HPO4两种酸式盐和Na3PO4一种正盐。磷还有一种含氧酸叫亚磷酸(H3PO3)。已知:H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。那么Na2HPO3为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空
(1)写出下列物质在水溶液中的电离方程式: NaHSO4_______ ; (NH4)2CO3_______ 。
(2)现有以下物质:①NaCl溶液 ②干冰 ③液态HCl ④铜 ⑤BaSO4固体 ⑥蔗糖 ⑦H2O ⑧NaOH固体 ⑨盐酸 ⑩NH3,其中能够导电的是_______ (填序号,下同);属于强电解质的是_______ ;属于非电解质的是_______ 。
(3)书写下列反应的离子方程式:
①大理石和稀盐酸反应:_______ ;
②Fe与CuSO4溶液反应:_______ ;
③Na2O2与H2O的反应:_______ 。
(4)用双线桥法标出下列方程式的电子转移情况________ 3NO2+H2O= 2HNO3+NO。
(5)用单线桥法标出下列方程式的电子转移情况______ Cl2+2NaBr= 2NaCl+Br2
(1)写出下列物质在水溶液中的电离方程式: NaHSO4
(2)现有以下物质:①NaCl溶液 ②干冰 ③液态HCl ④铜 ⑤BaSO4固体 ⑥蔗糖 ⑦H2O ⑧NaOH固体 ⑨盐酸 ⑩NH3,其中能够导电的是
(3)书写下列反应的离子方程式:
①大理石和稀盐酸反应:
②Fe与CuSO4溶液反应:
③Na2O2与H2O的反应:
(4)用双线桥法标出下列方程式的电子转移情况
(5)用单线桥法标出下列方程式的电子转移情况
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列10种物质:①铁② ③
③ 溶液④浓盐酸⑤氨气⑥
溶液④浓盐酸⑤氨气⑥ 固体⑦熔融的
固体⑦熔融的 ⑧
⑧ 固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
(1)上述物质中能导电的有___________ (填序号,下同);属于电解质的有___________ 。
(2) 不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产
不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产 ,同时得到两种副产品
,同时得到两种副产品 和
和 ,写出电解饱和食盐水的离子方程式:
,写出电解饱和食盐水的离子方程式:___________ 。
(3) 在熔融时的电离方程式为:
在熔融时的电离方程式为:___________ 。将 溶液逐滴加入
溶液逐滴加入 溶液中至溶液呈中性,反应的离子方程式为
溶液中至溶液呈中性,反应的离子方程式为___________ 。
(4) 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为: ,
,
①请用“双线桥”表示上述反应电子转移的方向和数目___________ 。
②浓盐酸在反应中显示出来的性质是___________ 。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(5) 是三元弱酸,磷还有一种含氧酸叫亚磷酸
是三元弱酸,磷还有一种含氧酸叫亚磷酸 ,它是一种二元弱酸,则
,它是一种二元弱酸,则 为
为________ (填“正盐”或“酸式盐”),写出 与足量
与足量 溶液反应的化学方程式
溶液反应的化学方程式________ 。
 ③
③ 溶液④浓盐酸⑤氨气⑥
溶液④浓盐酸⑤氨气⑥ 固体⑦熔融的
固体⑦熔融的 ⑧
⑧ 固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:(1)上述物质中能导电的有
(2)
 不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产
不但是日常生活中的调味品,也是一种重要的工业原料;工业上常采用电解饱和食盐水的方法生产 ,同时得到两种副产品
,同时得到两种副产品 和
和 ,写出电解饱和食盐水的离子方程式:
,写出电解饱和食盐水的离子方程式:(3)
 在熔融时的电离方程式为:
在熔融时的电离方程式为: 溶液逐滴加入
溶液逐滴加入 溶液中至溶液呈中性,反应的离子方程式为
溶液中至溶液呈中性,反应的离子方程式为(4)
 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为: ,
,①请用“双线桥”表示上述反应电子转移的方向和数目
②浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(5)
 是三元弱酸,磷还有一种含氧酸叫亚磷酸
是三元弱酸,磷还有一种含氧酸叫亚磷酸 ,它是一种二元弱酸,则
,它是一种二元弱酸,则 为
为 与足量
与足量 溶液反应的化学方程式
溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】核外电子排布与元素周期系的基本结构
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有_______ 种元素。其余各周期总是从ns能级开始,以np结束,而从ns能级开始以np结束递增的核电荷数(或电子数)就_______ 每个周期里的元素数。
②周期、能级组、元素种类的对应关系
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有
②周期、能级组、元素种类的对应关系
| 周期 | 对应能级组 | 对应能级组最多所能容纳的电子数 | 周期中所含元素种类 |
| 1 | 1s | 2 | 2 |
| 2 | 8 | ||
| 3 | 3s、3p | 8 | 8 |
| 4 | 18 | ||
| 5 | 5s、4d、5p | 18 | 18 |
| 6 | 32 | ||
| 7 | 7s、5f、6d、7p | 32 | 32 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫是人类认识最早的元素之一,含硫物质在现代生产和生活中发挥着重要作用。
(l)我国化学家姜雪峰因其在绿色有机硫化学领域的杰出贡献被遴选为“全球青年化学家元素周期表硫元素代表”。
①硫元素在元素周期表中的位置是____ 。
②乙硫醇(CH3CH2SH)是一种含硫有机物,其分子中S-H的极性小于CH3CH2OH分子中O-H的极性,请从原子结构角度解释其原因:____ 。
(2)自然界的硫循环过程如下图所示。
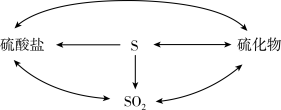
①上图所涉及的含硫物质中,能使品红溶液褪色的是____ 。
②降解石油(主要成分为CxHy)的过程中,在细菌催化作用下,石油与硫酸盐反应转化为碳酸氢盐,硫酸盐做____ (填“氧化剂”或“还原剂”)。
③煤炭中的硫化物主要为FeS2(S为-1价)。在潮湿的环境中,FeS2可在氧化亚铁硫杆菌(T.f)的作用下被空气氧化为Fe2(SO4)3,该反应的化学方程式为____ 。
(l)我国化学家姜雪峰因其在绿色有机硫化学领域的杰出贡献被遴选为“全球青年化学家元素周期表硫元素代表”。
①硫元素在元素周期表中的位置是
②乙硫醇(CH3CH2SH)是一种含硫有机物,其分子中S-H的极性小于CH3CH2OH分子中O-H的极性,请从原子结构角度解释其原因:
(2)自然界的硫循环过程如下图所示。

①上图所涉及的含硫物质中,能使品红溶液褪色的是
②降解石油(主要成分为CxHy)的过程中,在细菌催化作用下,石油与硫酸盐反应转化为碳酸氢盐,硫酸盐做
③煤炭中的硫化物主要为FeS2(S为-1价)。在潮湿的环境中,FeS2可在氧化亚铁硫杆菌(T.f)的作用下被空气氧化为Fe2(SO4)3,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图是元素周期表的一部分。回答下列问题:
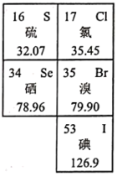
(1)溴被称为海洋元素。
①溴在元素周期表中位于第___________ 周期___________ 族。
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
③能够证明溴单质的氧化性强于碘单质的离子方程式是___________ 。
(2)硒是人体必需的微量元素。
①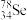 与
与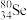 互称为
互称为___________ 。
②元素的气态氢化物的化学式为___________ 。
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:___________ 。
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是___________ (填字母)。
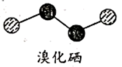
a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72

(1)溴被称为海洋元素。
①溴在元素周期表中位于第
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
③能够证明溴单质的氧化性强于碘单质的离子方程式是
(2)硒是人体必需的微量元素。
①
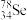 与
与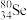 互称为
互称为②元素的气态氢化物的化学式为
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是

a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。完成下列填空:
(1)写出一个包含上述七种物质的氧化还原反应方程式,配平并标出电子转移方向和数目:___________________________ 。
(2)上述反应中,氧化剂是_____________ ,每转移1 mol电子,生成Cl2_____ L(标准状况)。
(3)在反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。写出该实验中涉及反应的离子反应方程式:_________________ 。
(4)根据以上实验,写出两个反应中氧化剂、氧化产物的氧化性强弱顺序__________ 。
(5)上述氧化还原反应体系中,属于第三周期元素的简单离子半径由大到小的顺序为________
(6)氯原子的最外层电子的轨道式为___________ ,氯原子核外有_______ 不同运动状态的电子。
(1)写出一个包含上述七种物质的氧化还原反应方程式,配平并标出电子转移方向和数目:
(2)上述反应中,氧化剂是
(3)在反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。写出该实验中涉及反应的离子反应方程式:
(4)根据以上实验,写出两个反应中氧化剂、氧化产物的氧化性强弱顺序
(5)上述氧化还原反应体系中,属于第三周期元素的简单离子半径由大到小的顺序为
(6)氯原子的最外层电子的轨道式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是________ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):________ >________ ;比较g、h的最高价氧化物对应水化物的酸性强弱________ >________ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_________________________ 。
(4)e的单质在足量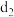 中燃烧的化学方程式:
中燃烧的化学方程式:_________________________ 。
(5)上述元素可组成盐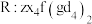 。向盛有
。向盛有 溶液的烧杯中滴加
溶液的烧杯中滴加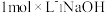 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化示意图如下:
溶液体积的变化示意图如下:
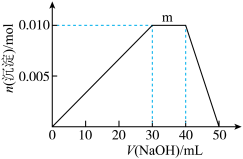
①R溶液的电离方程式____________________________ 。
②写出m点反应的离子方程式:____________________ 。
③若在R溶液中改加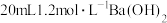 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为________  。
。

根据判断出的元素回答问题:
(1)f在周期表中的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同):
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:
(4)e的单质在足量
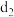 中燃烧的化学方程式:
中燃烧的化学方程式:(5)上述元素可组成盐
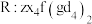 。向盛有
。向盛有 溶液的烧杯中滴加
溶液的烧杯中滴加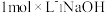 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化示意图如下:
溶液体积的变化示意图如下:
①R溶液的电离方程式
②写出m点反应的离子方程式:
③若在R溶液中改加
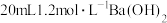 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为 。
。
您最近一年使用:0次

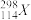 ,请根据原子结构理论和元素周期律预测:
,请根据原子结构理论和元素周期律预测:

