双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法。双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_________________________ ,双氧水的质量分数为27.5%(密度为1.10 g·cm-3),其浓度为________ 。
2020高三·山东·专题练习 查看更多[1]
(已下线)专题1.2 物质的量浓度及其计算 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》
更新时间:2020-04-05 09:01:35
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】一瓶久置的Na2SO3(杂质只有Na2SO4),为了测定其纯度,取样品5.0 g配成100 mL溶液,取其中25.00 mL于锥形瓶中,用0.10 mol•L-1酸性KMnO4溶液进行滴定,到终点时消耗KMnO4溶液20.00 mL,求此样品的纯度。_______________
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,其离子方程式是_______ 。
(2)CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为____________ 。
(3)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等,除去100 L锅炉水中 含氧气8 g/L的溶解氧,需要肼的质量为
含氧气8 g/L的溶解氧,需要肼的质量为__________ 。
(2)CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为
(3)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等,除去100 L锅炉水中
 含氧气8 g/L的溶解氧,需要肼的质量为
含氧气8 g/L的溶解氧,需要肼的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】一种由CuO和KHC2O4溶液反应得到的蓝色结晶[KaCub(C2O4)c·dH2O]。为测定其组成,进行了如下实验:
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:___ 。
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O
(1)3.5400g该样品中含n( )=
)=___ mol。
(2)3.5400g该样品中含n(Cu2+)=___ mol。
(3)通过计算确定该蓝色晶体的化学式(计算过程)___ 。
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O(1)3.5400g该样品中含n(
 )=
)=(2)3.5400g该样品中含n(Cu2+)=
(3)通过计算确定该蓝色晶体的化学式(计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】市售铁强化盐中铁含量测定。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数为___________ (列出式子即可)。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O
 =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为
(2)样品中铁元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】由碳酸铵 和硝酸铵
和硝酸铵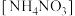 组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:
组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:
①第一份溶于水配成100mL溶液,再加入足量的 溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g
溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g
②第二份与足量浓NaOH溶液混合后加热,完全反应后生成标准状况下的气体2.8L
根据上述数据计算:
(1)每份固体中含碳酸铵的物质的量为________ mol。
(2)第一份所配溶液中硝酸铵的物质的量浓度为________  。
。
(3)原固体混合物中含氮元素的质量分数为________ 。(计算结果保留三位有效数字)
 和硝酸铵
和硝酸铵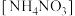 组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:
组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:①第一份溶于水配成100mL溶液,再加入足量的
 溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g
溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g②第二份与足量浓NaOH溶液混合后加热,完全反应后生成标准状况下的气体2.8L
根据上述数据计算:
(1)每份固体中含碳酸铵的物质的量为
(2)第一份所配溶液中硝酸铵的物质的量浓度为
 。
。(3)原固体混合物中含氮元素的质量分数为
您最近一年使用:0次



