已知 NH3和 Cl2在常温下可快速反应生成氮气:2 NH3 + 3Cl2 → N2 + 6HCl。当 Cl2和 NH3 比例不同时,产物有差异。
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 Cl2 和 NH3 的最佳比例为____________ 。该反应可用于检验化工生产中氯气是否泄漏。如氯气有少量泄漏,用氨气检验时有明显现象,此过程中发生反应的Cl2和NH3的体积比范围为___________ 。
(2)体积为1.12 L,质量为3.335 g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672 L(其中Cl2体积分数为50%)(气体体积均为标准状况下测定)。则原混合气体中N2的体积为_____________ mL。
(3)根据第(2)题数据,计算被氧化的NH3的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
(4)有Cl2和N2的混合气体,其中N2的体积分数为x,将1L该混合气体与1L氨气混合,讨论x取不同范围的数值时,所得气体体积y与x的关系式(所有气体体积均在相同状况下测定)。______________
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 Cl2 和 NH3 的最佳比例为
(2)体积为1.12 L,质量为3.335 g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672 L(其中Cl2体积分数为50%)(气体体积均为标准状况下测定)。则原混合气体中N2的体积为
(3)根据第(2)题数据,计算被氧化的NH3的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
| 学生编号 | 所列第一步算式 | 未知数X表示的意义 |
| 甲 | 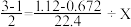 | |
| 乙 |  | |
(4)有Cl2和N2的混合气体,其中N2的体积分数为x,将1L该混合气体与1L氨气混合,讨论x取不同范围的数值时,所得气体体积y与x的关系式(所有气体体积均在相同状况下测定)。
2012·上海徐汇·二模 查看更多[1]
(已下线)上海市徐汇区2012届高三4月学习能力诊断化学试题
更新时间:2020-04-06 11:44:59
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】PCl3和PCl5能发生如下水解反应:PCl3+3H2O→H3PO3+3HCl;PCl5+4H2O→H3PO4+5HCl,现将一定量的PCl3和PCl5混合物溶于足量水中,在加热条件下缓缓通入0.020molO2,恰好将H3PO3氧化为H3PO4。往反应后的溶液中加入15.725gCa(OH)2,充分反应后磷元素全部转化为Ca3(PO4)2沉淀,过滤后得到2.5L滤液,测得pH为12。计算:
(1)Ca3(PO4)2(已知式量310)沉淀的质量____________ ;
(2)滤液中溶质的物质的量浓度__________________ 。
(1)Ca3(PO4)2(已知式量310)沉淀的质量
(2)滤液中溶质的物质的量浓度
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】把1.92gCu投入到一定量的浓硝酸中,充分反应,产生1.12L气体(标准状况)。计算参加反应的硝酸的物质的量。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】32g铜投入一定浓度的硝酸溶液中,铜完全溶解,共收集到NO和NO2的混合气体8.96L气体(标准状况)。
(1)计算产生NO和NO2的体积(标准状况)分别为多少L?(请写出计算过程)___________
(2)将盛有此混合气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为___________ L。
(3)向100mL0.8mol•L-1硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反应后,放出标准状况下的气体224mL,且测得溶液中铁只以Fe2+形式存在,为使Fe2+完全沉淀,可向反应后的溶液中加入0.1mol•L-1的NaOH___________ mL
(1)计算产生NO和NO2的体积(标准状况)分别为多少L?(请写出计算过程)
(2)将盛有此混合气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为
(3)向100mL0.8mol•L-1硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反应后,放出标准状况下的气体224mL,且测得溶液中铁只以Fe2+形式存在,为使Fe2+完全沉淀,可向反应后的溶液中加入0.1mol•L-1的NaOH
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】取一定质量的NaBr、NaI的混合物平均分成四等份,分别加水配成溶液并编号甲、乙、丙、丁。再分别向各溶液中通入一定体积的氯气。将反应后所得溶液蒸干、灼烧的固体质量列表如下:
(1)在标准状况下,Cl2的体积V为___________ mL。
(2)原混合物中NaBr的物质的量为__________ mol。
| 编号 | 甲 | 乙 | 丙 | 丁 |
| 固体成分 | NaCl、NaBr、NaI | NaCl、NaBr、NaI | NaCl、NaBr | NaCl |
| Cl2体积/mL | V | 2V | 3V | 4V |
| 固体质量/g | 77.3 | 59.0 | 45.4 | 40.95 |
(1)在标准状况下,Cl2的体积V为
(2)原混合物中NaBr的物质的量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】氨气、氯气和化合物A是常见化合物,在工农业生产中有重要的应用。根据题意回答下列问题:
(1)化合物A的相对分子质量为60(含四种元素),A在一定条件下水解有氨气产生,A分子中碳元素、氧元素和氢元素的质量百分含量分别是20%、26.674%和6.7%。计算确定A的结构简式为_______ 。说出A在一种用途___________ 。
(2)NH3和Cl2在常温下可快速反应生成氮气和氯化铵:8NH3+3Cl2 →N2+6NH4Cl。该反应可用于检验化工生产中氯气是否泄漏。若要在实验室配制体积比为336:1的氨水1kg,计算此氨水的物质的量的浓度为多少________ ?(已知氨水密度为0.92g·cm-3、水的密度为0.899g·cm-3)
(3)常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体总物质的量保持不变。求:
① 反应前氯气和氨气的物质的量之比为多少________ ?
② 反应后生成的氧化产物的质量为多少________ ?
(4)已知氨气和氯气混合可发生下列反应: 2NH3+3Cl2 → 6HCl+N2,NH3+HCl → NH4Cl 现有Cl2和NH3共aL,混合后充分反应,气体体积变为bL,问有多少升的NH3被氧化________ ?(气体前后气体体积均在同温同压下)。
(1)化合物A的相对分子质量为60(含四种元素),A在一定条件下水解有氨气产生,A分子中碳元素、氧元素和氢元素的质量百分含量分别是20%、26.674%和6.7%。计算确定A的结构简式为
(2)NH3和Cl2在常温下可快速反应生成氮气和氯化铵:8NH3+3Cl2 →N2+6NH4Cl。该反应可用于检验化工生产中氯气是否泄漏。若要在实验室配制体积比为336:1的氨水1kg,计算此氨水的物质的量的浓度为多少
(3)常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体总物质的量保持不变。求:
① 反应前氯气和氨气的物质的量之比为多少
② 反应后生成的氧化产物的质量为多少
(4)已知氨气和氯气混合可发生下列反应: 2NH3+3Cl2 → 6HCl+N2,NH3+HCl → NH4Cl 现有Cl2和NH3共aL,混合后充分反应,气体体积变为bL,问有多少升的NH3被氧化
您最近一年使用:0次
【推荐2】已知:4NH3+5O2  4NO+6H2O 4NO+3O2+2H2O
4NO+6H2O 4NO+3O2+2H2O  4HNO3。设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列计算:
4HNO3。设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列计算:
(1)使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为_______ (保留2位小数)。
(2)工业上用Mg(NO3)2制取浓HNO3的脱水剂(以下数据均为质量百分比浓度)。65%HNO3(质量为M1)中加72%Mg(NO3)2溶液(质量为M2)后蒸馏。分别得到97.5%HNO3和60%Mg(NO3)2溶液(不含HNO3)。若蒸馏过程中HNO3、Mg(NO3)2、H2O均无损耗,求蒸馏前的投料比M1/M2的值是_______ ;
(3)铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2, 反应中固体完全溶解,两种酸均恰好完全反应。若固体混合物的总质量为480 g,其中铜屑的质量分数为0.4,则混酸中HNO3与H2SO4的物质的量之比为________ ;480g固体混合物与一定量混酸微热后,充分反应,冷却恰好只得到CuSO4·5H2O,原混酸中H2SO4的质量分数为_______ 。
(4)①20.0moL的NH3用空气氧化,产生混合物的组成为:NO18.0mol、O212.0 mol、N2150.0 mol和一定量的硝酸,以及其它成分(高温下NO和O2不反应)。计算HNO3的物质的量为______ ;
②20.0moL 的NH3和一定量空气充分反应后,再转化为HNO3,设HNO3的物质的量n(A)和空气的物质的量n(B),写出当125≤n(B) ≤ 200时,n(A)和n(B)的关系式_______ 。
 4NO+6H2O 4NO+3O2+2H2O
4NO+6H2O 4NO+3O2+2H2O  4HNO3。设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列计算:
4HNO3。设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列计算:(1)使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为
(2)工业上用Mg(NO3)2制取浓HNO3的脱水剂(以下数据均为质量百分比浓度)。65%HNO3(质量为M1)中加72%Mg(NO3)2溶液(质量为M2)后蒸馏。分别得到97.5%HNO3和60%Mg(NO3)2溶液(不含HNO3)。若蒸馏过程中HNO3、Mg(NO3)2、H2O均无损耗,求蒸馏前的投料比M1/M2的值是
(3)铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2, 反应中固体完全溶解,两种酸均恰好完全反应。若固体混合物的总质量为480 g,其中铜屑的质量分数为0.4,则混酸中HNO3与H2SO4的物质的量之比为
(4)①20.0moL的NH3用空气氧化,产生混合物的组成为:NO18.0mol、O212.0 mol、N2150.0 mol和一定量的硝酸,以及其它成分(高温下NO和O2不反应)。计算HNO3的物质的量为
②20.0moL 的NH3和一定量空气充分反应后,再转化为HNO3,设HNO3的物质的量n(A)和空气的物质的量n(B),写出当125≤n(B) ≤ 200时,n(A)和n(B)的关系式
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】氮的氧化物既是可导致酸雨的物质,也是造成空气污染的重要物质,加大对氮的氧化物的治理是环境保护重要举措。
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:_____________________________ ,该反应中氧化剂是_________ ,还原剂是________________________________________ 。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成对大气无污染的气体,该反应的化学方程式为___________________________________ 。
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
现有VL某NaOH溶液能完全吸收nmol NO2和mmol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为_________ mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=_________ 。
③用含n和m的代数式表示所得溶液中NO3-和NO2-浓度的比值c(NO3-)∶c(NO2-)=_________ 。
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成对大气无污染的气体,该反应的化学方程式为
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
现有VL某NaOH溶液能完全吸收nmol NO2和mmol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=
③用含n和m的代数式表示所得溶液中NO3-和NO2-浓度的比值c(NO3-)∶c(NO2-)=
您最近一年使用:0次



