在a、b两支试管中,分别装上质量相等形状相同的一颗锌粒,然后向两支试管中:
(1)分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。则a、b两支试管中的现象:相同点是_______ ;不同点是_______ ,反应完毕后生成气体的总体积是a_______ b。
(2)分别加入相同pH、相同体积的稀盐酸和稀醋酸时,两支试管中的反应速率在反应刚开始时是a_______ b(填“大于”、“等于”或“小于”下同),当两种酸都反应完毕后生成气体的体积是a_______ b
(1)分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。则a、b两支试管中的现象:相同点是
(2)分别加入相同pH、相同体积的稀盐酸和稀醋酸时,两支试管中的反应速率在反应刚开始时是a
12-13高二上·云南红河·期末 查看更多[1]
(已下线)2011-2012学年云南蒙自高中高二上学期期末考试化学试卷
更新时间:2016-12-08 18:55:25
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】接触法制硫酸的三个阶段:煅烧、氧化、吸收。煅烧黄铁矿的化学方程式为:
4FeS2 + 11O2 → 2Fe2O3 + 8SO2。
完成下列填空:
(1)煅烧黄铁矿在________ (填设备名称)中进行,此反应中被氧化的元素是___________ 。
(2)SO2的催化氧化:2SO2(g)+O2(g) 2SO3(g),该反应的平衡常数表达式为K=
2SO3(g),该反应的平衡常数表达式为K= ______ ;反应达到平衡,及时分离出SO3,则平衡向_________ 方向移动(选填“正反应”“逆反应”)。其他条件不变,降低温度平衡向正反应方向移动,则正反应为__________ 反应(选填“吸热”“放热”)。
(3)下图为二氧化硫与氧气反应的速率(ν)与时间(t)的关系,判断在t1时刻曲线发生变化的原因是______ (选填编号)。
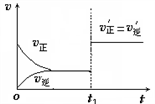
a. 增大O2的浓度
b. 扩大容器体积
c. 加入催化剂
d. 升高温度
改变条件后,平衡混合物中SO3的百分含量_______ (选填“增大”“减小”“不变”)。
(4)SO3的吸收:SO3 + H2O → H2SO4 。假定制备硫酸的整个过程中S元素共损失10%,则含1000 kg FeS2的黄铁矿可以制得98%的浓硫酸_____________ kg。
4FeS2 + 11O2 → 2Fe2O3 + 8SO2。
完成下列填空:
(1)煅烧黄铁矿在
(2)SO2的催化氧化:2SO2(g)+O2(g)
 2SO3(g),该反应的平衡常数表达式为K=
2SO3(g),该反应的平衡常数表达式为K= (3)下图为二氧化硫与氧气反应的速率(ν)与时间(t)的关系,判断在t1时刻曲线发生变化的原因是

a. 增大O2的浓度
b. 扩大容器体积
c. 加入催化剂
d. 升高温度
改变条件后,平衡混合物中SO3的百分含量
(4)SO3的吸收:SO3 + H2O → H2SO4 。假定制备硫酸的整个过程中S元素共损失10%,则含1000 kg FeS2的黄铁矿可以制得98%的浓硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】纳米级Cu2O由于具有优良的催化性能而受到关注,表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是______________ 。
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =__________ kJ·mol-1。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为________________ 。
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为____________ 。
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O 2H2(g)+O2(g) ΔH>0
2H2(g)+O2(g) ΔH>0
水蒸气的浓度随时间t变化如下表所示。
下列叙述正确的是________ (填字母代号)。
A.实验温度: T12
B.实验①前20 min的平均反应速率v(O2)=7×10-5 mol·L-1 min-1
C.实验②比实验①所用的催化剂效率低
D.T2条件下该反应的化学平衡常数为6.17×10-5mol/L
(6)25℃时,向50mL 0.018mol/L的AgNO3溶液中加入50mL 0.02mol/L盐酸,生成沉淀,若已知Kap(AgCl)=1.8×10-10,则此时溶液中的c(Ag+)=______________ 。(体积变化忽略不计)若再向沉淀生成后的溶液中加入100mL 0.01mol/L盐酸,是否继续产生沉淀_______ (填“是”或“否”)。
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,反应为2Cu+H2O Cu2O+H2↑ Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为

(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O
 2H2(g)+O2(g) ΔH>0
2H2(g)+O2(g) ΔH>0水蒸气的浓度随时间t变化如下表所示。
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是
A.实验温度: T12
B.实验①前20 min的平均反应速率v(O2)=7×10-5 mol·L-1 min-1
C.实验②比实验①所用的催化剂效率低
D.T2条件下该反应的化学平衡常数为6.17×10-5mol/L
(6)25℃时,向50mL 0.018mol/L的AgNO3溶液中加入50mL 0.02mol/L盐酸,生成沉淀,若已知Kap(AgCl)=1.8×10-10,则此时溶液中的c(Ag+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碘及其化合物在生活中应用广泛,含有碘离子的溶液需回收处理。
(1)“硫碘循环”法是分解水制备氢气的研究热点,涉及下列三个反应:
反应Ⅰ:SO2(g)+I2(aq)+2H2O(l)═2HI(aq)+H2SO4(aq)△H1
反应Ⅱ:HI(aq)═ H2(g)+
H2(g)+ I2(aq)△H2
I2(aq)△H2
反应Ⅲ:2H2SO4(aq)═2SO2(g)+O2(g)+2H2O(l)
①反应:SO2(g)+2H2O(l)═H2SO4(aq)+H2(g)的△H═______ (用△H1、△H2表示);
②分析上述反应,下列判断正确的是______ ;
A.反应Ⅲ易在常温下进行
B.反应I中SO2还原性比HI强
C.循环过程中需补充H2O
D.循环过程中产生1molO2同时产生1molH2
③反应I发生时,溶液中存在如下平衡:I2(aq)+I-(aq)⇌I3-(aq),其反应速率极快且平衡常数大。现将1mol SO2.缓缓通入含1molI2的水溶液中至恰好完全反应。溶液中I3-的物质的量n(I3-)随反应时间(t)的变化曲线如图所示。开始阶段n(I3-)逐渐增大的原因是:______ ;

(2)用海带提取碘时,需用氯气将碘离子氧化成单质。酸性条件下,若氯气过量还能将碘单质进一步氧化成碘酸根离子(IO3-),写出氯气与碘单质反应的离子方程式:______ ;
(3)氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为I-(aq)+AgCl(s)⇌AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)═______ [用c(Cl-)、Ksp(AgCl)和Ksp(AgI)表示].该方法去除碘离子的原理是______ 。
(1)“硫碘循环”法是分解水制备氢气的研究热点,涉及下列三个反应:
反应Ⅰ:SO2(g)+I2(aq)+2H2O(l)═2HI(aq)+H2SO4(aq)△H1
反应Ⅱ:HI(aq)═
 H2(g)+
H2(g)+ I2(aq)△H2
I2(aq)△H2反应Ⅲ:2H2SO4(aq)═2SO2(g)+O2(g)+2H2O(l)
①反应:SO2(g)+2H2O(l)═H2SO4(aq)+H2(g)的△H═
②分析上述反应,下列判断正确的是
A.反应Ⅲ易在常温下进行
B.反应I中SO2还原性比HI强
C.循环过程中需补充H2O
D.循环过程中产生1molO2同时产生1molH2
③反应I发生时,溶液中存在如下平衡:I2(aq)+I-(aq)⇌I3-(aq),其反应速率极快且平衡常数大。现将1mol SO2.缓缓通入含1molI2的水溶液中至恰好完全反应。溶液中I3-的物质的量n(I3-)随反应时间(t)的变化曲线如图所示。开始阶段n(I3-)逐渐增大的原因是:

(2)用海带提取碘时,需用氯气将碘离子氧化成单质。酸性条件下,若氯气过量还能将碘单质进一步氧化成碘酸根离子(IO3-),写出氯气与碘单质反应的离子方程式:
(3)氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为I-(aq)+AgCl(s)⇌AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)═
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】烟气(主要污染物SO2、NOx)是大气主要污染物,有效去除大气中SO2、NOx的是环境保护的重要课题。
(1)氨水法脱硫就是用足量的氨水将烟气中的SO2吸收,生成的盐再进一步氧化成硫酸铵。写出上述处理过程中发生反应的化学方程式______ 、______ 。
(2)用亚硫酸钠吸收法可实现SO2的循环使用,步骤如下:第一步,用亚硫酸钠溶液吸收SO2;第二步,加热吸收液,使之重新生成亚硫酸钠。写出上述处理过程中发生反应的化学方程式______ 、______ 。
(3)可以氨气还原法处理NOx,生成无污染的N2。写出氨气与NO2发生反应的化学方程式______ 。
(4)环保部门为测定某硫酸厂周围空气中SO2的体积分数,做了如下实验:取标准状况下的空气2.000L(含N2、O2、CO2、SO2等),缓慢通过足量溴水,在所得溶液中加入过量的BaCl2溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.466g。试回答:
①加入过量BaCl2溶液的目的是______ 。
②该空气样品中SO2的体积分数为______ 。
(1)氨水法脱硫就是用足量的氨水将烟气中的SO2吸收,生成的盐再进一步氧化成硫酸铵。写出上述处理过程中发生反应的化学方程式
(2)用亚硫酸钠吸收法可实现SO2的循环使用,步骤如下:第一步,用亚硫酸钠溶液吸收SO2;第二步,加热吸收液,使之重新生成亚硫酸钠。写出上述处理过程中发生反应的化学方程式
(3)可以氨气还原法处理NOx,生成无污染的N2。写出氨气与NO2发生反应的化学方程式
(4)环保部门为测定某硫酸厂周围空气中SO2的体积分数,做了如下实验:取标准状况下的空气2.000L(含N2、O2、CO2、SO2等),缓慢通过足量溴水,在所得溶液中加入过量的BaCl2溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.466g。试回答:
①加入过量BaCl2溶液的目的是
②该空气样品中SO2的体积分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】无论在办公室还是居室里,在漂亮的花瓶中插上一束美丽的鲜花,将会给紧张而又忙碌的工作、生活带来轻松和愉悦的心情。如果在花瓶中加入“鲜花保鲜剂”,就会延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后回答下列问题:
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是________ (填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林不含K+)________ mol·L-1(只要求写表达式,不需计算)。
(3)配制过程中,下列操作对配制结果没有影响的是________ (填字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有________ (填化学符号)。
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林不含K+)
(3)配制过程中,下列操作对配制结果没有影响的是
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】S4N4在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定S4N4的纯度。称取1.100 g S4N4样品,加入NaOH溶液,并加热,释放出的氨气用足量100 mL1 mol/L硼酸吸收[反应方程式为2NH3+4H3BO3=(NH4)2B2O7+5H2O,假定反应过程中溶液体积不变]。反应后的溶液以甲基红―亚甲蓝为指示剂,再用1 mol/L的盐酸[滴定反应方程式为(NH4)2B2O7+2HCl+5H2O=2NH4Cl+4 H3BO3]进行滴定,重复三次实验。实验数据记录如下表所示:
则制得的S4N4的纯度为___________ (保留4位有效数字)。
| 实验序号 | 初始读数(mL) | 最终读数(mL) |
| Ⅰ | 0.20 | 20.22 |
| Ⅱ | 0.40 | 24.85 |
| Ⅲ | 1.00 | 20.98 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在标准状况下,①6.72 L CH4气体;②3.01×1023个 HCl气体分子;③13.6 g H2S气体;④0.2 mol NH3,下列对这四种气体所含分子物质的量的关系从小到大的排列是(用上述数字序号表示)______ 。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要的仪器名称为(写出三种)______ 。
②该同学将所得精盐配成溶液,用于另一实验:实验中需要用60 mL 2 mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为______ ,该同学将精盐放在天平的右盘中称量好后,配制成溶液,则该溶液的浓度______ 2 mol·L-1(填“>”、“<”或“=”)。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要的仪器名称为(写出三种)
②该同学将所得精盐配成溶液,用于另一实验:实验中需要用60 mL 2 mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】三水乳酸亚铁晶体[(CH3CHOHCOO)2Fe•3H2O,Mr=288]是一种很好的补铁剂,易溶于水,吸收效果比无机铁好。可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是______ (填字母),原因是_______________________ 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是__________________ 。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是_____________________ 。
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是______________________________________ 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是_______________ 。
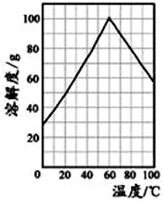
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液____________ ,得到FeSO4·7H2O晶体。
(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是____________________ 。经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol•L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)219.7mL。滴定反应为Ce4++Fe2+═Ce3++Fe3+,则产品中乳酸亚铁晶体的质量分数为__________ 。
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液

(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CaO2难溶于水,溶于酸生成过氧化氢,在医药上用作杀菌剂、防腐剂等。
Ⅰ.CaO2制备原理:Ca(OH)2(s)+H2O2(aq)=CaO2(s)+2H2O(l);ΔH<0
不同浓度的H2O2对反应生成CaO2产率的影响如下表:
(1)分析题给信息,解释H2O2浓度大于20%后CaO2产率反而减小的原因:___________ 。
Ⅱ.过氧化钙中常含有CaO杂质,实验室可按以下步骤测定CaO2含量。
步骤1:准确称取0.04~0.05g过氧化钙样品,置于250mL的锥形瓶中;
步骤2:分别加入30mL蒸馏水和2 mL盐酸(3mol∙L-1),振荡使之溶解;
步骤3:向锥形瓶中加入5mLKI溶液(100g·L-1);
步骤4:用硫代硫酸钠标准溶液滴定,至溶液呈浅黄色,然后________ ,用硫代硫酸钠标准溶液继续滴定,________ ,记录数据;
步骤5:平行测定3次,计算试样中CaO2的质量分数。滴定时发生的反应为2Na2S2O3+I2=Na2S4O6+2NaI。
(2)过氧化钙溶解时选用盐酸而不选用硫酸溶液的原因是___________ 。
(3)加入KI溶液后发生反应的离子方程式为____________ 。
(4)请补充完整实验步骤4中的内容:____________ ;____________ 。
Ⅰ.CaO2制备原理:Ca(OH)2(s)+H2O2(aq)=CaO2(s)+2H2O(l);ΔH<0
不同浓度的H2O2对反应生成CaO2产率的影响如下表:
| H2O2/% | 5 | 10 | 15 | 20 | 25 | 30 |
| CaO2/% | 62.40 | 63.10 | 63.20 | 64.54 | 62.42 | 60.40 |
(1)分析题给信息,解释H2O2浓度大于20%后CaO2产率反而减小的原因:
Ⅱ.过氧化钙中常含有CaO杂质,实验室可按以下步骤测定CaO2含量。
步骤1:准确称取0.04~0.05g过氧化钙样品,置于250mL的锥形瓶中;
步骤2:分别加入30mL蒸馏水和2 mL盐酸(3mol∙L-1),振荡使之溶解;
步骤3:向锥形瓶中加入5mLKI溶液(100g·L-1);
步骤4:用硫代硫酸钠标准溶液滴定,至溶液呈浅黄色,然后
步骤5:平行测定3次,计算试样中CaO2的质量分数。滴定时发生的反应为2Na2S2O3+I2=Na2S4O6+2NaI。
(2)过氧化钙溶解时选用盐酸而不选用硫酸溶液的原因是
(3)加入KI溶液后发生反应的离子方程式为
(4)请补充完整实验步骤4中的内容:
您最近一年使用:0次



