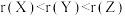如图是元素周期表的一部分,所列字母分别代表一种化学元素。下列说法正确的是( )
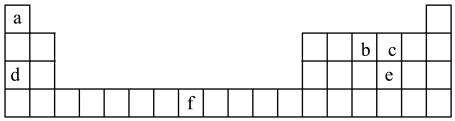

| A.b的第一电离能小于c的第一电离能 |
| B.d在c的常见单质中燃烧,产物中既含有离子键也含有共价键 |
| C.e与a组成的化合物沸点比水低,原因是水分子之间可形成氢键 |
| D.f元素的基态原子失去4s能级上的所有电子后所形成的离子最稳定 |
更新时间:2020-04-05 20:18:28
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素)。对比中学常见元素周期表,思考扇形元素周期表的填充规律,下列说法正确的是


| A.②⑧⑨对应简单离子的半径依次减小 |
| B.⑥的金属性比⑦的金属性弱 |
| C.元素⑩位于常见元素周期表第四周期VIII族 |
| D.①与③④⑤均可形成化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】元素在元素周期表中的分区说法正确的是
| A.s区的元素一定是主族元素 | B.d区元素一定是副族元素 |
| C.p区的元素一定是主族元素 | D.ds区元素一定是副族元素 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是| A.A、B、C三种元素的电负性:C>B>A |
| B.B、C、D、E四种元素的第一电离能:B>C>E>D |
C. 中阴离子的空间结构为三角锥形 中阴离子的空间结构为三角锥形 |
D.F的常见离子的核外电子排布图为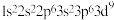 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.1mol乙酸分子(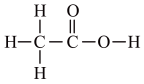 )中 )中 键的数目为8 键的数目为8 |
B.标准状况下,2.24L  溶于水,溶液中 溶于水,溶液中 、 、 和 和 的微粒数之和小于0.1 的微粒数之和小于0.1 |
C.电解精炼铜阳极质量减少6.4g时,转移电子数为0.2 |
D.31g基态P原子中含有的未成对电子数为3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
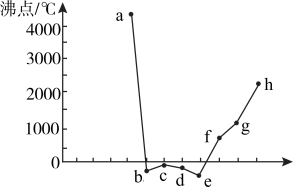
【推荐1】元素a-h为原子序数连续的八种短周期元素,它们的常见单质的沸点与原子序数的关系如图所示,其中d的单质呈淡黄绿色,下列说法正确的是

| A.d元素位于元素周期表第3周期VIIA族 |
| B.上述元素基态原子中e的第一电离能最大 |
| C.a与c形成的化合物均是极性键构成的极性分子 |
| D.f、g、h分别与c形成的化合物均属于离子化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,下列有关说法正确的是
| A.X的原子半径大于Y的原子半径 |
| B.X的电负性大于Y的电负性 |
| C.X的阴离子半径大于Y的阳离子半径 |
| D.X的第一电离能小于Y的第一电离能 |
您最近一年使用:0次
【推荐3】以下有关元素性质的说法不正确的是
| A.具有下列电子排布式的原子:①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,原子半径最大的是④ |
| B.具有下列价电子排布式的原子:①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,第一电离能最大的是③ |
| C.①Na、K、Rb ②N、P、S ③Na、P、Cl,元素的电负性随原子序数增大而增大的是③ |
| D.某主族元素气态基态离子的逐级电离能数据(单位:kJ·mol-1)分别为738、1451、7733、10540、13630、17995、21703……它与氯气反应时,生成的阳离子是X3+ |
您最近一年使用:0次

 轨道上有5个电子,Z与Y属于同一主族,X的气态氢化物水溶液呈碱性。下列说法正确的是
轨道上有5个电子,Z与Y属于同一主族,X的气态氢化物水溶液呈碱性。下列说法正确的是