根据已学知识,回答下列问题。
(1)已知下列元素基态原子的电子排布式,判断它们所在的周期和族。
①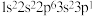
___________________ ;
②
___________________ ;
③
___________________ ;
④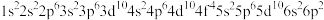
___________________ 。
(2)已知下列元素在周期表中的位置,写出它们的元素符号和价电子排布式。
①第4周期IVB族____________ 、____________ ;
②第5周期VIIA族____________ 、____________ 。
(1)已知下列元素基态原子的电子排布式,判断它们所在的周期和族。
①
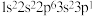
②

③

④
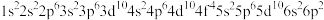
(2)已知下列元素在周期表中的位置,写出它们的元素符号和价电子排布式。
①第4周期IVB族
②第5周期VIIA族
更新时间:2020-04-09 10:09:42
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表列出了①~⑩十种元素在周期表中的位置。
请用化学用语和必要的文字按要求回答下列问题:
(1)写出①的同位素氘的原子符号___ ;元素③和⑧形成的化合物中的化学键类型为___ ,用电子式表示其形成过程___ ;元素①、⑤和⑧形成的三原子化合物的电子式为___ 。
(2)①-⑩元素最高价氧化物对应的水化物酸性最强的是___ (填化学式),碱性最强的是___ (填化学式),呈两性的氧化物与强碱反应的离子方程式为___ 。
(3)元素⑤、⑥、⑦的单质氧化性依次___ (填“增强”或“减弱”),其气态氢化物中稳定性最弱的是___ 。(均填化学式)
(4)②③④⑥⑧元素原子半径由大到小的顺序为___ ;①~⑥元素能形成10电子简单离子中半径最大的是___ 。(均用化学符号表示)

请用化学用语和必要的文字按要求回答下列问题:
(1)写出①的同位素氘的原子符号
(2)①-⑩元素最高价氧化物对应的水化物酸性最强的是
(3)元素⑤、⑥、⑦的单质氧化性依次
(4)②③④⑥⑧元素原子半径由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分(注意:用元素符号或化学式填空)
(1)C的离子的结构示意图____ ,G元素的氧化物化学式___ ,H的氢化物的化学式__________ 。
(2)H元素的单质的电子式_____ ;
(3)A-H八种元素中(a)原子半径最大的元素是____ ,(b)单质的还原性最强的元素是____ ,(c)最高价氧化物对应水化物酸性最强的是_____ ;(d)最高价氧化物对应水化物碱性最强的是_______ 。
(4)用电子式表示AE 2的形成过程_______________ 。
(5)B与C的最高价氧化物对应水化物反应的离子方程式_______________ 。
 族 族周期 | ⅠA | ⅡA | ⅢA | IVA | VA | VIA | VIIA | O族 |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A | ||||||
(2)H元素的单质的电子式
(3)A-H八种元素中(a)原子半径最大的元素是
(4)用电子式表示AE 2的形成过程
(5)B与C的最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
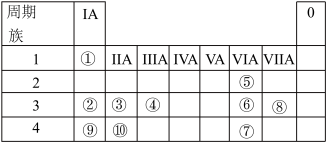
【推荐3】下表为元素周期表的一部分,列出了7种元素在元素周期表中的位置:
请按要求回答下列问题:
(1)7种元素中,原子半径最小的是_____ (填序号)。
(2)写出③的元素符号___________ 。
(3)写出⑦的元素名称___________ ,⑦的元素形成的单质常见用途是______________ 。
(4)元素④的氢化物与元素⑧的单质反应的化学方程式为___________________ 。
(5)元素⑤和元素⑥最高价氧化物的水化物碱性由强到弱关系为_______________ (用化学式表示)。
(6)元素②形成的最简单氢化物的空间结构为_____________ 。
(7)元素⑥的最高价氧化物的水化物和元素⑧形成的氢化物反应的离子方程式__________ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
请按要求回答下列问题:
(1)7种元素中,原子半径最小的是
(2)写出③的元素符号
(3)写出⑦的元素名称
(4)元素④的氢化物与元素⑧的单质反应的化学方程式为
(5)元素⑤和元素⑥最高价氧化物的水化物碱性由强到弱关系为
(6)元素②形成的最简单氢化物的空间结构为
(7)元素⑥的最高价氧化物的水化物和元素⑧形成的氢化物反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,与FeS2可联合制备铁粉精(FexOy)和H2SO4。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为_________ 。
(2)比较 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:_________ 。
(3) 与
与 和
和 之间的作用力分别为
之间的作用力分别为_________ 。
ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。
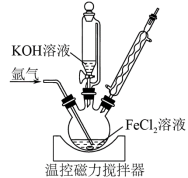
①三颈烧瓶发生反应的离子方程式为_________ 。
②检验反应是否进行完全的操作是_________ 。
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是_________ 。
②计算实验所得产品的产率_________ 。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为
(2)比较
 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:(3)
 与
与 和
和 之间的作用力分别为
之间的作用力分别为ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。

①三颈烧瓶发生反应的离子方程式为
②检验反应是否进行完全的操作是
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是
②计算实验所得产品的产率
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】高氯酸三碳酰肼合镍 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:
(1)基态Ni原子的电子排布式为_______ 。
(2)基态碳原子核外电子有_______ 种不同运动状态。
(3) 的中心原子的价层电子对数为
的中心原子的价层电子对数为_______ , 的VSEPR模型是
的VSEPR模型是_______ 。
(4)化学式中的CHZ为碳酰肼,其结构为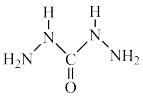 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:
①CHZ中氮原子的杂化轨道类型为_______ 。
②1molCHZ中含有的σ键数目为_______ NA。
③键角:
_______ (填“>”“<”或“=”) 。
。
(5)常温下, 的HClO溶液的pH约为
的HClO溶液的pH约为_______ [已知: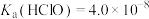 ,
, ]。
]。
 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:(1)基态Ni原子的电子排布式为
(2)基态碳原子核外电子有
(3)
 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的VSEPR模型是
的VSEPR模型是(4)化学式中的CHZ为碳酰肼,其结构为
 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:①CHZ中氮原子的杂化轨道类型为
②1molCHZ中含有的σ键数目为
③键角:

 。
。(5)常温下,
 的HClO溶液的pH约为
的HClO溶液的pH约为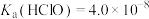 ,
, ]。
]。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题
(1)钛在元素周期表中的位置___________ ,基态钛原子的价层电子轨道表示式为___________ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有___________ 种。下列状态的钛元素形成得微粒中,电离其最外层的一个电子所需能量最小的是___________ (填序号)。
A.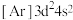 B.
B.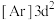 C.
C.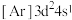 D.
D.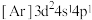
(2)第三周期元素中第一电离能介于Al和P的元素有___________ 种。与Co同周期,基态原子有1个未成对电子的元素有___________ 种。
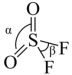
(3) 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
(4) 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为___________ ,其主要原因是___________ 。
(5)铜离子的一种配合物化学式为 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为___________ 。
(6)醋酸 中C原子的杂化类型为
中C原子的杂化类型为___________ 。
(7)等物质的量的 和
和 中,σ键数目之比
中,σ键数目之比___________ 。
(1)钛在元素周期表中的位置
A.
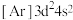 B.
B.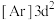 C.
C.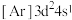 D.
D.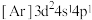
(2)第三周期元素中第一电离能介于Al和P的元素有
(3)
 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是
(4)
 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为(5)铜离子的一种配合物化学式为
 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为(6)醋酸
 中C原子的杂化类型为
中C原子的杂化类型为(7)等物质的量的
 和
和 中,σ键数目之比
中,σ键数目之比
您最近一年使用:0次



