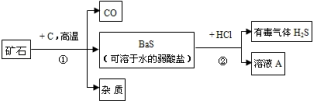
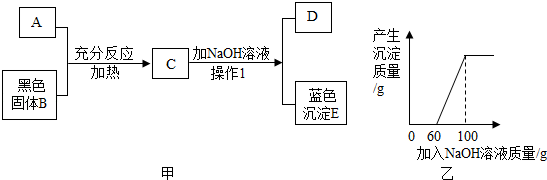
为分析由氧化铜和铜组成的某混合物中氧化铜的质量分数,现取3份该混合物各20克,分别缓慢加入50克、100克、150克的某稀硫酸中,测得三组实验数据如右表:
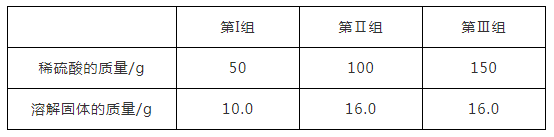
(1)第2组实验中反应物_____ (填“氧化铜”、“稀硫酸”或“氧化铜与稀硫酸”)反应完。
(2)20克样品中含铜的质量分数为_____ 。
(3)根据表中数据计算所用的稀硫酸溶质的质量分数(写出计算过程)_____ 。
(4)将第2组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图_____ 。
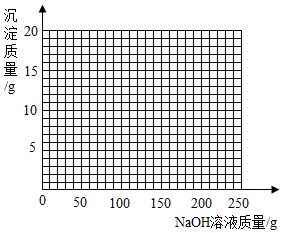

(1)第2组实验中反应物
(2)20克样品中含铜的质量分数为
(3)根据表中数据计算所用的稀硫酸溶质的质量分数(写出计算过程)
(4)将第2组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图

2020·浙江杭州·模拟预测 查看更多[1]
更新时间:2020-09-11 17:17:56
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】如图表示五种不同类别物质间的关系。A是铁锈的主要成分,C俗称苛性钠,请结合图示回答问题(图中“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质)。
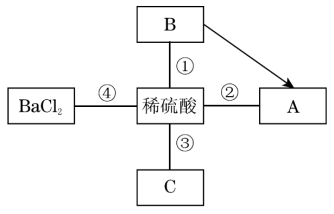
(1)B物质是__________ ;
(2)在①、②、③、④四个反应中,不能体现酸的化学通性的是________ (填序号)。

(1)B物质是
(2)在①、②、③、④四个反应中,不能体现酸的化学通性的是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】在天平的两个托盘上各放一只烧杯,烧杯中都盛有质量和质量分数相等的稀盐酸,此时天平保持平衡,如果在烧杯中分别同时投入相同质量的足量的锌粉和镁粉。
在整个反应过程中天平指针将会如何偏转呢?请判断指针发生偏转的情况并分析原因。______________________
在整个反应过程中天平指针将会如何偏转呢?请判断指针发生偏转的情况并分析原因。
您最近一年使用:0次
解答题
|
较难
(0.4)
名校
【推荐1】某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液;反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
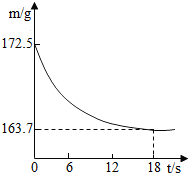
(1)生成CO2的质量为_______ ;
(2)求恰好完全反应后所得到不饱和NaCl溶液中溶质的质量分数。_______

(1)生成CO2的质量为
(2)求恰好完全反应后所得到不饱和NaCl溶液中溶质的质量分数。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】实验室有五种失去标签的无色溶液,它们分别是稀盐酸,稀硫酸,氯化钠溶液、氢氧化钠溶液、氢氧化钡溶液中的一种,为完成鉴别同学们设计如下方案,五种溶液分别标号A、B、 C、D、E。
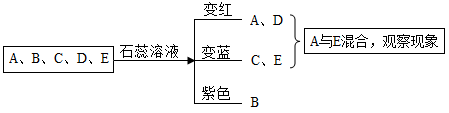
(1)另取A与E混合,若出现的现象是______ 可完成所有物质的鉴别;
(2)实验后,将所有试管中的物质倒入干净的烧杯中,过滤得白色沉淀和红色溶液。向所得红色溶液中加入足量下列物质,一定会有明显实验现象的是______ 。
A.AgNO3溶液 B.Na2SO4溶液 C.Ba(OH)2溶液 D.Na2CO3溶液

(1)另取A与E混合,若出现的现象是
(2)实验后,将所有试管中的物质倒入干净的烧杯中,过滤得白色沉淀和红色溶液。向所得红色溶液中加入足量下列物质,一定会有明显实验现象的是
A.AgNO3溶液 B.Na2SO4溶液 C.Ba(OH)2溶液 D.Na2CO3溶液
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】某废液M可能含有硫酸钠、氯化钠、碳酸钠、氢氧化钠中的一种或几种,为确定其成分进行实验。
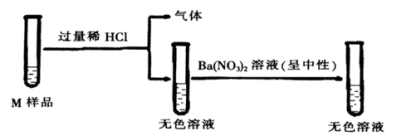
(1)反应生成气体的化学方程式是_____ 。
(2)M中一定没有_____ 。
(3)为进一步确定M的成分,进行实验,步骤如下:
Ⅰ 重新取M样品,滴加过量的试剂X,静置;
Ⅱ 取Ⅰ中的上层清液,滴加酚酞;
Ⅲ 向Ⅱ中的溶液滴加过量的稀硝酸;
Ⅳ 向Ⅲ中的溶液滴加试剂Y。
完成填空:
试剂X是_____ (选填“氯化钡”或“硝酸钡”)溶液;试剂Y是_____ 溶液。能确定M中含有氢氧化钠的最主要的一个现象是_____ ;能确定M中含有氯化钠的最主要的一个现象是_____ 。(需写明现象对应的步骤编号)

(1)反应生成气体的化学方程式是
(2)M中一定没有
(3)为进一步确定M的成分,进行实验,步骤如下:
Ⅰ 重新取M样品,滴加过量的试剂X,静置;
Ⅱ 取Ⅰ中的上层清液,滴加酚酞;
Ⅲ 向Ⅱ中的溶液滴加过量的稀硝酸;
Ⅳ 向Ⅲ中的溶液滴加试剂Y。
完成填空:
试剂X是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】在完成实验“二氧化碳的制取”后,废液桶中倾倒了含有较多盐酸的混合溶液。为避免酸液污染环境,化学兴趣小组做了如下实验:取废液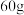 ,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液
,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液 与加入的碳酸钠溶液的质量关系如右图所示:(不考虑
与加入的碳酸钠溶液的质量关系如右图所示:(不考虑 溶于水对溶液酸碱性的影响)
溶于水对溶液酸碱性的影响)
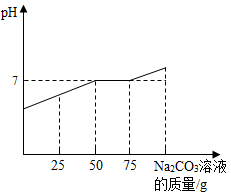
(1)通过右图可知,当碳酸钠溶液质量加到_____  时,废液中的盐酸恰好处理完。
时,废液中的盐酸恰好处理完。
(2)计算废液中氯化钙的质量分数_____ 。
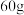 ,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液
,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液 与加入的碳酸钠溶液的质量关系如右图所示:(不考虑
与加入的碳酸钠溶液的质量关系如右图所示:(不考虑 溶于水对溶液酸碱性的影响)
溶于水对溶液酸碱性的影响)
(1)通过右图可知,当碳酸钠溶液质量加到
 时,废液中的盐酸恰好处理完。
时,废液中的盐酸恰好处理完。(2)计算废液中氯化钙的质量分数
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】某同学为了研究生石灰CaO露置于空气中变质情况,设计如下实验,请通过分析计算:
取10克生石灰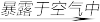 粉末A质量为12克
粉末A质量为12克 气体B
气体B
 沉淀质量为2.5克。
沉淀质量为2.5克。
(1)生成气体B的质量为_________ ;
(2)粉末A的成分除CaO外还有_________ (写化学式);
(3)粉末A中CaO质量分数是_________ (结果精确到0.1%)。
取10克生石灰
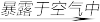 粉末A质量为12克
粉末A质量为12克 气体B
气体B
 沉淀质量为2.5克。
沉淀质量为2.5克。(1)生成气体B的质量为
(2)粉末A的成分除CaO外还有
(3)粉末A中CaO质量分数是
您最近一年使用:0次