分类,类比是初中化学常用的学习方法。
(1)初中化学有许多实验,若按照实验方法分类,可将实验_____ (填字母)分为一类;分类的依是_____ 。
(2)磷酸盐,磷酸氢盐的溶解性和碳酸盐相似,磷酸二氢盐和碳酸氢盐溶解性相似,则磷酸钡的溶解性为_____ (填“可溶”或“微溶”或“难溶”),碳酸钙可以和水、二氧化碳(看做碳酸)反应生成碳酸氢钙,请写出向磷酸钙固体中加入磷酸(H3PO4)溶液后,固体消失的反应的化学方程式_____ 。
(1)初中化学有许多实验,若按照实验方法分类,可将实验
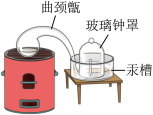 | 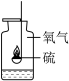 | 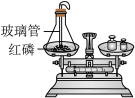 | 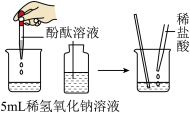 |
| A.测定空气中氧气的含量 | B.探究硫在氧气中燃烧 | C.探究反应前后物质的质量关系 | D.探究酸和碱能否发生反应 |
(2)磷酸盐,磷酸氢盐的溶解性和碳酸盐相似,磷酸二氢盐和碳酸氢盐溶解性相似,则磷酸钡的溶解性为
更新时间:2019-06-24 22:21:12
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组的同学利用下图所示的装置,对质量守恒定律进行探究。试回答下列问题:

(1)I、提出假设:白磷在空气中燃烧符合质量守恒定律吗?
Ⅱ、设计实验:小云同学将一定质量的白磷放入装置内,称得A装置的总质量为203.1g,然后将烧红的玻璃管伸入瓶内,并立即塞紧玻璃塞。
Ⅲ、观察现象:此时观察到锥形瓶内的现象是______ ,装置冷却后,再次称量A装置总质量为203.1g。
1V、总结:①该反应符合质量守恒定律;
②在实验设计上,玻璃管上方系一瘪气球的目的是______ 。
③实验结束后(锥形瓶已冷却至室温),发现瓶中白磷过量,为防止白磷在空气中燃烧,将锥形瓶瓶口倒置于盛满水的水槽中,拔下瓶塞,发现水进入锥形瓶中,则进入瓶中的水占锥形瓶容积的______ ,原因是______ 。
(2)小宾同学认为碳酸钠与稀盐酸反应也符合质量守恒定律,于是他设计了B装置,药品及装置的总质量为300.4g,反应结束后,他与小云的实验进行对比:冷却至室温,气球胀大的是______ (选填“A”或“B”或“A和B”),称量反应后药品及装置的总质量为300.0g,你认为小兵同学数据减少的原因可能是______ (填序号)
A.稀盐酸不足 B.碳酸钠中含有不与稀盐酸反应的杂质
C.装置气密性不好 D.气球受到浮力的影响
(3)小结:由质量守恒定律可知,化学反应前后一定不变的是______(填序号)
①原子数目②原子的种类 ③分子数目 ④分子的种类 ⑤元素的种类 ⑥物质的总质量 ⑦物质的种类
(4)某登山运动员要登上最高峰一一珠穆朗玛峰峰顶,但需要自带氧气。假如每名运动员冲顶时消耗自带液氧4.8kg,若在实验室用高锰酸钾为原料制取相同质量的氧气,则需要多少千克高锰酸钾?

(1)I、提出假设:白磷在空气中燃烧符合质量守恒定律吗?
Ⅱ、设计实验:小云同学将一定质量的白磷放入装置内,称得A装置的总质量为203.1g,然后将烧红的玻璃管伸入瓶内,并立即塞紧玻璃塞。
Ⅲ、观察现象:此时观察到锥形瓶内的现象是
1V、总结:①该反应符合质量守恒定律;
②在实验设计上,玻璃管上方系一瘪气球的目的是
③实验结束后(锥形瓶已冷却至室温),发现瓶中白磷过量,为防止白磷在空气中燃烧,将锥形瓶瓶口倒置于盛满水的水槽中,拔下瓶塞,发现水进入锥形瓶中,则进入瓶中的水占锥形瓶容积的
(2)小宾同学认为碳酸钠与稀盐酸反应也符合质量守恒定律,于是他设计了B装置,药品及装置的总质量为300.4g,反应结束后,他与小云的实验进行对比:冷却至室温,气球胀大的是
A.稀盐酸不足 B.碳酸钠中含有不与稀盐酸反应的杂质
C.装置气密性不好 D.气球受到浮力的影响
(3)小结:由质量守恒定律可知,化学反应前后一定不变的是______(填序号)
①原子数目②原子的种类 ③分子数目 ④分子的种类 ⑤元素的种类 ⑥物质的总质量 ⑦物质的种类
| A.①②⑤⑥ | B.①②③⑤ | C.①②⑤⑦ | D.③④⑥⑦ |
(4)某登山运动员要登上最高峰一一珠穆朗玛峰峰顶,但需要自带氧气。假如每名运动员冲顶时消耗自带液氧4.8kg,若在实验室用高锰酸钾为原料制取相同质量的氧气,则需要多少千克高锰酸钾?
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
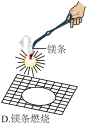
【推荐2】某化学兴趣小组的同学设计了下图A—D四个实验装置图(托盘天平略)来验证质量守恒定律。
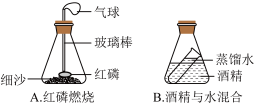
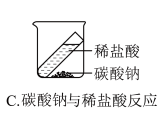
(1)雨菲同学认为只有A装置能用来验证质量守恒定律,A装置所示实验中发生反应的化学方程式______ ;在实验中看到气球的变化是______ ;他否定B装置的理由是______ 。
(2)D装置中发生反应的化学方程式______ 。
(3)D装置实验,结果在石棉网上收集到产物的质量小于镁条的质量,你认为出现这样结果的原因可能是______ 。
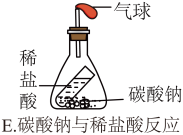
(4)炳添同学将C装置进行改进,改进后的装置如图E所示。此实验中锥形瓶内(不包括气球)的现象是______ 。
(5)通过上述实验探究可知要验证质量守恒定律,如果有气体参加或有气体生成的化学反应必须在______ 中进行。
(6)通过上述实验探究,从宏观和微观的角度理解,在化学反应前后,下列各项中肯定没有变化的是______ 。(填序号)
①原子的数目 ②分子的数目 ③元素的种类 ④原子的质量 ⑤物质的种类 ⑥原子的种类 ⑦分子的种类



(1)雨菲同学认为只有A装置能用来验证质量守恒定律,A装置所示实验中发生反应的化学方程式
(2)D装置中发生反应的化学方程式
(3)D装置实验,结果在石棉网上收集到产物的质量小于镁条的质量,你认为出现这样结果的原因可能是
(4)炳添同学将C装置进行改进,改进后的装置如图E所示。此实验中锥形瓶内(不包括气球)的现象是

(5)通过上述实验探究可知要验证质量守恒定律,如果有气体参加或有气体生成的化学反应必须在
(6)通过上述实验探究,从宏观和微观的角度理解,在化学反应前后,下列各项中肯定没有变化的是
①原子的数目 ②分子的数目 ③元素的种类 ④原子的质量 ⑤物质的种类 ⑥原子的种类 ⑦分子的种类
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】小明、小强和小峰在学习了“质量守恒定律”后来到化学实验室亲自进行了实验探究,如图是他们分别设计的实验,请你与他们一起进行探究,并回答问题。
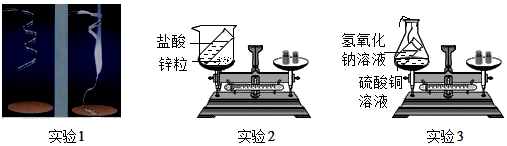
实验1:称量镁条,点燃,待反应结束后,再称量;
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量;
实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量;
数据见下表:(锌与盐酸反应:Zn+2HCl=ZnCl2+H2↑;氢氧化钠溶液与硫酸铜溶液反应:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
(1)写出实验1反应的化学方程式_____ ;
(2)上述三个反应_____ (填“符合”或“不符合”)质量守恒定律,实验_____ 正确反映了反应物与生成物的质量关系;
(3)由上述实验我们得到启示,探究_____ 的反应验证质量守恒定律,实验必须在密闭的装置中进行;
(4)由质量守恒定律可知,化学反应前后,一定不变的是_____ (填序号);
①物质种类②元素种类③原子种类④分子种类⑤分子数目⑥原子数目。

实验1:称量镁条,点燃,待反应结束后,再称量;
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量;
实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量;
数据见下表:(锌与盐酸反应:Zn+2HCl=ZnCl2+H2↑;氢氧化钠溶液与硫酸铜溶液反应:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
| 编号 | 实验1 | 实验2 | 实验3 |
| 反应前称量质量 | 9.6g | 212.6g | 118.4g |
| 反应后称量质量 | 16.0g | 212.4g | 118.4g |
(1)写出实验1反应的化学方程式
(2)上述三个反应
(3)由上述实验我们得到启示,探究
(4)由质量守恒定律可知,化学反应前后,一定不变的是
①物质种类②元素种类③原子种类④分子种类⑤分子数目⑥原子数目。
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】如图所示是测定空气里氧气含量的装置,气密性良好,在集气瓶内加入少量水,将水面上方空间分为5等份,用弹簧夹夹紧胶皮管。点燃红磷后,迅速伸入瓶中并塞紧塞子;待燃烧停止并冷却至室温后,打开弹簧夹。

(1)空气是混合物,其中含有氧气、_______ 、稀有气体、二氧化碳等,其中氧气按体积计算约占空气体积的_____ 。
(2)初中阶段,我们用如右图所示的装置和药品研究空气的组成。
a.红磷燃烧时,加入过量红磷的目的是_______________ 。
b.红磷燃烧的实验现象是____________ 。
c.写出发生反应的文字表达式________ 。
d.实验过程中,燃着的红磷熄灭后,当冷却至室温时,水能进入集气瓶中,其原因为________ 。

(1)空气是混合物,其中含有氧气、
(2)初中阶段,我们用如右图所示的装置和药品研究空气的组成。
a.红磷燃烧时,加入过量红磷的目的是
b.红磷燃烧的实验现象是
c.写出发生反应的文字表达式
d.实验过程中,燃着的红磷熄灭后,当冷却至室温时,水能进入集气瓶中,其原因为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】用燃烧红磷法测定空气中氧气的含量,如图1所示,请回答下列问题。

(1)红磷点燃后观察到的现象是___________ 。该反应的文字(或符号)表达式为 _______ 。待红磷燃烧熄灭并冷却到室温后,打开弹簧夹,发现水被吸入集气瓶,水面上升,约占瓶内原有空气体积的 _______ 。
(2)实验完毕,若进入集气瓶中水的体积比预期结果小,你认为导致这一结果的原因可能是_____ (写一条即可)。
(3)实验中不能用铁丝代替红磷,原因______ 。
(4)小龙同学对实验进行反思后,提出了改进方法,如图2所示,你认为实验改进后的优点是________ 。

(1)红磷点燃后观察到的现象是
(2)实验完毕,若进入集气瓶中水的体积比预期结果小,你认为导致这一结果的原因可能是
(3)实验中不能用铁丝代替红磷,原因
(4)小龙同学对实验进行反思后,提出了改进方法,如图2所示,你认为实验改进后的优点是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】下图是初中化学涉及的重要的实验及操作图,按要求完成各题:
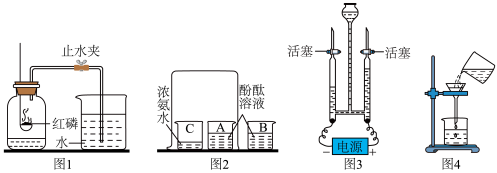
(1)①图1探究的内容是:______ 。
②集气瓶内放少量水的目的是:______ 。
③实验过程看到的现象是红磷燃烧,产生______ ;恢复到室温打开止水夹,烧杯中的水倒流进入集气瓶,进入集气瓶的水占瓶内气体体积的五分之一。
④实验结论是:氧气约占空气体积的______ 。
⑤若选择木炭做可燃物,导致测得的结果______ ,原因是______ 。
(2)图2装置中______ (填“A”或“B”或“C”)烧杯中的液体变红,通过实验现象得出______ 。此实验中B烧杯的作用是______ 。
(3)①图3为电解水实验,写出反应的文字表达式______ 。
②实验时加入少量的氢氧化钠溶液的目的是______ 。
③负极收集到的气体与正极收集到的气体体积比为______ ,用______ 检验两种气体,其中检验正极气体时看到的现象是______ 。
(4)①指出图4实验中的明显两处错误:
错误一______ ;错误二______ 。
②若滤纸没有紧贴在漏斗内壁上,导致的后果是______ 。
③过滤后液体仍然浑浊的原因______ (答一点)。
④水的净化过程中过滤只是除去水中的______ (填“不溶性”或“可溶性”)杂质。

(1)①图1探究的内容是:
②集气瓶内放少量水的目的是:
③实验过程看到的现象是红磷燃烧,产生
④实验结论是:氧气约占空气体积的
⑤若选择木炭做可燃物,导致测得的结果
(2)图2装置中
(3)①图3为电解水实验,写出反应的文字表达式
②实验时加入少量的氢氧化钠溶液的目的是
③负极收集到的气体与正极收集到的气体体积比为
(4)①指出图4实验中的明显两处错误:
错误一
②若滤纸没有紧贴在漏斗内壁上,导致的后果是
③过滤后液体仍然浑浊的原因
④水的净化过程中过滤只是除去水中的
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据下列图示实验回答问题.
A B
B C
C D
D
(1)上述装置中的实验都是物质在空气或氧气中燃烧,反应中都有的现象是________ ,
(2)若在B装置中预先放少量的澄清石灰水,其作用是________ .
(3)A、C中少量水的作用分别是________ 、 ________ .
A
 B
B C
C D
D
(1)上述装置中的实验都是物质在空气或氧气中燃烧,反应中都有的现象是
(2)若在B装置中预先放少量的澄清石灰水,其作用是
(3)A、C中少量水的作用分别是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】根据下列图1、图2、图3回答问题:

(1)图1中:红磷熄灭并冷却后,打开止水夹,集气瓶内水位最终约在刻度_______ 处,由此得出:氧气约占空气体积的_______ 。已知金属镁在空气中燃烧,可分别与氧气和氮气反应,都生成固体物质,该实验中的红磷_______ (填“能”或“不能”)用镁来代替。
(2)图2中:硫在氧气中燃烧时,可观察到的现象是_______ ;铁丝在氧气中燃烧时,集气瓶内水的作用是_______ ,该反应的文字表达式为_______ 。
(3)图3中:可观察到的现象是_______ ,由此实验得出的结论是:分子_______ 。

(1)图1中:红磷熄灭并冷却后,打开止水夹,集气瓶内水位最终约在刻度
(2)图2中:硫在氧气中燃烧时,可观察到的现象是
(3)图3中:可观察到的现象是
您最近一年使用:0次
【推荐1】实验小组对稀NaOH溶液与稀盐酸的反应进行研究。实验装置见图1。用恒压漏斗匀速滴加某溶液,过程中,溶液pH和温度随时间的变化分别见图2和图3。______ ,恒压漏斗能匀速滴加溶液的原因是______ 。
(2)溶液X是______ ,40s时溶液中质量分数最高的溶质是______ 。
(3)盐酸和氢氧化钠反应的化学反应方程式为______ ,反应过程中溶液温度先升高后下降的原因是______ 。
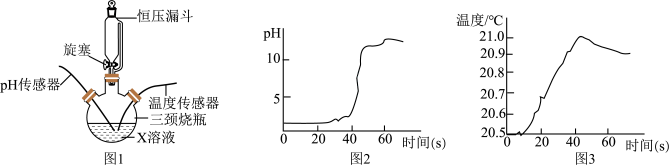
(2)溶液X是
(3)盐酸和氢氧化钠反应的化学反应方程式为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】初中化学课上,同学们利用下列实验探究碱的化学性质:

(1)A实验恰好完全反应后的实验现象为______ 。
(2)若要用广泛pH试纸测定反应后溶液的pH,以下说法错误的是______ 。
A.先用水润湿pH试纸
B. 用玻璃棒蘸取待测液,滴在pH试纸上
C. 与标准比色卡对照后,得出溶液的pH=7.0
(3)B实验中反应的化学方程式为______ 。
(4)实验结束后,同学们将A、B、C中的废液倒入同一只废液缸中,最后发现废液浑浊并显红色。得知该废液显______ 性。为探究废液的成分,将废液过滤,向滤液中加入足量的硝酸钙溶液,得到白色沉淀,红色褪去。于是同学们确定加硝酸钙溶液之前废液中除酚酞、碳酸钙、水以外,肯定还含有的物质是______ (填化学用语,下同),一定没有的阴离子是______ 。

(1)A实验恰好完全反应后的实验现象为
(2)若要用广泛pH试纸测定反应后溶液的pH,以下说法错误的是
A.先用水润湿pH试纸
B. 用玻璃棒蘸取待测液,滴在pH试纸上
C. 与标准比色卡对照后,得出溶液的pH=7.0
(3)B实验中反应的化学方程式为
(4)实验结束后,同学们将A、B、C中的废液倒入同一只废液缸中,最后发现废液浑浊并显红色。得知该废液显
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐3】重庆一中化学兴趣小组分别设计了3组与“酸碱中和反应”有关的实验。
【第一组】提出问题:探究氢氧化钠溶液和盐酸的反应是否放热。
进行实验:向盛有氢氧化钠溶液的试管中,逐滴匀速加入稀盐酸。
(1)符合这一过程中pH变化的曲线为_____。
(2)用温度传感器测量反应过程中溶液的温度,发现温度明显升高。为确定该反应是否为放热反应,需补做下列实验:分别向上述实验所用的氢氧化钠溶液、盐酸溶液中加水稀释,并用温度传感器测定实验过程中温度的变化,实验所得图像分别如图:
实验结论:氢氧化钠溶液和盐酸的反应是放热反应。
【第二组】实验目的:用电导率传感器测量氢氧化钠溶液中滴加稀盐酸的电导率变化(如图)。
①电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小(离子浓度指溶液中某种离子的数目与溶液总体积之比)。
②相同温度下溶液电导率越大离子浓度越大。
分析讨论:
(3)①如图表示该反应过程中烧杯内不同时间点的微观粒子示意图,按时间先后排列的顺序为_____ (填序号)。_____ (用文字描述)。
【第三组】发现问题:进行下图实验后,取试管C中的无色溶液加热浓缩,“意外”发现溶液由无色又变成红色。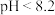 的溶液中呈无色,在
的溶液中呈无色,在 的溶液中呈红色。
的溶液中呈红色。
分析讨论:反应后无色溶液中仍存在少量_____ 离子,加热蒸发,其浓度增大,使溶液的颜色变红。
迁移拓展:另取一组药品进行如上图实验,并取C中溶液用精密仪器测得 的离子个数之比为1∶1∶1,则该溶液应为
的离子个数之比为1∶1∶1,则该溶液应为_____ (填“酸性”、“中性”或“碱性”)。
【第一组】提出问题:探究氢氧化钠溶液和盐酸的反应是否放热。
进行实验:向盛有氢氧化钠溶液的试管中,逐滴匀速加入稀盐酸。
(1)符合这一过程中pH变化的曲线为_____。
A. | B. |
C. | D. |
(2)用温度传感器测量反应过程中溶液的温度,发现温度明显升高。为确定该反应是否为放热反应,需补做下列实验:分别向上述实验所用的氢氧化钠溶液、盐酸溶液中加水稀释,并用温度传感器测定实验过程中温度的变化,实验所得图像分别如图:

| A.只有氢氧化钠溶液 |
| B.只有稀盐酸 |
| C.氢氧化钠溶液和稀盐酸 |
实验结论:氢氧化钠溶液和盐酸的反应是放热反应。
【第二组】实验目的:用电导率传感器测量氢氧化钠溶液中滴加稀盐酸的电导率变化(如图)。

①电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小(离子浓度指溶液中某种离子的数目与溶液总体积之比)。
②相同温度下溶液电导率越大离子浓度越大。
分析讨论:
(3)①如图表示该反应过程中烧杯内不同时间点的微观粒子示意图,按时间先后排列的顺序为

【第三组】发现问题:进行下图实验后,取试管C中的无色溶液加热浓缩,“意外”发现溶液由无色又变成红色。

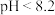 的溶液中呈无色,在
的溶液中呈无色,在 的溶液中呈红色。
的溶液中呈红色。分析讨论:反应后无色溶液中仍存在少量
迁移拓展:另取一组药品进行如上图实验,并取C中溶液用精密仪器测得
 的离子个数之比为1∶1∶1,则该溶液应为
的离子个数之比为1∶1∶1,则该溶液应为
您最近一年使用:0次




