解题方法
1 . 下列化学用语与其对应的描述都正确的是
A. ——两个氮气分子 ——两个氮气分子 | B. ——60个碳原子 ——60个碳原子 |
| C.Co——一氧化碳 | D.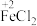 ——氯化亚铁中铁的化合价为 ——氯化亚铁中铁的化合价为 |
您最近一年使用:0次
2 . 2024年4月25日,“神舟十八号”载人飞船发射圆满成功。因减重需要,此次发射的火箭推进舱使用的是极端制造的2.4米超宽铝合金薄板,铝合金板材属于
| A.合成材料 | B.金属材料 | C.复合材料 | D.无机材料 |
您最近一年使用:0次
2024九年级下·辽宁·专题练习
3 . 对于金属材料,我们应该从多角度了解。
I、金属的冶炼
(1)锡是最早发现并使用的金属之一,现广泛应用于航天、电子信息、化工等领域。锡砂主要成分为SnO2(杂质不含锡元素),其含锡量约为70%,则该锡砂中SnO2的质量分数约为______ (结果保留一位小数)。
(2)“古法炼锡”工艺流程:将木炭和锡砂相间逐层投入锡炉,高温熔炼冶锡,同时会产生CO,该反应的化学方程式为______ 。炼制时,“点铅勾锡”是炼锡的关键,加铅能使锡较易熔化流出,其原因是______ 。
Ⅱ、金属的性质
(3)研究人员取等质量、颗粒大小相同、不同锡含量的锡铝合金,加入25℃50mL的蒸馏水中,氢气产量与时间关系曲线如图所示。______ 。
②铝跟热水反应时易形成致密的氧化膜阻碍反应,加入锡制成锡铝合金后能破坏氧化膜。据图分析,在相同实验条件下,0~8min内,锡含量与产生氢气的速率关系为______ 。
Ⅲ、金属的锈蚀与防护
(4)将锡镀于铁制品表面可防止铁生锈,其原理是______ 。
(5)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。“发蓝”过程属于______ (填“物理“或“化学”)变化。
Ⅳ、金属的回收再利用
某工厂为充分利用废弃金属,将严重生锈的废铁屑(杂质不溶于水也不与稀盐酸反应)经过如图流程制备高铁酸钾。
②氧化时,发生的反应有4HCl+4FeCl2+O2=4FeCl3+2H2O
③高铁酸钾(K2FeO4)是一种绿色环保、多功能水处理剂。
(6)“酸浸”过程中为了提高铁元素的浸出率,除了适当提高酸的浓度、适当升高温度、搅拌,还可以采取的措施是______ 。
(7)“酸浸”后溶液中可能含有的阳离子除了Fe2+还有______ (填离子符号)。
(8)反应I中涉及的化学反应有:2FeCl3+3NaClO+10NaOH=2Na2FeO4+aNaCl+5H2O。其中a=______ 。
(9)反应Ⅱ主要涉及饱和KOH溶液与Na2FeO4溶液之间的复分解反应,推测溶解度:K2FeO4______ Na2FeO4(填“>”、“=”或“<”)。
I、金属的冶炼
(1)锡是最早发现并使用的金属之一,现广泛应用于航天、电子信息、化工等领域。锡砂主要成分为SnO2(杂质不含锡元素),其含锡量约为70%,则该锡砂中SnO2的质量分数约为
(2)“古法炼锡”工艺流程:将木炭和锡砂相间逐层投入锡炉,高温熔炼冶锡,同时会产生CO,该反应的化学方程式为
Ⅱ、金属的性质
(3)研究人员取等质量、颗粒大小相同、不同锡含量的锡铝合金,加入25℃50mL的蒸馏水中,氢气产量与时间关系曲线如图所示。

②铝跟热水反应时易形成致密的氧化膜阻碍反应,加入锡制成锡铝合金后能破坏氧化膜。据图分析,在相同实验条件下,0~8min内,锡含量与产生氢气的速率关系为
Ⅲ、金属的锈蚀与防护
(4)将锡镀于铁制品表面可防止铁生锈,其原理是
(5)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。“发蓝”过程属于
Ⅳ、金属的回收再利用
某工厂为充分利用废弃金属,将严重生锈的废铁屑(杂质不溶于水也不与稀盐酸反应)经过如图流程制备高铁酸钾。
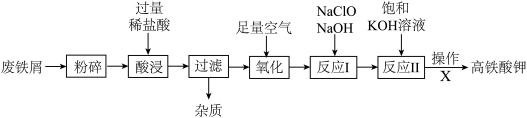
②氧化时,发生的反应有4HCl+4FeCl2+O2=4FeCl3+2H2O
③高铁酸钾(K2FeO4)是一种绿色环保、多功能水处理剂。
(6)“酸浸”过程中为了提高铁元素的浸出率,除了适当提高酸的浓度、适当升高温度、搅拌,还可以采取的措施是
(7)“酸浸”后溶液中可能含有的阳离子除了Fe2+还有
(8)反应I中涉及的化学反应有:2FeCl3+3NaClO+10NaOH=2Na2FeO4+aNaCl+5H2O。其中a=
(9)反应Ⅱ主要涉及饱和KOH溶液与Na2FeO4溶液之间的复分解反应,推测溶解度:K2FeO4
您最近一年使用:0次
2024九年级下·辽宁·专题练习
解题方法
4 . 草木灰可作纺织品漂洗剂等,小组同学对草木灰中的成分、性质、含量和应用等进行了探究。
探究一:提取草木灰中的
【查阅资料1】①草木灰的主要成分是
② 的溶解度曲线如图1所示。
的溶解度曲线如图1所示。
步骤1:如图2所示,用60℃水浸洗草木灰。
步骤2:过滤,洗涤滤渣2次,合并滤液。
步骤3:蒸发滤液,结晶并烘干得到 固体。
固体。
(1)步骤1中选用60℃的温水而不用冷水浸洗草木灰的原因是______ 。
(2)根据图3所示的信息,请从节能与省时两方面综合考虑,提取草木灰中 比较适宜的转速和浸取时间为
比较适宜的转速和浸取时间为______ 。 溶液显碱性的原因。
溶液显碱性的原因。
【查阅资料2】:氯化钙的水溶液呈中性。
【猜想与假设】猜想1:溶液呈碱性是由于溶液中的 引起的。
引起的。
猜想2:溶液呈碱性是由于溶液中的引起的。
【进行实验2】
(3)向1支洁净的小试管中加入少量 固体,再加入少量蒸馏水,振荡,待固体完全溶解后,滴入3滴酚酞溶液,溶液变红,再逐滴滴入
固体,再加入少量蒸馏水,振荡,待固体完全溶解后,滴入3滴酚酞溶液,溶液变红,再逐滴滴入 溶液至过量时,出现
溶液至过量时,出现______ 现象,说明溶液呈碱性是由于溶液中的 引起的。
引起的。
实验三:测定碳酸钾含量
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
【进行实验3】
取上述第三步中固体3.30g进行图4实验。______ 。
【数据与解释】
(5)称量图4中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为______ %,与表格中数据相比明显偏低,原因可能是______ (填序号)。
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
探究四:草木灰的应用。
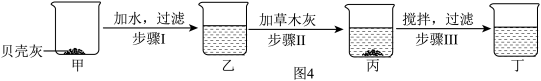
【查阅资料3】《周礼考工记》中载有“涑帛”的方法,即利用“灰”(草木灰)和“蜃”(贝壳灰,主要成分为CaO)混合加水所得溶液来洗涤丝帛,使其与茧层丝胶蛋白发生反应而溶解(脱胶),经过水洗后可使丝洗得干净亮丽。
【进行实验4】根据上述资料设计如图4所示的实验,并对丁中溶液的成分进行了探究。
【作出猜想】
(6)猜想1:只有KOH 猜想2:KOH和 猜想3:
猜想3:______ 。
【进行实验5】
(7)取少量丁中澄清溶液分别加入试管A、B中:
【延伸应用】
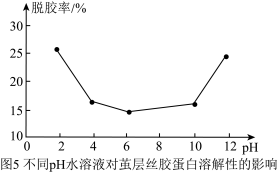
(8)同学们查阅资料得知,根据图5所示数据分析,选用______(填字母)洗涤丝帛效果较好。
探究一:提取草木灰中的

【查阅资料1】①草木灰的主要成分是

②
 的溶解度曲线如图1所示。
的溶解度曲线如图1所示。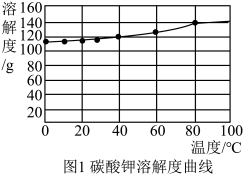
步骤1:如图2所示,用60℃水浸洗草木灰。
步骤2:过滤,洗涤滤渣2次,合并滤液。
步骤3:蒸发滤液,结晶并烘干得到
 固体。
固体。
(1)步骤1中选用60℃的温水而不用冷水浸洗草木灰的原因是
(2)根据图3所示的信息,请从节能与省时两方面综合考虑,提取草木灰中
 比较适宜的转速和浸取时间为
比较适宜的转速和浸取时间为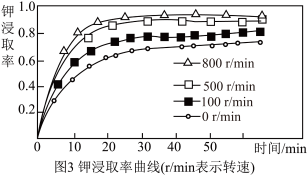
 溶液显碱性的原因。
溶液显碱性的原因。【查阅资料2】:氯化钙的水溶液呈中性。
【猜想与假设】猜想1:溶液呈碱性是由于溶液中的
 引起的。
引起的。猜想2:溶液呈碱性是由于溶液中的引起的。
【进行实验2】
(3)向1支洁净的小试管中加入少量
 固体,再加入少量蒸馏水,振荡,待固体完全溶解后,滴入3滴酚酞溶液,溶液变红,再逐滴滴入
固体,再加入少量蒸馏水,振荡,待固体完全溶解后,滴入3滴酚酞溶液,溶液变红,再逐滴滴入 溶液至过量时,出现
溶液至过量时,出现 引起的。
引起的。实验三:测定碳酸钾含量
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
【进行实验3】
取上述第三步中固体3.30g进行图4实验。
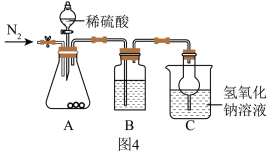
【数据与解释】
(5)称量图4中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
探究四:草木灰的应用。
【查阅资料3】《周礼考工记》中载有“涑帛”的方法,即利用“灰”(草木灰)和“蜃”(贝壳灰,主要成分为CaO)混合加水所得溶液来洗涤丝帛,使其与茧层丝胶蛋白发生反应而溶解(脱胶),经过水洗后可使丝洗得干净亮丽。
【进行实验4】根据上述资料设计如图4所示的实验,并对丁中溶液的成分进行了探究。
【作出猜想】
(6)猜想1:只有KOH 猜想2:KOH和
 猜想3:
猜想3:【进行实验5】
(7)取少量丁中澄清溶液分别加入试管A、B中:
实验序号 | 操作 | 现象 | 结论 |
1 | 向A中通入 | 溶液不变浑浊 | 猜想 |
2 | 向B中滴加少量 | 猜想2正确 |
【延伸应用】
(8)同学们查阅资料得知,根据图5所示数据分析,选用______(填字母)洗涤丝帛效果较好。
A.浓度为10%的 溶液pH=11.6 溶液pH=11.6 | B.浓度为1%的KOH溶液的pH=13.2 |
您最近一年使用:0次
2024九年级下·辽宁·专题练习
解题方法
5 . 葡萄中富含K、Ca、Na、Fe、Zn、Mg等元素,在栽种过程中容易产生病虫害,可通过定期施肥、中和酸性土壤、喷洒农药等方法来增强葡萄抗病能力。若发病,可用硫酸铜配制农药波尔多液进行喷洒。
葡萄酒是以鲜葡萄或葡萄汁为原料,经酿酒酵母菌株将葡萄汁中的糖转化为酒精,同时生成了高级醇、酯类、单萜等香气化合物。
葡萄酒酿造的工艺流程如图所示。
为防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,葡萄酒酿制中还会适量添加SO2,其添加量对主要香气物质总量影响如图2所示。国际食品添加剂联合专家委员会(JECFA)制定的二氧化硫安全摄入限是每天每公斤体重0.7mg。
(1)“压榨取汁”类似于实验室中的______ 操作。
(2)在制造葡萄酒的原料葡萄中,属于人体中微量元素的有______ 。
(3)配制农药波尔多液时,不宜用铝制容器,其原因是______ (用化学方程式表示)。
(4)在酿造葡萄酒的过程中,加入一定量SO2的作用是______ 。
(5)对于一个体重65kg的成年人,每天二氧化硫安全摄入量是______ mg。
(6)下列说法正确的是______ (填字母)。
a.SO2添加量在100mg·L-1时,高级醇总量最高
b.酯类总量随着SO2添加量的增大而增大
c.单萜总量随着SO2添加量的增加,先增大后减小
d.氯化钠能代替二氧化硫添加到葡萄酒中
e.在其他条件相同时,发酵动力最好的酿酒酵母菌株是LA-FR
(7)发酵是将葡萄汁中的糖分转化成酒精和二氧化碳的过程。通常采用带塞的密闭式不锈钢罐进行发酵,罐内的装液量控制在80%左右。“浸渍发酵”装液时留出一定的空间,目的是______ 。
(8)用橡木桶陈酿葡萄酒,可以改善葡萄酒的色泽,并带有橡木香气和果香。从微粒的观点解释能闻到香气的主要原因是______ 。
葡萄酒是以鲜葡萄或葡萄汁为原料,经酿酒酵母菌株将葡萄汁中的糖转化为酒精,同时生成了高级醇、酯类、单萜等香气化合物。
葡萄酒酿造的工艺流程如图所示。
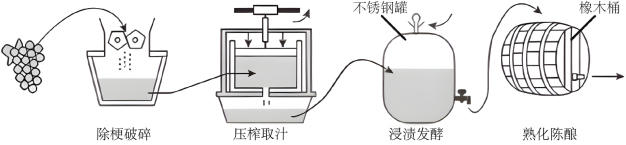
为防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,葡萄酒酿制中还会适量添加SO2,其添加量对主要香气物质总量影响如图2所示。国际食品添加剂联合专家委员会(JECFA)制定的二氧化硫安全摄入限是每天每公斤体重0.7mg。

(1)“压榨取汁”类似于实验室中的
(2)在制造葡萄酒的原料葡萄中,属于人体中微量元素的有
(3)配制农药波尔多液时,不宜用铝制容器,其原因是
(4)在酿造葡萄酒的过程中,加入一定量SO2的作用是
(5)对于一个体重65kg的成年人,每天二氧化硫安全摄入量是
(6)下列说法正确的是
a.SO2添加量在100mg·L-1时,高级醇总量最高
b.酯类总量随着SO2添加量的增大而增大
c.单萜总量随着SO2添加量的增加,先增大后减小
d.氯化钠能代替二氧化硫添加到葡萄酒中
e.在其他条件相同时,发酵动力最好的酿酒酵母菌株是LA-FR
(7)发酵是将葡萄汁中的糖分转化成酒精和二氧化碳的过程。通常采用带塞的密闭式不锈钢罐进行发酵,罐内的装液量控制在80%左右。“浸渍发酵”装液时留出一定的空间,目的是
(8)用橡木桶陈酿葡萄酒,可以改善葡萄酒的色泽,并带有橡木香气和果香。从微粒的观点解释能闻到香气的主要原因是
您最近一年使用:0次
2024九年级下·辽宁·专题练习
6 . 亚硝酸钠 外观与氯化钠相似,易溶于水,有毒。在肉类制品加工中常少量添加,用作发色剂、防腐剂,能改善腌制品的外观和风味。某兴趣小组对此开展如下探究:
外观与氯化钠相似,易溶于水,有毒。在肉类制品加工中常少量添加,用作发色剂、防腐剂,能改善腌制品的外观和风味。某兴趣小组对此开展如下探究:
探究一、认识
(1)组成: 氮元素的化合价为
氮元素的化合价为______ 价。
(2)物理性质: 被称为“工业盐”,与氯化钠一样也具有咸味。从组成分析,两种盐具有咸味的可能原因是
被称为“工业盐”,与氯化钠一样也具有咸味。从组成分析,两种盐具有咸味的可能原因是______ 。
(3)还原性:暴露在空气中的部分 会与氧气反应生成无毒的硝酸钠,写出该反应的化学方程式
会与氧气反应生成无毒的硝酸钠,写出该反应的化学方程式______ 。
探究二、影响腌鱼中 含量的因素
含量的因素
取不同质量比的鱼和盐进行腌制,采集不同时间、温度的实验数据如下:
【实验1】鱼、盐质量比 时,两种温度下亚硝酸盐含量与时间关系如图所示:
时,两种温度下亚硝酸盐含量与时间关系如图所示:______ 。
【实验2】室温下,不同鱼、盐质量比的腌鱼中亚硝酸盐含量 随时间的变化的数据如表:
随时间的变化的数据如表:
(5)①表中X=______ 。
②依据表中数据分析,欲使腌鱼中亚硝酸盐含量保持较低,合理建议是______ 。
探究三、泡菜中 含量的影响因素
含量的影响因素
泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成的。蔬菜中含有的硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐【如亚硝酸钠(NaNO2)】能与胃酸(主要成分是盐酸)反应,产生亚硝酸(HNO2)和氯化物(如NaCl)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。
(6)亚硝酸钠与盐酸反应的基本类型是______ 。
(7)室温下,用芹菜制作的泡菜,最佳食用时间是______(填字母序号)。
(8)下列关于制作泡菜的说法中,合理的是______(填字母序号)。
探究三、工业废水中的处理
(9)某工厂的金属切割加工废液中含有 的
的 ,为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液(反应原理:
,为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液(反应原理: )。若工厂需处理
)。若工厂需处理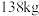 废液,计算最少需消耗
废液,计算最少需消耗 的质量
的质量______ 。
 外观与氯化钠相似,易溶于水,有毒。在肉类制品加工中常少量添加,用作发色剂、防腐剂,能改善腌制品的外观和风味。某兴趣小组对此开展如下探究:
外观与氯化钠相似,易溶于水,有毒。在肉类制品加工中常少量添加,用作发色剂、防腐剂,能改善腌制品的外观和风味。某兴趣小组对此开展如下探究:探究一、认识

(1)组成:
 氮元素的化合价为
氮元素的化合价为(2)物理性质:
 被称为“工业盐”,与氯化钠一样也具有咸味。从组成分析,两种盐具有咸味的可能原因是
被称为“工业盐”,与氯化钠一样也具有咸味。从组成分析,两种盐具有咸味的可能原因是(3)还原性:暴露在空气中的部分
 会与氧气反应生成无毒的硝酸钠,写出该反应的化学方程式
会与氧气反应生成无毒的硝酸钠,写出该反应的化学方程式探究二、影响腌鱼中
 含量的因素
含量的因素取不同质量比的鱼和盐进行腌制,采集不同时间、温度的实验数据如下:
【实验1】鱼、盐质量比
 时,两种温度下亚硝酸盐含量与时间关系如图所示:
时,两种温度下亚硝酸盐含量与时间关系如图所示:
【实验2】室温下,不同鱼、盐质量比的腌鱼中亚硝酸盐含量
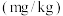 随时间的变化的数据如表:
随时间的变化的数据如表:时间/天 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
鱼、盐质量比 | 0.32 | 1.35 | 1.81 | 1.30 | 1.61 | 1.18 | 0.91 | 0.86 | 0.99 |
鱼、盐质量比 |
| 0.47 | 0.43 | 0.41 | 0.90 | 0.68 | 0.65 | 0.60 | 0.72 |
鱼、盐质量比 | 0.32 | 0.38 | 0.49 | 0.61 | 0.35 | 0.82 | 0.44 | 0.39 | 0.49 |
(5)①表中X=
②依据表中数据分析,欲使腌鱼中亚硝酸盐含量保持较低,合理建议是
探究三、泡菜中
 含量的影响因素
含量的影响因素泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成的。蔬菜中含有的硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐【如亚硝酸钠(NaNO2)】能与胃酸(主要成分是盐酸)反应,产生亚硝酸(HNO2)和氯化物(如NaCl)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。

(6)亚硝酸钠与盐酸反应的基本类型是
(7)室温下,用芹菜制作的泡菜,最佳食用时间是______(填字母序号)。
| A.泡制2﹣3天 | B.泡制5﹣6天 | C.泡制12天后 |
(8)下列关于制作泡菜的说法中,合理的是______(填字母序号)。
| A.最好加入一些姜汁 |
| B.加适量水果 |
| C.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关 |
探究三、工业废水中的处理
(9)某工厂的金属切割加工废液中含有
 的
的 ,为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液(反应原理:
,为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液(反应原理: )。若工厂需处理
)。若工厂需处理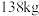 废液,计算最少需消耗
废液,计算最少需消耗 的质量
的质量
您最近一年使用:0次
2024九年级下·辽宁·专题练习
7 . CO2的制备及应用。
I、CO2制备
(1)某兴趣小组利用注射器进行如图所示探究。请回答相关问题。______ 。
②图丙:仪器a的名称是______ 。用手向左推动注射器活塞,若观察到______ ,则装置的气密性良好。
③实验室制备CO2时,选择丁装置的优点是______ 。
④实验室制备CO2的化学方程式是______ 。
(2)为得到干燥纯净的CO2,乙中产生的气体应依次通过分别盛有______ 、______ (填字母)的B、C装置。
Ⅱ、CO2应用
用CO2合成新型固体消毒剂过氧化尿素【CO(NH2)2·H2O2】的一种制备流程如下。______ 。
(4)过氧化尿素制备原理: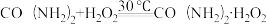
①反应釜中投放的质量比 需稍大于理论值,其主要原因是
需稍大于理论值,其主要原因是______ 。
②制得的过氧化尿素粗产品混有尿素。已知过氧化尿素在45℃以上不稳定。提纯该产品的操作步骤是溶解、______ 、冷却结晶、过滤、洗涤、低温干燥。
I、CO2制备
(1)某兴趣小组利用注射器进行如图所示探究。请回答相关问题。
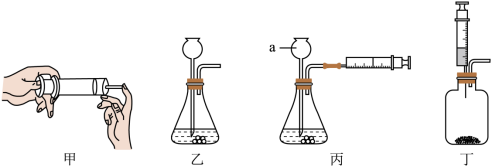
②图丙:仪器a的名称是
③实验室制备CO2时,选择丁装置的优点是
④实验室制备CO2的化学方程式是
(2)为得到干燥纯净的CO2,乙中产生的气体应依次通过分别盛有

Ⅱ、CO2应用
用CO2合成新型固体消毒剂过氧化尿素【CO(NH2)2·H2O2】的一种制备流程如下。
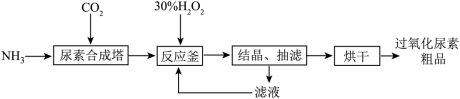
(4)过氧化尿素制备原理:
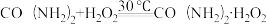
①反应釜中投放的质量比
 需稍大于理论值,其主要原因是
需稍大于理论值,其主要原因是②制得的过氧化尿素粗产品混有尿素。已知过氧化尿素在45℃以上不稳定。提纯该产品的操作步骤是溶解、
您最近一年使用:0次
2024九年级下·辽宁·专题练习
8 . 氢气燃烧热值高,约是煤的4倍,被视为理想的清洁燃料。我国氢能的利用还处于起步阶段,2022年中国各能源一次性消费占比如图1所示。
光解水:在太阳光驱动下催化水发生分解反应。虽然这项技术操作简单,能耗低,无二次污染,但因光腐蚀,能量转换效率低等问题,目前并未实际投入生产。研究发现使用氮化铟镓/氮化镓作为催化剂进行光解水可以提高制氢效率。不同温度下使用该催化剂分解水的速率如图2所示。
电解水:利用电能将水分解。海水中成分复杂,电解时易对电极等材料造成腐蚀或生成不需要的副产物。针对上述问题,我国科学家研制了全球首套海上制氢平台,该平台将海水中的水以水汽的形式跨膜转移,实现了海水中的杂质完全分离。分解海水所需电能完全来自风能和太阳能,向世界展示零碳能源的中国方案。
依据文章内容回答下列问题。
(1)由图1可知,2022年我国能源一次性消费占比最高的是______ 。
(2)光解水目前未实际投入生产,其原因是______ 。
(3)由图2可知,温度升高会加快使用氮化铟镓/氮化镓为催化剂进行光解水的反应速率,证据是______ 。
(4)电解水的化学方程式为______ 。
(5)判断下列说法是否正确(填“对”或“错”)。
①煤的热值没有氢气高______ 。
②电解海水时,海水中溶解的物质会对电极造成腐蚀。______ 。
(6)我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时,分解的微观过程用示意图表示如图:(“〇”表示氢原子,“●”表示氧原子,“ ” 表示催化剂)。
” 表示催化剂)。______ (填数字序号),上述过程中说明在化学变化中不能再分的粒子是______ 。
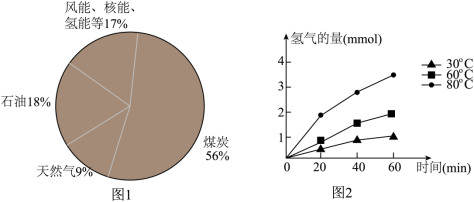
光解水:在太阳光驱动下催化水发生分解反应。虽然这项技术操作简单,能耗低,无二次污染,但因光腐蚀,能量转换效率低等问题,目前并未实际投入生产。研究发现使用氮化铟镓/氮化镓作为催化剂进行光解水可以提高制氢效率。不同温度下使用该催化剂分解水的速率如图2所示。
电解水:利用电能将水分解。海水中成分复杂,电解时易对电极等材料造成腐蚀或生成不需要的副产物。针对上述问题,我国科学家研制了全球首套海上制氢平台,该平台将海水中的水以水汽的形式跨膜转移,实现了海水中的杂质完全分离。分解海水所需电能完全来自风能和太阳能,向世界展示零碳能源的中国方案。
依据文章内容回答下列问题。
(1)由图1可知,2022年我国能源一次性消费占比最高的是
(2)光解水目前未实际投入生产,其原因是
(3)由图2可知,温度升高会加快使用氮化铟镓/氮化镓为催化剂进行光解水的反应速率,证据是
(4)电解水的化学方程式为
(5)判断下列说法是否正确(填“对”或“错”)。
①煤的热值没有氢气高
②电解海水时,海水中溶解的物质会对电极造成腐蚀。
(6)我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时,分解的微观过程用示意图表示如图:(“〇”表示氢原子,“●”表示氧原子,“
 ” 表示催化剂)。
” 表示催化剂)。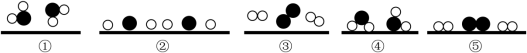
您最近一年使用:0次
2024九年级下·辽宁·专题练习
解题方法
9 . 下列实验设计不能 达到目的的是
|
|
|
|
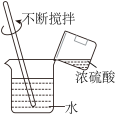
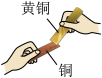
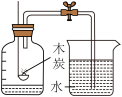
A.探究水的组成 | B.稀释浓硫酸 | C.比较黄铜和铜的硬度 | D.测定空气成分 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024九年级下·辽宁·专题练习
解题方法
10 . 在“粗盐中难溶性杂质的去除”实验中,下列操作中正确的是
A.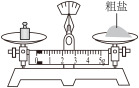 称量 称量 | B.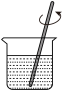 溶解 溶解 |
C.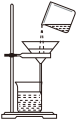 过滤 过滤 | D.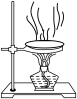 蒸发 蒸发 |
您最近一年使用:0次