1 . 下面是初中化学中常见的几个实验,请回答下列问题。______ ,根据该现象可知,二氧化碳具有______ 的性质。
(2)实验二中加热片刻后,可观察到棉球上蘸有的酒精燃烧,而棉球上蘸有的水不燃烧,由此可得出燃烧的条件之一是______ 。
(3)实验三是一组对比实验,一段时间后试管______ (选填“甲”或“乙”)中的铁钉会锈蚀,该实验说明铁生锈与______ 有关。

(2)实验二中加热片刻后,可观察到棉球上蘸有的酒精燃烧,而棉球上蘸有的水不燃烧,由此可得出燃烧的条件之一是
(3)实验三是一组对比实验,一段时间后试管
您最近一年使用:0次
2 . 为了证明NaOH能与CO2发生了反应,将两支充满CO2的相同试管分别倒扣在等体积的水和NaOH溶液中。乙中液面高于甲,说明NaOH与CO2发生了反应,该反应的化学方程式为_____ ,本实验中甲的作用是_____ 。

您最近一年使用:0次
解题方法
3 . 为比较 溶液和
溶液和 溶液对
溶液对 分解的催化效果,某研究小组进行了如下探究:
分解的催化效果,某研究小组进行了如下探究: 分解的催化效果,实验时对二者需要控制的变量是
分解的催化效果,实验时对二者需要控制的变量是______ 。如图甲,可通过观察______ 来定性比较两者的催化效果。写出 溶液用
溶液用 作催化剂分解的化学方程式
作催化剂分解的化学方程式______ 。
(2)如图乙,实验前检查该装置气密性的方法是______ 。定量比较两者的催化效果,可测量生成等体积气体所需的______ ;
(3)在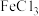 溶液中,究竟是哪种粒子起催化作用呢?
溶液中,究竟是哪种粒子起催化作用呢?
猜想1:铁离子;猜想2:______ ;猜想3:水分子。
小明同学认为可以排除猜想3,他这样认为的原因是______ 。
 溶液和
溶液和 溶液对
溶液对 分解的催化效果,某研究小组进行了如下探究:
分解的催化效果,某研究小组进行了如下探究:
 分解的催化效果,实验时对二者需要控制的变量是
分解的催化效果,实验时对二者需要控制的变量是 溶液用
溶液用 作催化剂分解的化学方程式
作催化剂分解的化学方程式(2)如图乙,实验前检查该装置气密性的方法是
(3)在
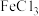 溶液中,究竟是哪种粒子起催化作用呢?
溶液中,究竟是哪种粒子起催化作用呢?猜想1:铁离子;猜想2:
小明同学认为可以排除猜想3,他这样认为的原因是
您最近一年使用:0次
名校
4 . 研究表明,Fe能够将烟气中的有害气体NO转化为N2,同时生成铁的氧化物。利用下图所示装置模拟烟气中NO的转化过程,探究影响NO脱出效果的因素。
【解释与结论】
(1)配平化学方程式:__________ 。
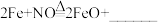 。
。
(2)①②③的目的是___________ 。
(3)由②⑤⑧可以得到的结论是___________ 。
(4)③中,若将铁丝网尺寸改为160mm×30mm,则NO脱出效率___________ (填“>”或“<”)60%。
(5)依据实验数据,得出NO脱出效率的最佳工业生产条件是___________。
【反思与评价】
(6)补做实验证明了铁丝直径对NO脱出效果也有影响。实验方案:750℃,采用铁丝网尺寸80mm×80mm,___________ 。

| 序号 | 铁丝网尺寸(长×宽)/mm2 | 温度/℃ | NO脱出效率/% |
| ① | 160×80 | 750 | 100 |
| ② | 80×80 | 750 | 80 |
| ③ | 160×40 | 750 | 60 |
| ④ | 160×80 | 850 | 100 |
| ⑤ | 80×80 | 850 | 90 |
| ⑥ | 160×40 | 850 | 85 |
| ⑦ | 160×80 | 950 | 100 |
| ⑧ | 80×80 | 950 | 95 |
| ⑨ | 160×40 | 950 | 94 |
(1)配平化学方程式:
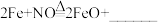 。
。(2)①②③的目的是
(3)由②⑤⑧可以得到的结论是
(4)③中,若将铁丝网尺寸改为160mm×30mm,则NO脱出效率
(5)依据实验数据,得出NO脱出效率的最佳工业生产条件是___________。
| A.铁丝网尺寸160mm×80mm,温度950℃ |
| B.铁丝网尺寸160mm×80mm,温度750℃ |
| C.铁丝网尺寸160mm×40mm,温度750℃ |
【反思与评价】
(6)补做实验证明了铁丝直径对NO脱出效果也有影响。实验方案:750℃,采用铁丝网尺寸80mm×80mm,
您最近一年使用:0次
2024-05-18更新
|
122次组卷
|
2卷引用:2024年北京市通州区九年级一模化学试卷
解题方法
5 . 某化学兴趣小组同学共同
探究如何对“木炭还原氧化铜”的实验进行改进。
任务一 按照教材中方法实验,探讨实验存在的不足
如图1所示组装仪器,加热5min 后,试管内开始有少量砖红色固体出现。
(1)木炭粉和氧化铜完全反应的化学方程式为__________ 。金属网罩的作用是__________ 。
(2)取3 次上述实验得到的红色固体,分别加入足量的稀硫酸,均观察到__________ 现象,说明实验中均生成了氧化亚铜。
任务二 探究影响木炭还原氧化铜实验效果的因素
【实验 I】如图2所示,将试管竖直放置,放入1.2 g 木炭及足量氧化铜进行实验。加热2min 后,试管内固体开始持续红热,澄清石灰水变浑浊,数秒后有光亮的红色块状金属生成。__________ 。相比较试管略倾斜横放的方式,竖直放置试管用时较短,现象明显,原因可能是__________ 。
【实验Ⅱ】用不同质量配比的木炭粉与氧化铜的混合物进行实验,实验现象如下表:
(4)实验Ⅱ中效果最理想的一组实验是__________ (填实验序号)。
(5)根据上述实验小组同学一致认为没有必要进行质量比为1:14的实验,理由是__________ 。第5次 实验中几乎没有黑色物质剩余,其原因可能是__________ 。澄清石灰水变浑浊__________ (填“能”或“不能”)作为木炭跟氧化铜开始反应的充分证据。
【实验Ⅲ】探究药品总量及试管大小对反应现象的影响。
(6)实验Ⅲ可得出的结论是:药品总量对反应现象有影响;通过对照__________ 两组实验,说明试管大小对实验现象无明显影响。
探究如何对“木炭还原氧化铜”的实验进行改进。
任务一 按照教材中方法实验,探讨实验存在的不足
如图1所示组装仪器,加热5min 后,试管内开始有少量砖红色固体出现。
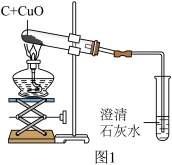
(1)木炭粉和氧化铜完全反应的化学方程式为
(2)取3 次上述实验得到的红色固体,分别加入足量的稀硫酸,均观察到
任务二 探究影响木炭还原氧化铜实验效果的因素
【实验 I】如图2所示,将试管竖直放置,放入1.2 g 木炭及足量氧化铜进行实验。加热2min 后,试管内固体开始持续红热,澄清石灰水变浑浊,数秒后有光亮的红色块状金属生成。

【实验Ⅱ】用不同质量配比的木炭粉与氧化铜的混合物进行实验,实验现象如下表:
| 实验序号 | 木炭粉与氧化铜的质量比 | 出现大量红色固体的时间 | 反应后物质的颜色、状态 | |
| 1 | 1:8 | 2´26 | 产生红色固体,有金属光泽 | 混有砖红色和黑色物质 |
| 2 | 1:9 | 2´05 | 铜块较小,有少量黑色物质 | |
| 3 | 1:10 | 1´44 | 铜块较小,有极少量黑色物质 | |
| 4 | 1:11 | 1´50 | 铜块较大,有极少量黑色物质 | |
| 5 | 1:12 | 1´55 | 铜块较大,几乎无黑色物质 | |
| 6 | 1:13 | 1´53 | 铜块较小,有较多黑色物质 | |
(4)实验Ⅱ中效果最理想的一组实验是
(5)根据上述实验小组同学一致认为没有必要进行质量比为1:14的实验,理由是
【实验Ⅲ】探究药品总量及试管大小对反应现象的影响。
| 实验序号 | 药品的总质量/g | 试管的尺寸/mm | 反应后物质的颜色、状态 | |
| 1 | 1.1 | 18×180 | 均有红色块状 | 有少量黑色物质 |
| 2 | 1.1 | 20×200 | 有少量黑色物质 | |
| 3 | 2.2 | 18×180 | 有较多黑色物质 | |
| 4 | 2.2 | 20×200 | 有较多黑色物质 | |
(6)实验Ⅲ可得出的结论是:药品总量对反应现象有影响;通过对照
您最近一年使用:0次
解题方法
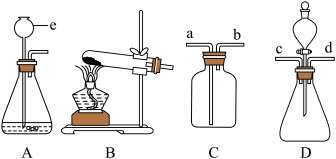
6 . 实验是学习化学的主要途径,下图是实验室制取常见气体及检验其相关性质的装置,根据图示回答下列问题。___________ ;
(2)实验室制取氧气可采取下列两种方案,药品如下:
方案一:氯酸钾和二氧化锰
方案二:过氧化氢溶液和二氧化锰
下列相关说法正确的是___________(填序号);
(3)老师给出了利用装置D来证明二氧化碳可与水发生反应的相关实验步骤:
①从d端通入氮气②从分液漏斗中加适量水③从c端通入二氧化碳
④将干燥的紫色石蕊小花放入D装置的瓶中。
请你确定正确的顺序___________ (填字母序号,可重复)来完成实验。
(2)实验室制取氧气可采取下列两种方案,药品如下:
方案一:氯酸钾和二氧化锰
方案二:过氧化氢溶液和二氧化锰
下列相关说法正确的是___________(填序号);
| A.方案一耗能更多,方案二更清洁环保 |
| B.两反应物能用于制取氧气的前提条件是都含有氧元素 |
| C.制取氧气时,氯酸钾比过氧化氢的氧元素利用率更高 |
(3)老师给出了利用装置D来证明二氧化碳可与水发生反应的相关实验步骤:
①从d端通入氮气②从分液漏斗中加适量水③从c端通入二氧化碳
④将干燥的紫色石蕊小花放入D装置的瓶中。
请你确定正确的顺序
您最近一年使用:0次
7 . 阅读下列短文,回答问题。
甲醛(HCHO)是主要的室内空气污染物之一,它是一种无色有刺激性气味、能溶于水的气体。室内甲醛主要来源于建筑材料、家具、各种黏合剂涂料和合成纺织品等。室内甲醛的释放量与温度、湿度和家具数量等有关。科研人员通过实验研究了室内甲醛的释放量与温度的关系,结果如图1。除开窗通风还可用活性炭或光触媒辅助去除室内甲醛。在紫外线照射下,光触媒催化甲醛与空气中氧气反应转化为 和
和 。相同条件下活性炭和光触媒去除室内甲醛的相关研究数据如图2(该实验在自然光照的密闭室内进行)。
。相同条件下活性炭和光触媒去除室内甲醛的相关研究数据如图2(该实验在自然光照的密闭室内进行)。
(2)写出在紫外线照射下,光触媒催化甲醛转化为二氧化碳和水的化学方程式______ 。
(3)由图1可知,在实验研究的温度范围内,其它条件相同时,室内甲醛的释放量与温度的关系是______ 。
(4)在光触媒的实验中,8~24小时和32~48小时两个时间段内,甲醛浓度均没有明显下降,可能原因是______ (写一点即可)。
甲醛(HCHO)是主要的室内空气污染物之一,它是一种无色有刺激性气味、能溶于水的气体。室内甲醛主要来源于建筑材料、家具、各种黏合剂涂料和合成纺织品等。室内甲醛的释放量与温度、湿度和家具数量等有关。科研人员通过实验研究了室内甲醛的释放量与温度的关系,结果如图1。除开窗通风还可用活性炭或光触媒辅助去除室内甲醛。在紫外线照射下,光触媒催化甲醛与空气中氧气反应转化为
 和
和 。相同条件下活性炭和光触媒去除室内甲醛的相关研究数据如图2(该实验在自然光照的密闭室内进行)。
。相同条件下活性炭和光触媒去除室内甲醛的相关研究数据如图2(该实验在自然光照的密闭室内进行)。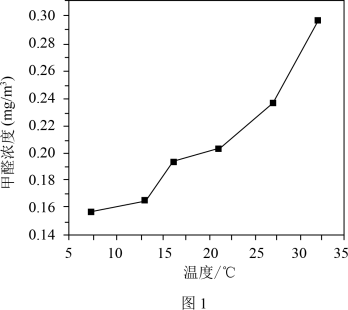

| A.甲醛属于氧化物 |
| B.“甲醛有刺激性气味”属于甲醛的化学性质 |
| C.活性炭能吸附甲醛,是因为活性炭具有疏松多孔结构 |
| D.由图2可知使用活性炭去除甲醛时,应增加活性炭的用量 |
(2)写出在紫外线照射下,光触媒催化甲醛转化为二氧化碳和水的化学方程式
(3)由图1可知,在实验研究的温度范围内,其它条件相同时,室内甲醛的释放量与温度的关系是
(4)在光触媒的实验中,8~24小时和32~48小时两个时间段内,甲醛浓度均没有明显下降,可能原因是
您最近一年使用:0次
名校
8 . 碱式碳酸铜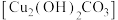 常用制造于烟火、颜料等。小组同学实验探究影响
常用制造于烟火、颜料等。小组同学实验探究影响 产率的因素。
产率的因素。
【资料】①产率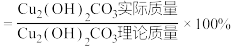
② 是绿色固体,难溶于水,酸性条件下不稳定。
是绿色固体,难溶于水,酸性条件下不稳定。
③制备原理: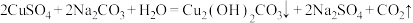 。
。
【进行实验】
取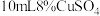 溶液,加入不同体积
溶液,加入不同体积 溶液,在不同温度下,反应一段时间,测定
溶液,在不同温度下,反应一段时间,测定 的产率。
的产率。
【解释与结论】
(1)反应完成后,将生成物进行______ (填操作名称)并洗涤、干燥、称重,计算产率。
(2)为了使生成的 稳定,实验过程中需保持反应体系的pH
稳定,实验过程中需保持反应体系的pH______ 7(填“>”或“<”)。
(3)实验①②③的目的是______ 。
(4)由实验④⑤⑥可得到的结论是______ 。
(5)由上述实验能得出反应时间与 产率的关系,依据的实验是
产率的关系,依据的实验是______ (填实验序号)。
【继续实验】
(6)补做实验,在上述实验最佳制备条件下,证明用 替代
替代 ,产率会更高。
,产率会更高。
实验方案:取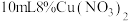 溶液,加入
溶液,加入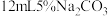 溶液,
溶液,______ 。
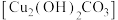 常用制造于烟火、颜料等。小组同学实验探究影响
常用制造于烟火、颜料等。小组同学实验探究影响 产率的因素。
产率的因素。【资料】①产率
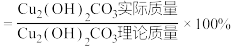
②
 是绿色固体,难溶于水,酸性条件下不稳定。
是绿色固体,难溶于水,酸性条件下不稳定。③制备原理:
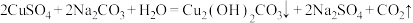 。
。【进行实验】
取
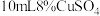 溶液,加入不同体积
溶液,加入不同体积 溶液,在不同温度下,反应一段时间,测定
溶液,在不同温度下,反应一段时间,测定 的产率。
的产率。【解释与结论】
| 序号 | 温度/℃ | Na2CO3溶液体积/mL | 反应时间/min | 产率/% |
| ① | 20 | 8 | 1 | 63.5 |
| ② | 20 | 10 | 1 | 69.1 |
| ③ | 20 | 12 | 1 | 73.3 |
| ④ | 20 | 12 | 3 | 74.6 |
| ⑤ | 40 | 12 | 3 | 80.3 |
| ⑥ | 60 | 12 | 3 | 86.8 |
| ⑦ | 60 | 12 | 1 | 74.3 |
| ⑧ | 60 | 12 | 2 | 79.6 |
| ⑨ | 60 | 12 | 4 | 90.4 |
(2)为了使生成的
 稳定,实验过程中需保持反应体系的pH
稳定,实验过程中需保持反应体系的pH(3)实验①②③的目的是
(4)由实验④⑤⑥可得到的结论是
(5)由上述实验能得出反应时间与
 产率的关系,依据的实验是
产率的关系,依据的实验是【继续实验】
(6)补做实验,在上述实验最佳制备条件下,证明用
 替代
替代 ,产率会更高。
,产率会更高。实验方案:取
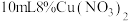 溶液,加入
溶液,加入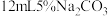 溶液,
溶液,
您最近一年使用:0次
9 . 阅读科普短文,回答下列问题。
生物质是指利用大气、水、土地等通过光合作用而产生的各种有机体,即一切有生命的可以生长的有机物质通称为生物质。它包括所有的植物、微生物以及以植物、微生物为食物的动物及其生产的废弃物,可再生、低污染、分布广泛。
生物质能是贮存在生物质中的能量,是人类历史上最早使用的能源,属可再生能源。据计算,生物质储存的能量比世界能源消费总量大2倍。现代较为有效地利用生物质能的方式有:将秸秆粉碎、添加乳酸菌发酵,即可做成牲畜饲料;以秸秆为主要原料,经粉碎、厌氧发酵即可生产沼气;利用秸秆和畜禽粪便为原料,经无害化处理、发酵腐熟就可制成有机肥料;秸秆经粉碎、水解、糖化发酵、蒸馏等过程,可获得燃料酒精。
目前,生物质能已成为世界第四大能源。它燃烧后灰渣极少,且燃烧后的灰烬是品位极高的优质有机钾肥,是一种清洁能源。生物柴油是生物质燃料的一种,但在其生产过程中,副产物甘油(C6H8O3)产生的环境污染制约了其产业发展,处理方法之一为光催化重整法。该方法是在常温常压和太阳光的驱动下,利用催化剂处理甘油产生氢气。二氧化钛(TiO2)由于具有安全、无生物毒性、耐腐蚀、廉价、可重复利用等优点,已成为甘油处理最常用的催化剂之一。为了提高催化效果,常将TiO2与其他物质相结合形成复合催化剂。其他条件相同时,几种催化剂的催化效果如图所示。____________ ,属于________ (填“有机物”或“无机物”)。
(2)酒精充分燃烧的化学方程式为_________________________ ,若充分燃烧后产生二氧化碳的质量为13.2g,则消耗酒精的质量为____________ 。
(3)文中提到的现代有效利用生物质能的方式有____________ 种。每种方式都涉及到的一个化学变化过程是____________ 。
(4)下列有关生物质能的说法正确的是 。
(5)甘油处理最常用的催化剂之一是二氧化钛,因为___________ (写出两点即可)。
(6)由图示可知,在生产时间相同时,影响氢气产量的因素为______________ ;通过对比图中信息,还可以得到的结论是____________________ 。
生物质是指利用大气、水、土地等通过光合作用而产生的各种有机体,即一切有生命的可以生长的有机物质通称为生物质。它包括所有的植物、微生物以及以植物、微生物为食物的动物及其生产的废弃物,可再生、低污染、分布广泛。
生物质能是贮存在生物质中的能量,是人类历史上最早使用的能源,属可再生能源。据计算,生物质储存的能量比世界能源消费总量大2倍。现代较为有效地利用生物质能的方式有:将秸秆粉碎、添加乳酸菌发酵,即可做成牲畜饲料;以秸秆为主要原料,经粉碎、厌氧发酵即可生产沼气;利用秸秆和畜禽粪便为原料,经无害化处理、发酵腐熟就可制成有机肥料;秸秆经粉碎、水解、糖化发酵、蒸馏等过程,可获得燃料酒精。
目前,生物质能已成为世界第四大能源。它燃烧后灰渣极少,且燃烧后的灰烬是品位极高的优质有机钾肥,是一种清洁能源。生物柴油是生物质燃料的一种,但在其生产过程中,副产物甘油(C6H8O3)产生的环境污染制约了其产业发展,处理方法之一为光催化重整法。该方法是在常温常压和太阳光的驱动下,利用催化剂处理甘油产生氢气。二氧化钛(TiO2)由于具有安全、无生物毒性、耐腐蚀、廉价、可重复利用等优点,已成为甘油处理最常用的催化剂之一。为了提高催化效果,常将TiO2与其他物质相结合形成复合催化剂。其他条件相同时,几种催化剂的催化效果如图所示。

(2)酒精充分燃烧的化学方程式为
(3)文中提到的现代有效利用生物质能的方式有
(4)下列有关生物质能的说法正确的是 。
| A.生物质能虽然储量丰富,但是不可再生,要节约使用。 |
| B.生物质燃料燃烧后的灰烬能为农作物提供营养元素,是优质肥料。 |
| C.生物柴油是生物质燃料的一种,其生产和使用都不会产生污染。 |
| D.为了提高催化效果,常将TiO2与其他物质相结合形成复合催化剂。 |
(5)甘油处理最常用的催化剂之一是二氧化钛,因为
(6)由图示可知,在生产时间相同时,影响氢气产量的因素为
您最近一年使用:0次
10 . 古籍记载:“夫土壤之性,有酸碱之异。……知土壤之性,择地而耕,方能得谷之丰收。”某化学社团开展土壤酸碱性对农作物生长影响的实践活动,帮助农场优化农作物种植。
任务一:知土壤之性
【查阅资料】
(1)该地区85%农用地呈酸性,即pH____ 7(填“>”、“<”“=”)。
【实验研究】
小组分工合作,测定农场内不同区域土壤酸碱性。分别取不同样品各10g溶于25mL蒸馏水中,充分搅拌,过滤得溶液,用pH计测样品pH如表1。
表1.常温(25℃)下各样品pH
【结论分析】
(2)对比样品编号1-1、1-2组及2-1、2-2组的结果,得出的结论是_____ 。
(3)能说明交通因素对土壤pH有影响的一组样品编号为_____ (任选一组)。
【实验反思】
样品编号2-3测定结果异常。小组同学认为,溶解样品所用蒸馏水没有经煮沸冷却处理,导致结果偏低。
任务二:择地而耕
(4)结合表2分析,种植马铃薯适合在_____ 任选一种表1中测定结果无异常耕地类型)。
表2.蔬菜生长适宜的土壤pH范围
任务一:知土壤之性
【查阅资料】
(1)该地区85%农用地呈酸性,即pH
【实验研究】
小组分工合作,测定农场内不同区域土壤酸碱性。分别取不同样品各10g溶于25mL蒸馏水中,充分搅拌,过滤得溶液,用pH计测样品pH如表1。
表1.常温(25℃)下各样品pH
| 样品编号 | 采样地点 | 采样深度(cm) | pH |
| 1-1 | 耕地(靠近交通区域) | 5 | 5.24 |
| 1-2 | 10 | 3.13 | |
| 1-3 | 耕地(远离交通区域) | 5 | 5.53 |
| 1-4 | 10 | 5.44 | |
| 2-1 | 景观园林地(靠近交通区域) | 5 | 5.68 |
| 2-2 | 10 | 5.46 | |
| 2-3 | 景观园林地(远离交通区域) | 5 | 6.08 |
| 2-4 | 10 | 6.08 |
(2)对比样品编号1-1、1-2组及2-1、2-2组的结果,得出的结论是
(3)能说明交通因素对土壤pH有影响的一组样品编号为
【实验反思】
样品编号2-3测定结果异常。小组同学认为,溶解样品所用蒸馏水没有经煮沸冷却处理,导致结果偏低。
任务二:择地而耕
(4)结合表2分析,种植马铃薯适合在
表2.蔬菜生长适宜的土壤pH范围
| 蔬菜 | 萝卜 | 辣椒 | 马铃薯 |
| pH | 5.3~7.0 | 6.2~7.2 | 5.5~6.5 |
您最近一年使用:0次



