解题方法
1 . 碳酸锂( )是制备锂电池的重要原料。工业上用锂辉石精矿(主要成分为
)是制备锂电池的重要原料。工业上用锂辉石精矿(主要成分为 ,其余成分不溶于水,也不参与反应)为原料制备
,其余成分不溶于水,也不参与反应)为原料制备 的流程如下:
的流程如下:________ 。
(2)酸浸槽中发生反应的化学方程式为________ 。
(3)为了探究酸浸槽中的最佳条件,做了4组实验,酸浸时间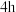 ,其余相关数据见表。
,其余相关数据见表。
①能说明温度对锂元素的浸出率有影响的实验组别是________ 。
②根据A组和B组实验对比,得出硫酸浓度对锂元素浸出率的影响是:________ 。
(4)反应器中加入过量饱和 溶液,除了将
溶液,除了将 全部转化成
全部转化成 提高产率外,还起到
提高产率外,还起到________ 的作用。
(5)根据 的溶解度曲线图(见图),推测洗涤槽中采用的试剂是
的溶解度曲线图(见图),推测洗涤槽中采用的试剂是________ (填“冰水”或“热水”)。
 )是制备锂电池的重要原料。工业上用锂辉石精矿(主要成分为
)是制备锂电池的重要原料。工业上用锂辉石精矿(主要成分为 ,其余成分不溶于水,也不参与反应)为原料制备
,其余成分不溶于水,也不参与反应)为原料制备 的流程如下:
的流程如下: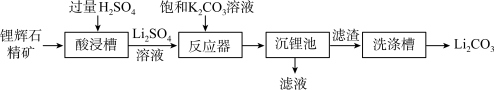
(2)酸浸槽中发生反应的化学方程式为
(3)为了探究酸浸槽中的最佳条件,做了4组实验,酸浸时间
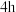 ,其余相关数据见表。
,其余相关数据见表。| 组别 | 矿酸比 | 硫酸浓度(%) | 温度(℃) | 锂元素浸出率(%) |
| A | 1:1 | 90 | 100 | 70.34 |
| B | 1:1 | 98 | 100 | 73.89 |
| C | 1:1 | 98 | 150 | 78.24 |
| D | 1:3 | 98 | 200 | 85.53 |
②根据A组和B组实验对比,得出硫酸浓度对锂元素浸出率的影响是:
(4)反应器中加入过量饱和
 溶液,除了将
溶液,除了将 全部转化成
全部转化成 提高产率外,还起到
提高产率外,还起到(5)根据
 的溶解度曲线图(见图),推测洗涤槽中采用的试剂是
的溶解度曲线图(见图),推测洗涤槽中采用的试剂是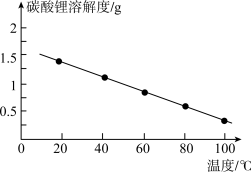
您最近一年使用:0次
2 . 次氯酸钠溶液是一种广泛应用的消毒剂,但由于其易自然分解,不宜长时间存储。某化学小组同学欲通过实验探究影响次氯酸钠稳定性的因素。
【查阅资料】
1.次氯酸钠溶液是一种呈微黄色,有类似氯气的刺激性气味,稳定性差于氯气,见光易分解、易挥发的液体。
2.次氯酸钠的稳定性可以通过测量有效氯的衰减速率来进行比较,相同时间内,次氯酸钠溶液的衰减量越大,衰减速率越快,次氯酸钠的稳定性就越差。
【进行实验】
将3种不同质量分数的次氯酸钠溶液放置在正常光线、温度一定的房间内,研究周期为30天,测量次氯酸钠溶液的有效氯的衰减量,将实验结果记录于表格。
【解释与结论】
(1)次氯酸钠的化学式为NaClO,其中氯元素的化合价为_______ 。
(2)根据实验分析,实验5中,a应为_______ 。
(3)由实验①②③可以得到的结论是_______ 。
(4)若要探究次氯酸钠溶液的质量分数对次氯酸钠稳定性的影响,应选择的实验是_______ (写实验序号)。
(5)根据实验数据可知,储备次氯酸钠溶液最好选择的质量分数和储备温度是_______ 。
(6)对次氯酸钠溶液的日常保存,提出你的一些建议。_______ 。
【继续实验】
(7)补做实验:证明储存时间对次氯酸钠溶液有效氯的衰减量有影响。实验方案:将一份质量分数为10%的次氯酸钠溶液放置在正常光线,_______ 。
【查阅资料】
1.次氯酸钠溶液是一种呈微黄色,有类似氯气的刺激性气味,稳定性差于氯气,见光易分解、易挥发的液体。
2.次氯酸钠的稳定性可以通过测量有效氯的衰减速率来进行比较,相同时间内,次氯酸钠溶液的衰减量越大,衰减速率越快,次氯酸钠的稳定性就越差。
【进行实验】
将3种不同质量分数的次氯酸钠溶液放置在正常光线、温度一定的房间内,研究周期为30天,测量次氯酸钠溶液的有效氯的衰减量,将实验结果记录于表格。
| 实验序号 | 次氯酸钠溶液的质量分数/% | 温度/℃ | 有效氯的衰减量/% |
① | 10 | 16-18 | 7.0 |
② | 20-22 | 9.0 | |
③ | 25-28 | 15.0 | |
④ | 7 | 16-18 | 3.5 |
⑤ | a | 4.0 | |
⑥ | 25-28 | 11.0 | |
⑦ | 5 | 16-18 | 1.9 |
⑧ | 20-22 | 2.0 | |
⑨ | 25-28 | 3.5 |
(1)次氯酸钠的化学式为NaClO,其中氯元素的化合价为
(2)根据实验分析,实验5中,a应为
(3)由实验①②③可以得到的结论是
(4)若要探究次氯酸钠溶液的质量分数对次氯酸钠稳定性的影响,应选择的实验是
(5)根据实验数据可知,储备次氯酸钠溶液最好选择的质量分数和储备温度是
(6)对次氯酸钠溶液的日常保存,提出你的一些建议。
【继续实验】
(7)补做实验:证明储存时间对次氯酸钠溶液有效氯的衰减量有影响。实验方案:将一份质量分数为10%的次氯酸钠溶液放置在正常光线,
您最近一年使用:0次
3 . 絮凝剂常用于污水处理。聚合硫酸铁(PFS)溶于水后形成多种络合物,使水中的悬浮物聚集,在重力作用下沉降。实验小组探究PFS对悬浮物的净化效果。
【进行实验】取200 mL浑浊程度相同的水样于烧杯中,调节水样pH,加入PFS,使水样中PFS达到一定浓度,搅拌,静置一段时间后,测定浊度去除率(浊度去除率越高,净化效果越好)。结果如下表:
【解释与结论】
(1)硫酸铁是制备PFS的重要原料。补全制备硫酸铁的化学方程式:NaClO3+6FeSO4+3H2SO4=NaCl+3Fe2(SO4)3+_____ H2O。
(2)探究水样中PFS浓度对悬浮物的净化效果影响的实验是_____ (填序号)。
(3)③比④浊度去除率低的原因是_____ 。
(4)由⑤⑦⑧得到的结论是_____ 。
(5)PFS对悬浮物净化效果最佳的实验条件是_____ 。
【反思与评价】
(6)明矾也是常用的絮凝剂。继续实验,发现相同条件下明矾对水中悬浮物的净化效果比PFS差,其实验方案是:取200 mL浑浊程度相同的水样于烧杯中,_____ 。
【进行实验】取200 mL浑浊程度相同的水样于烧杯中,调节水样pH,加入PFS,使水样中PFS达到一定浓度,搅拌,静置一段时间后,测定浊度去除率(浊度去除率越高,净化效果越好)。结果如下表:
| 序号 | 水样pH | 水样中PFS浓度(mg·L-1) | 静置时间(min) | 浊度去除率(%) |
| ① | 7.57 | 50 | 20 | 90.83 |
| ② | 7.57 | 75 | 20 | 96.95 |
| ③ | 7.57 | 100 | 10 | 88.15 |
| ④ | 7.57 | 100 | 15 | 91.14 |
| ⑤ | 7.57 | 100 | 20 | 93.17 |
| ⑥ | 7.57 | 125 | 20 | 84.52 |
| ⑦ | 6.14 | 100 | 20 | 79.72 |
| ⑧ | 9.01 | 100 | 20 | 83.26 |
(1)硫酸铁是制备PFS的重要原料。补全制备硫酸铁的化学方程式:NaClO3+6FeSO4+3H2SO4=NaCl+3Fe2(SO4)3+
(2)探究水样中PFS浓度对悬浮物的净化效果影响的实验是
(3)③比④浊度去除率低的原因是
(4)由⑤⑦⑧得到的结论是
(5)PFS对悬浮物净化效果最佳的实验条件是
【反思与评价】
(6)明矾也是常用的絮凝剂。继续实验,发现相同条件下明矾对水中悬浮物的净化效果比PFS差,其实验方案是:取200 mL浑浊程度相同的水样于烧杯中,
您最近一年使用:0次
4 . 花青素具有显著的抗氧化功能,广泛存在于植物中、实验小组对紫薯中的花青素展开了研究。
【查阅资料】
①紫薯中的花青素随溶液pH变化,会呈现不同的颜色:
②烫漂是加工紫薯粉的方法之一。花青素保留率越高,加工效果越好。
③花青素保留率越高,说明其在该条件下的稳定性越好。
【进行实验】
实验1:测定溶液的酸碱性。
实验2:探究一定条件下,烫漂加工紫薯粉过程中花青素稳定性的影响因素。实验数据如下表:
实验3:探究一定条件下,pH对花青素稳定性的影响。实验结果如下图:
(1)实验1的结论是______ 。
(2)实验2:
①a=______ 。
②ADE的目的是______ 。
③由BCD可以得到的结论是______ 。
(3)实验3的数据可作为pH越大,花青素的稳定性越差的证据,理由是______ 。
【反思与评价】
(4)结合实验2和实验3,烫漂加工紫薯粉的最佳实验条件为______ 。
【查阅资料】
①紫薯中的花青素随溶液pH变化,会呈现不同的颜色:
| pH值 | 1~4 | 5~7 | 8~10 | 11 | 12 | 13 |
| 颜色 | 洋红色 | 淡洋红色 | 淡紫色 | 蓝色 | 蓝黄色 | 土黄色 |
③花青素保留率越高,说明其在该条件下的稳定性越好。
【进行实验】
实验1:测定溶液的酸碱性。
| 实验操作 | 实验现象 | 实验结论 |
| 向试管中加入少量纯碱溶液,滴加2滴紫薯汁。 | 溶液变为蓝色 | ______ |
| 实验序号 | 烫漂温度/℃ | 烫漂时间/min | 成品花青素保留率/% |
| A | 65 | a | 2.95 |
| B | 75 | 1 | 6.49 |
| C | 75 | 3 | 10.39 |
| D | 75 | 5 | 12.01 |
| E | 100 | 5 | 42.86 |

(1)实验1的结论是
(2)实验2:
①a=
②ADE的目的是
③由BCD可以得到的结论是
(3)实验3的数据可作为pH越大,花青素的稳定性越差的证据,理由是
【反思与评价】
(4)结合实验2和实验3,烫漂加工紫薯粉的最佳实验条件为
您最近一年使用:0次
解题方法
5 . 化学小组在“设计和制作简易供氧器”的实践活动中,探究影响供氧剂过碳酸钠产氧速率的因素。
【查阅资料】
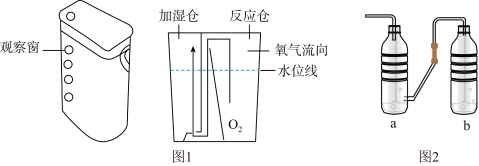
Ⅰ. 化学小组研究了图1所示的某品牌制氧机的装置原理后,利用身边物品自制了如图2所示的简易供氧器。
实验1:探究药品用量、温度对产氧速率的影响
【进行实验】在不同温度下,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入相同体积的水,测得平均产氧速率数据如下表所示。
实验2:探究加水量对产氧速率的影响
【进行实验】20℃时,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入不同体积的水,测得平均产氧速率及反应过程中温度变化数据如下表所示。
【解释与结论】
(1)实验中,过氧化氢分解生成氧气的化学方程式为_______ 。
(2)设计实验①②的目的是_______ 。
(3)由①③可以得到的结论是_______ 。
(4)⑤中x应为_______ 。
(5)依据实验2可知,该制氧过程中发生的化学反应属于_______ (填“吸热”或“放热”)反应。
【反思与评价】
(6)由上述实验可知,适当增加加水量可减缓产氧速率,其证据是_______ 。
(7)某同学欲进一步探究MnO2质量对产氧速率有影响,设计的实验方案是:20℃时,_______ 。
【查阅资料】
Ⅰ. 化学小组研究了图1所示的某品牌制氧机的装置原理后,利用身边物品自制了如图2所示的简易供氧器。
实验1:探究药品用量、温度对产氧速率的影响
【进行实验】在不同温度下,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入相同体积的水,测得平均产氧速率数据如下表所示。
| 序号 | 过碳酸钠质量/g | MnO2质量/g | 温度/℃ | 平均产氧速率mL/s |
| ① | 10 | 0.3 | 26 | 2.73 |
| ② | 20 | 0.3 | 26 | 8.56 |
| ③ | 10 | 0.3 | 41 | 4.54 |
【进行实验】20℃时,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入不同体积的水,测得平均产氧速率及反应过程中温度变化数据如下表所示。
| 序号 | 过碳酸钠质量/g | MnO2质量/g | 加水体积/mL | 反应液最高温度/℃ | 平均产氧速率mL/s |
| ④ | 240 | 2.5 | 350 | 98 | 33.3 |
| ⑤ | x | 2.5 | 500 | 74 | 15 |
| ⑥ | 240 | 2.5 | 800 | 53 | 10 |
(1)实验中,过氧化氢分解生成氧气的化学方程式为
(2)设计实验①②的目的是
(3)由①③可以得到的结论是
(4)⑤中x应为
(5)依据实验2可知,该制氧过程中发生的化学反应属于
【反思与评价】
(6)由上述实验可知,适当增加加水量可减缓产氧速率,其证据是
(7)某同学欲进一步探究MnO2质量对产氧速率有影响,设计的实验方案是:20℃时,
您最近一年使用:0次
6 . 下图“黑面包”实验中,加入浓硫酸和水时,绵白糖变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。小组同学实验探究影响实验效果的因素。
Ⅰ.绵白糖的主要成分是蔗糖。
Ⅱ.实验中涉及的化学反应有:
①蔗糖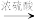 碳+水
碳+水
②C + 2H2SO4 CO2↑+ 2SO2↑+ 2H2O
CO2↑+ 2SO2↑+ 2H2O
③2KMnO4 + 3SO2 + 2H2O=K2SO4 + 2MnO2↓+ 2H2SO4
【进行实验】在100 mL烧杯中进行实验,实验数据记录如下:
说明:用产物高度简单衡量实验效果,高度越高,实验效果越好。
【解释与结论】
(1)绵白糖中一定含有的元素有______ 。
(2)0.5%高锰酸钾溶液的作用是______ 。
(3)根据实验数据推断,在100 mL烧杯中,使用10 g绵白糖进行实验,选择最佳的浓硫酸体积和水的滴数分别是______ 。
(4)实验①~⑤的目的是______ 。
(5)不能得出“绵白糖质量、浓硫酸体积等条件相同时,水滴数越多,效果越好”的结论,依据的实验是______ (填序号)。
【反思与评价】
(6)为进一步证明“烧杯的体积小,实验效果更明显”的结论,需要补做实验:在50 mL和250 mL烧杯中分别加入10 g绵白糖、5 mL浓硫酸、10滴水。下列现象属于50 mL烧杯中的是______(填序号)。

Ⅰ.绵白糖的主要成分是蔗糖。
Ⅱ.实验中涉及的化学反应有:
①蔗糖
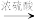 碳+水
碳+水②C + 2H2SO4
 CO2↑+ 2SO2↑+ 2H2O
CO2↑+ 2SO2↑+ 2H2O③2KMnO4 + 3SO2 + 2H2O=K2SO4 + 2MnO2↓+ 2H2SO4
【进行实验】在100 mL烧杯中进行实验,实验数据记录如下:
| 实验 | 绵白糖质量/g | 浓硫酸体积/mL | 水滴数 | 产物高度/cm |
| ① | 10 | 5 | 10 | 4.5 |
| ② | 20 | 5 | 10 | 6.8 |
| ③ | 30 | 5 | 10 | 10.0 |
| ④ | 35 | 5 | 10 | 11.5 |
| ⑤ | 40 | 5 | 10 | 11.5 |
| ⑥ | 10 | 10 | 10 | 9.0 |
| ⑦ | 10 | 15 | 10 | 7.0 |
| ⑧ | 10 | 5 | 20 | 8.0 |
| ⑨ | 10 | 5 | 30 | 6.2 |
| ⑩ | 10 | 5 | 40 | 5.0 |
【解释与结论】
(1)绵白糖中一定含有的元素有
(2)0.5%高锰酸钾溶液的作用是
(3)根据实验数据推断,在100 mL烧杯中,使用10 g绵白糖进行实验,选择最佳的浓硫酸体积和水的滴数分别是
(4)实验①~⑤的目的是
(5)不能得出“绵白糖质量、浓硫酸体积等条件相同时,水滴数越多,效果越好”的结论,依据的实验是
【反思与评价】
(6)为进一步证明“烧杯的体积小,实验效果更明显”的结论,需要补做实验:在50 mL和250 mL烧杯中分别加入10 g绵白糖、5 mL浓硫酸、10滴水。下列现象属于50 mL烧杯中的是______(填序号)。
| A.放出热量 | B.有刺激性气味 | C.产物高度2.3 cm | D.产物高度7.5 cm |
您最近一年使用:0次
7 . 兴趣小组同学对影响“化学小火箭”发射效果的因素进行探究。
制作并发射“化学小火箭”:常温下,取一定质量的试剂A装填于基座。取一定质量的试剂B装填于箭体,向箭体加入一定质量的水(20℃)后振荡,将箭体迅速扣在基座上。
第1组实验
第2组实验
【解释与结论】
(1)柠檬酸能与小苏打发生反应,配平其反应的化学方程式:______ 。
1C6H8O7+NaHCO3═1C6H5O7Na3+CO2↑+3H2O
(2)“化学小火箭”能发射的原因是______ 。
(3)下列变量中,属于第1组实验控制的变量的是______(填序号)。
(4)第2组实验的目的:探究小苏打装填于基座,柠檬酸装填于箭体,______ 。
(5)其他条件相同时,柠檬酸装填于箭体比装填于基座的发射效果_______ (填“好”“差”或“一样”)。
【反思与评价】
(6)补做实验证明了水的温度对“化学小火箭”的发射效果也有影响。实验方案:常温下,取1.5g小苏打装填于基座,______ 。
(7)除了利用柠檬酸和小苏打反应发射“化学小火箭”,还可选用的其他物质是______ (写出1组即可)。
制作并发射“化学小火箭”:常温下,取一定质量的试剂A装填于基座。取一定质量的试剂B装填于箭体,向箭体加入一定质量的水(20℃)后振荡,将箭体迅速扣在基座上。

第1组实验
| 序号 | ① | ② | ③ | ④ | ⑤ | |
| 基座 | 柠檬酸/g | 0.5 | 1 | 1.5 | 2 | 2.5 |
| 箭体 | 小苏打/g | 2.5 | 2 | 1.5 | 1 | 0.5 |
| 水/g | 17 | 17 | 17 | 17 | 17 | |
| 发射高度/m | 0.33 | 0.42 | 2.70 | 2.21 | 0.88 | |
| 序号 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 基座 | 小苏打/g | 2.5 | 2 | 1.5 | 1 | 0.5 |
| 箭体 | 柠檬酸/g | 0.5 | 1 | 1.5 | 2 | 2.5 |
| 水/g | 17 | 17 | 17 | 17 | 17 | |
| 发射高度/m | 0.46 | 0.96 | 3.26 | 2.67 | 1.15 | |
(1)柠檬酸能与小苏打发生反应,配平其反应的化学方程式:
1C6H8O7+NaHCO3═1C6H5O7Na3+CO2↑+3H2O
(2)“化学小火箭”能发射的原因是
(3)下列变量中,属于第1组实验控制的变量的是______(填序号)。
| A.发射高度 |
| B.柠檬酸和小苏打的质量和 |
| C.水的温度和质量 |
| D.柠檬酸与小苏打的质量比 |
| E.试剂的装填位置 |
(4)第2组实验的目的:探究小苏打装填于基座,柠檬酸装填于箭体,
(5)其他条件相同时,柠檬酸装填于箭体比装填于基座的发射效果
【反思与评价】
(6)补做实验证明了水的温度对“化学小火箭”的发射效果也有影响。实验方案:常温下,取1.5g小苏打装填于基座,
(7)除了利用柠檬酸和小苏打反应发射“化学小火箭”,还可选用的其他物质是
您最近一年使用:0次
8 . 高锰酸钾沾到白色的实验服上,会出现棕褐色的污渍,难以清洗。某学习小组经查阅资料了解到可用草酸溶液(添加少量稀硫酸)进行清洗,于是设计了如下实验,对去除棕褐色污渍反应速率的影响因素进行了探究。
【进行实验】将均匀染上棕褐色污渍的布条平均分为5份后进行实验,实验数据如下表:
(实验中使用的水、草酸溶液、硫酸溶液的密度均视为1 g/mL)
说明:本实验中,溶液总体积可看作是各液体的体积之和。
【解释与结论】
(1)配制草酸溶液的操作如下图所示。_______ ;正确的操作顺序是_______ (填序号)。
(2)①②③的目的是_______ 。
(3)③④⑤可以得出的结论是_______ 。
(4)①中,若将草酸溶液体积改为5ml,则布条褪色所用时间_______ (填“>”或“<”)189s。
(5)补做实验探究0.5%硫酸溶液的用量是否会影响反应速率。实验方案如下:20℃时,用2%的草酸溶液60ml、_______ 配制成洗涤试剂,清洗污渍程度相同的布条,记录布条褪色时间。
【进行实验】将均匀染上棕褐色污渍的布条平均分为5份后进行实验,实验数据如下表:
(实验中使用的水、草酸溶液、硫酸溶液的密度均视为1 g/mL)
| 实验 编号 | 温度 | 洗涤试剂及用量/mL | 布条褪色 所用时间/s | ||
| 水 | 2%草酸溶液 | 0.5%硫酸溶液 | |||
| ① | 20℃ | 109 | 10 | 1 | 189 |
| ② | 20℃ | 89 | 30 | 1 | 158 |
| ③ | 20℃ | 59 | 60 | 1 | 120 |
| ④ | 30℃ | 59 | 60 | 1 | 95 |
| ⑤ | 40℃ | 59 | 60 | 1 | 80 |
【解释与结论】
(1)配制草酸溶液的操作如下图所示。

(2)①②③的目的是
(3)③④⑤可以得出的结论是
(4)①中,若将草酸溶液体积改为5ml,则布条褪色所用时间
(5)补做实验探究0.5%硫酸溶液的用量是否会影响反应速率。实验方案如下:20℃时,用2%的草酸溶液60ml、
您最近一年使用:0次
9 . 羊毛衫具有良好的保暖性和舒适性,超临界CO2扎染技术可用于羊毛衫扎染。实验小组对超临界CO2扎染技术中羊毛衫染色效果的影响因素进行了探究。
【进行实验】
按照设计图案对羊毛衫进行捆扎,放入染色釜、在超临界CO2的作用下注入染料,在不同的条件下完成扎染过程,测试染色后的羊毛衫色差。实验数据记录如下:
注:色差值越大,表示超临界CO2扎染技术中羊毛衫染色效果越好。
【解释与结论】
(1)CO2中碳、氧元素的质量比为_______ 。
(2)①②③的目的是_______ 。
(3)①中,若将扎染温度改为60℃,则色差值_______ (填“>”“<”或“=”)23。
(4)由③④⑤得出的结论是_______ 。
(5)探究染料用量对羊毛衫染色效果的影响,需要对比的实验是_______ (填序号)。
【反思与评价】
(6)继续实验,发现“扎染时间对羊毛衫染色效果有很大影响”,其实验方案为:按照设计图案对羊毛衫进行捆扎,放入染色釜,在超临界CO2的作用下注入染料,_______ 。
【进行实验】
按照设计图案对羊毛衫进行捆扎,放入染色釜、在超临界CO2的作用下注入染料,在不同的条件下完成扎染过程,测试染色后的羊毛衫色差。实验数据记录如下:
| 实验序号 | 扎染温度/℃ | 扎染压力/MPa | 扎染时间/min | 染料用量/% | 色差值 |
| ① | 80 | 20 | 60 | 6 | 23 |
| ② | 90 | 20 | 60 | 6 | 28 |
| ③ | 100 | 20 | 60 | 6 | 42 |
| ④ | 100 | 10 | 60 | 6 | 18 |
| ⑤ | 100 | 15 | 60 | 6 | 28 |
| ⑥ | 100 | 20 | 60 | 2 | 36 |
| ⑦ | 100 | 20 | 60 | 4 | 38 |
【解释与结论】
(1)CO2中碳、氧元素的质量比为
(2)①②③的目的是
(3)①中,若将扎染温度改为60℃,则色差值
(4)由③④⑤得出的结论是
(5)探究染料用量对羊毛衫染色效果的影响,需要对比的实验是
【反思与评价】
(6)继续实验,发现“扎染时间对羊毛衫染色效果有很大影响”,其实验方案为:按照设计图案对羊毛衫进行捆扎,放入染色釜,在超临界CO2的作用下注入染料,
您最近一年使用:0次
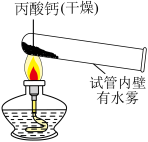
10 . 丙酸钙为白色固体,易溶于水,可作食品防霉剂,国家标准规定了其用于制作面食、糕点时每千克面粉中的最大使用量。小组同学实验探究其性质和防霉的效果。
Ⅰ.探究丙酸钙的性质
【进行实验】用下图装置(夹持仪器已略去)完成实验,记录如下:
【解释与结论】
(1)由①中现象说明丙酸钙一定含有_____ 元素。
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。在实验②中,若要证明①中冷却后的固体里含有碳酸盐,则烧杯中A溶液的溶质是_____ 。
Ⅱ.探究丙酸钙防霉的效果
【进行实验】分别按下列①~⑧的配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
【解释与结论】
(3)第1组,③中X为_____ 。
(4)设计第2组实验的目的是_____ 。
(5)在①-⑧实验中,能证明“有无蔗糖对丙酸钙防霉效果无影响”的所有实验组合是_____ 。
【反思与评价】
(6)结合生活经验,你对日常使用的食品添加剂有什么看法:_____ (一条即可)。
Ⅰ.探究丙酸钙的性质
【进行实验】用下图装置(夹持仪器已略去)完成实验,记录如下:
| 序号 | ① | ② |
| 装置 |
|
|
(1)由①中现象说明丙酸钙一定含有
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。在实验②中,若要证明①中冷却后的固体里含有碳酸盐,则烧杯中A溶液的溶质是
Ⅱ.探究丙酸钙防霉的效果
【进行实验】分别按下列①~⑧的配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
| 组别 | 第1组 | 第2组 | |||||||
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 配方 | 面粉/g | 50 | 50 | 50 | 50 | 50 | 50 | 50 | 50 |
| 酵母/g | 0.75 | 0.75 | X | 0.75 | 0.75 | 0.75 | 0.75 | 0.75 | |
| 蔗糖/g | 0 | 0 | 0 | 0 | 5 | 5 | 5 | 5 | |
| 丙酸钙/g | 0 | 0.06 | 0.10 | 0.15 | 0 | 0.06 | 0.10 | 0.15 | |
| 开始发霉时间 | 第3天 | 第4天 | 第5天 | 第6天 | 第3天 | 第4天 | 第5天 | 第6天 | |
(3)第1组,③中X为
(4)设计第2组实验的目的是
(5)在①-⑧实验中,能证明“有无蔗糖对丙酸钙防霉效果无影响”的所有实验组合是
【反思与评价】
(6)结合生活经验,你对日常使用的食品添加剂有什么看法:
您最近一年使用:0次