名校
1 . 有机增塑剂 和
和 的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是
的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是
 和
和 的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是
的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是| A.Y、Z互为同素异形体 | B.元素的第一电离能:W>R |
| C.原子半径:R>X | D.常温常压下,X、W的单质为固体 |
您最近半年使用:0次
2023-12-16更新
|
590次组卷
|
2卷引用:山东省实验中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
2 . 位于3个不同短周期的6种主族元素W、R、Q、X、Y、Z,原子序数依次增大,R为地壳中含量最丰富的元素,W与Q、R与Y分别同主族,X为同周期的简单离子中半径最小的元素。回答下列问题:
(1)请写出元素符号:W为_______ 、R为_______ 、Q为_______ 。
(2)Q、X的最高价氧化物对应水化物之间能发生反应,其离子方程式为_______ 。
(3)实验室制备Z单质的化学方程式:_______ 。
(4)常见化合物甲、乙均含W、R、Q、Y四种元素,则甲、乙两溶液反应的离子方程式为:_______ 。
(5) 和
和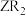 均可作自来水消毒剂,且消毒时还原产物均为Z-,则与8.7g
均可作自来水消毒剂,且消毒时还原产物均为Z-,则与8.7g 的氧化能力相当的
的氧化能力相当的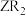 的质量为
的质量为_______ g。
(6)溶液丙 与溶液丁(QRW),两种溶液等体积混合后,沉淀物中含X元素的质量是溶液中含X元素的质量的一半,则丙、丁两种溶液物质的量浓度之比可能为
与溶液丁(QRW),两种溶液等体积混合后,沉淀物中含X元素的质量是溶液中含X元素的质量的一半,则丙、丁两种溶液物质的量浓度之比可能为_______ 。
①1∶1 ②2∶3 ③3∶10 ④3∶11
(1)请写出元素符号:W为
(2)Q、X的最高价氧化物对应水化物之间能发生反应,其离子方程式为
(3)实验室制备Z单质的化学方程式:
(4)常见化合物甲、乙均含W、R、Q、Y四种元素,则甲、乙两溶液反应的离子方程式为:
(5)
 和
和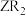 均可作自来水消毒剂,且消毒时还原产物均为Z-,则与8.7g
均可作自来水消毒剂,且消毒时还原产物均为Z-,则与8.7g 的氧化能力相当的
的氧化能力相当的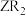 的质量为
的质量为(6)溶液丙
 与溶液丁(QRW),两种溶液等体积混合后,沉淀物中含X元素的质量是溶液中含X元素的质量的一半,则丙、丁两种溶液物质的量浓度之比可能为
与溶液丁(QRW),两种溶液等体积混合后,沉淀物中含X元素的质量是溶液中含X元素的质量的一半,则丙、丁两种溶液物质的量浓度之比可能为①1∶1 ②2∶3 ③3∶10 ④3∶11
您最近半年使用:0次
2022-03-17更新
|
743次组卷
|
2卷引用:福建省龙岩第一中学2021-2022学年高一下学期第二次月考化学试题
解题方法
3 . 短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(一)(1)D在周期表中的位置是_______ ,写出实验室制备单质F的离子方程式__________ 。
(2)化学组成为BDF2的电子式为:______ ,A、C、F三种元素形成的化合物CA4F为________ 化合物(填 “离子”或“共价”)。
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:______________________________ 。
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是_________ (用元素离子符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性________ 于F(填“强”或“弱”),并用化学方程式证明上述结论___________________________________________________ 。
(二)以CA3代替氢气研发氨燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 CA3+3O2=2C2+6H2O.该电池负极的电极反应式为________ ;每消耗3.4g CA3转移的电子数目为______ 。
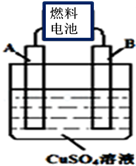
(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为______ ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为________ L。
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

图1 图2
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是____ ,溶液中的H+向_____ 极移动(填“正”或“负”),t1时,原电池中电子流动方向发生改变,其原因是___________ 。
(一)(1)D在周期表中的位置是
(2)化学组成为BDF2的电子式为:
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是
(5)元素B和F的非金属性强弱,B的非金属性
(二)以CA3代替氢气研发氨燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 CA3+3O2=2C2+6H2O.该电池负极的电极反应式为
(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为

(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

图1 图2
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是
您最近半年使用:0次
解题方法
4 . X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。据此回答下列问题:
(1)L的常见原子组成符号为___________ ;M在元素周期表中的位置为_________________ ;五种元素的原子半径从大到小的顺序是_________________ (用具体元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为__________ ,B的结构式为__________________ 。Z和L也能组成原子数目比2∶4的分子C, 已知1 mol 液态C和液态B燃烧时生成无毒无害物质,并释放524.5 kJ的热量,试写出该反应的热化学方程式为________________ 。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为___________ ,其最高价氧化物对应的水化物化学式为___________ 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是________ (填字母代号)。
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R。写出阳极生成R的电极反应式:______________________ 。
(1)L的常见原子组成符号为
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
| A.+99.7 kJ·mol-1 | B.+29.7 kJ·mol-1 | C.-20.6 kJ·mol-1 | D.-241.8 kJ·mol-1 |
您最近半年使用:0次
解题方法
5 . A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,A、B、F三者原子序数之和为25,且知B、F同主族,1.8g E与足量的盐酸反应生成ECl3和2.24L氢气(标准状况下),D+和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,试判断:
(1)六种元素中非金属性最强的是_________ (填代号),该元素在周期表中的位置_____
(2)由A、B、D三种元素形成化合物的电子式_______________
(3)下列能够说明B、F非金属性强弱的方法有____________
A.最高价氧化物对应水化物酸性
B.气态氢化物的热稳定性
C.气态氢化物的沸点B比F高
D.向F的气态氢化物溶液中通入B单质,有浑浊
(4)写出下列反应的离子方程式
①由A、B、D、F四种元素可以组成两种酸式盐,写出这两种盐相反应的离子方程式_______
②写出足量D的最高价氧化物对应水化物与ECl3相互反应的离子方程式______________
(1)六种元素中非金属性最强的是
(2)由A、B、D三种元素形成化合物的电子式
(3)下列能够说明B、F非金属性强弱的方法有
A.最高价氧化物对应水化物酸性
B.气态氢化物的热稳定性
C.气态氢化物的沸点B比F高
D.向F的气态氢化物溶液中通入B单质,有浑浊
(4)写出下列反应的离子方程式
①由A、B、D、F四种元素可以组成两种酸式盐,写出这两种盐相反应的离子方程式
②写出足量D的最高价氧化物对应水化物与ECl3相互反应的离子方程式
您最近半年使用:0次
6 . 元素X、Y、Z、W、M、N原子序数依次增大,X与M、W与N分别同主族,且元素X、Y、Z、W分属两个短周期,它们四者原子序数之和为22,最外层电子数之和为16,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,请回答下列问题:
(1)Y元素在周期表中的位置是__________________________ ,X、Y、Z、W、M的原子半径由大到小的顺序为:_______________ (用元素符号表示)。
(2)写出Y2X2的电子式____________ ;Z2X4结构式 _______________ 。
(3)X、Z、W形成的化合物,水溶液一定显酸性的盐是______________ ,其原因是_____________ (用离子方程式表示),该物质所含化学键的类型是_____________ 。
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为_______________ 。
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式___________________ 。
(6)写出NW2通入硝酸钡溶液中的离子方程式______________ 。
(1)Y元素在周期表中的位置是
(2)写出Y2X2的电子式
(3)X、Z、W形成的化合物,水溶液一定显酸性的盐是
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式
(6)写出NW2通入硝酸钡溶液中的离子方程式
您最近半年使用:0次
13-14高三上·辽宁抚顺·期中
解题方法
7 . X,Y,Z,Q,R是五种短周期元素,原子序数依次增大.X,Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z,R分别是地壳中含量最高的非金属元素和金属元素.请回答下列问题:
(1)上述元素原子半径由大到小的顺序是(写元素符号)____________________ 。
(2)X,Y,Z能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写名称)____________________ 。
该物质能使酸性高锰酸钾溶液褪色同时生成一种生活中常见有机物,此过程的离子方程式为____________________ 。
(3)由以上某些元素组成的化合物A,B,C,D有如下转化关系
A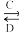 B(在水溶液中进行)
B(在水溶液中进行)
其中C是溶于水显酸性的气体;D是淡黄色固体.
写出C的结构式____________________ 。;
①如果A,B均由三种元素组成,B为两性不溶物,则由A转化为B的离子方程式____________________ 。
②如果A由三种元素组成,B由四种元素组成,A,B溶液均显碱性.用离子方程式表示A溶液显碱性的原因____________________ 。. A,B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是____________________ 。;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有____________________ 。
(1)上述元素原子半径由大到小的顺序是(写元素符号)
(2)X,Y,Z能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写名称)
该物质能使酸性高锰酸钾溶液褪色同时生成一种生活中常见有机物,此过程的离子方程式为
(3)由以上某些元素组成的化合物A,B,C,D有如下转化关系
A
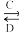 B(在水溶液中进行)
B(在水溶液中进行)其中C是溶于水显酸性的气体;D是淡黄色固体.
写出C的结构式
①如果A,B均由三种元素组成,B为两性不溶物,则由A转化为B的离子方程式
②如果A由三种元素组成,B由四种元素组成,A,B溶液均显碱性.用离子方程式表示A溶液显碱性的原因
您最近半年使用:0次



