名校
解题方法
1 . 下列有关物质的性质与用途具有对应关系的是
A. 是红棕色粉末,可用作油漆的颜料 是红棕色粉末,可用作油漆的颜料 |
B. 能溶于水,可用于生产盐酸 能溶于水,可用于生产盐酸 |
C. 为白色固体,可用于游泳池杀菌消毒 为白色固体,可用于游泳池杀菌消毒 |
D. 能与碱反应,可用作焙制糕点的膨松剂 能与碱反应,可用作焙制糕点的膨松剂 |
您最近一年使用:0次
2023-01-10更新
|
311次组卷
|
4卷引用:湖南省株洲市渌口区第三中学2022-2023学年高一上学期期末考试化学试题
湖南省株洲市渌口区第三中学2022-2023学年高一上学期期末考试化学试题江苏省南通市通州区2022-2023学年高一上学期期末考试化学试题山东省曹县第一中学2022-2023学年高一上学期期末考试化学试题(已下线)题型02 重要元素及其化合物的性质和转化-学易金卷:备战2023-2024学年高一化学期末真题分类汇编(江苏专用)
名校
解题方法
2 . 硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:___________ ;向混合溶液中通入热空气的反应的离子方程式是___________ ;可循环利用的物质是___________ (填化学式)。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:___________ 。(氨水用“NH3·H2O”表示)
②有数据表明,吸收塔中溶液的pH在5.5﹣6.0之间,生产效率较高。当控制好尾气的流量一定时,调节溶液的pH的方法是___________ 。
(3)氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如图:
的形式存在。某工厂处理氨氮废水的流程如图:
含 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标
①过程②加入NaClO溶液可将氨氮物质(以NH3表示)转化为无毒物质,请用离子方程式表示该转化过程___________ 。
②含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的___________ (填字母)。
a.KOH b.Na2SO3 c.KMnO4 d.Na2S
(1)用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
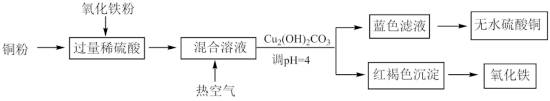
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

②有数据表明,吸收塔中溶液的pH在5.5﹣6.0之间,生产效率较高。当控制好尾气的流量一定时,调节溶液的pH的方法是
(3)氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以
 和
和 的形式存在。某工厂处理氨氮废水的流程如图:
的形式存在。某工厂处理氨氮废水的流程如图:含
 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标①过程②加入NaClO溶液可将氨氮物质(以NH3表示)转化为无毒物质,请用离子方程式表示该转化过程
②含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
a.KOH b.Na2SO3 c.KMnO4 d.Na2S
您最近一年使用:0次
2024-05-03更新
|
173次组卷
|
2卷引用:湖南省常德市石门县第一中学2023-2024学年高一下学期化学期中考试题
3 . 钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
I. 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:

(1) 的电子式为
的电子式为___________ 。
(2)样液中加入 后产生氧气,说明
后产生氧气,说明 与水反应的过程中还生成了
与水反应的过程中还生成了___________ (填化学式)。
(3)用该方法制备的 中含有碳酸钠。若
中含有碳酸钠。若 样品可消耗
样品可消耗 的
的 溶液
溶液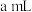 ,则该样品的纯度为
,则该样品的纯度为___________ 。
II.工业上以侯氏制碱法为基础生产焦亚硫酸钠( ,能溶于水)的工艺流程如下:
,能溶于水)的工艺流程如下:

(4)反应I的化学方程式是___________ 。
(5)关于上述流程,下列说法不正确的是___________(填字母)。
(6)Y溶液中含有阳离子有 ,
, 和离子X。检验离子X的方法是
和离子X。检验离子X的方法是___________ 。
(7)反应III包含多步反应:
第一步:……
第二步: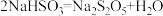
为了减少产品 中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为
中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为___________ 。
(8)已知 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为___________ 。
I.
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:
(1)
 的电子式为
的电子式为(2)样液中加入
 后产生氧气,说明
后产生氧气,说明 与水反应的过程中还生成了
与水反应的过程中还生成了(3)用该方法制备的
 中含有碳酸钠。若
中含有碳酸钠。若 样品可消耗
样品可消耗 的
的 溶液
溶液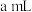 ,则该样品的纯度为
,则该样品的纯度为II.工业上以侯氏制碱法为基础生产焦亚硫酸钠(
 ,能溶于水)的工艺流程如下:
,能溶于水)的工艺流程如下:
(4)反应I的化学方程式是
(5)关于上述流程,下列说法不正确的是___________(填字母)。
A.氨气溶于水使溶液呈碱性的原因是: |
B. 在空气中灼烧发生反应的化学方程式为 在空气中灼烧发生反应的化学方程式为 |
C.该流程中, 可以循环使用 可以循环使用 |
| D.溶液乙经过蒸发结晶得到硫酸铜晶体 |
 ,
, 和离子X。检验离子X的方法是
和离子X。检验离子X的方法是(7)反应III包含多步反应:
第一步:……
第二步:
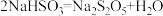
为了减少产品
 中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为
中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为(8)已知
 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
4 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性,其中含氯消毒剂在生产生活中有着广泛的用途。
Ⅰ.某化学兴趣小组用如图装置制备家用消毒液。

(1)写出装置B中反应的离子方程式___________ 。
(2)装置A中的溶液是___________ ,长玻璃导管的作用是___________ 。图中装置的连接顺序是B、___________ 。
(3)用化学方程式表示装置D中“84”消毒液的生成过程:___________ 。
(4)居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是___________ 。
(5)某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为
的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为___________ 。
Ⅱ.世界卫生组织将定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(6)消毒效率是用单位质量的消毒剂得电子数来表示的, 作消毒剂时和
作消毒剂时和 一样,还原产物均为
一样,还原产物均为 。
。 的消毒效率是
的消毒效率是 的
的___________ 倍(保留两位小数)。
Ⅰ.某化学兴趣小组用如图装置制备家用消毒液。

(1)写出装置B中反应的离子方程式
(2)装置A中的溶液是
(3)用化学方程式表示装置D中“84”消毒液的生成过程:
(4)居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是
(5)某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和
 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为
的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为Ⅱ.世界卫生组织将定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(6)消毒效率是用单位质量的消毒剂得电子数来表示的,
 作消毒剂时和
作消毒剂时和 一样,还原产物均为
一样,还原产物均为 。
。 的消毒效率是
的消毒效率是 的
的
您最近一年使用:0次



