解题方法
1 . 如图为某市售盐酸试剂瓶标签上的部分数据。
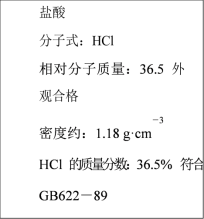
回答下列问题:
(1)该盐酸的物质的量浓度为___________ 。
(2)下列实验操作会导致实验结果偏低的是___________ (填序号)。
①配制 100 g 10%的 CuSO4 溶液,称取 10 g 硫酸铜晶体溶于 90 g 水中;
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮;
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为 0.2 g, 所得溶液的浓度;
④用酸式滴定管量取用 98%,密度为 1.84 g·cm-3 的浓 H2SO4 配制 200 mL 2mol·L-1 的稀 H2SO4 时,先平视后仰视。
(3)已知 CO 和 CO2 的混合气体 14.4 g,在标准状况下所占的体积为 8.96 L。则该混合气体中,CO 的质量为____ g,CO2 的物质的量为______ mol。
(4)1 mol 氧气在放电条件下,有 30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是___________ (填字母)。
A.16 B.17.8 C.18.4 D.35.6
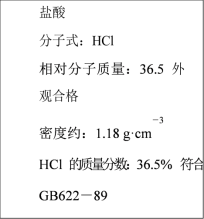
回答下列问题:
(1)该盐酸的物质的量浓度为
(2)下列实验操作会导致实验结果偏低的是
①配制 100 g 10%的 CuSO4 溶液,称取 10 g 硫酸铜晶体溶于 90 g 水中;
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮;
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为 0.2 g, 所得溶液的浓度;
④用酸式滴定管量取用 98%,密度为 1.84 g·cm-3 的浓 H2SO4 配制 200 mL 2mol·L-1 的稀 H2SO4 时,先平视后仰视。
(3)已知 CO 和 CO2 的混合气体 14.4 g,在标准状况下所占的体积为 8.96 L。则该混合气体中,CO 的质量为
(4)1 mol 氧气在放电条件下,有 30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是
A.16 B.17.8 C.18.4 D.35.6
您最近一年使用:0次
名校
2 . 下列实验操作或记录正确的是
| A.常温常压下测得1mol N2和CO的混合气体质量为28 g |
| B.用量筒测得排水法收集制得的氢气体积为50.28mL |
| C.用托盘天平称得2.50 gCuSO4·5H2O,受热充分失水后,固体质量减轻0.90g |
| D.欲配制0.10mol•L-1的硫酸920mL,需量取密度为1.84g•cm-3、质量分数为98%的浓硫酸的体积为5.0mL |
您最近一年使用:0次
2020-10-20更新
|
748次组卷
|
7卷引用:江西省南昌市八一中学2020-2021学年高一上学期10月考试化学试题
江西省南昌市八一中学2020-2021学年高一上学期10月考试化学试题安徽省安庆市第一中学2020-2021学年高一上学期期中考试化学试题甘肃省武威第一中学2020-2021学年高一上学期期中考试化学试题安徽省怀宁中学2020-2021学年高一上学期第二次质量检测化学试题天津市静海区第一中学2020-2021学年高一上学期期末考试化学试题(已下线)第二章 海水中的重要元素——钠和氯(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)辽宁省鞍山市普通高中2022-2023学年高一上学期第三次月考化学试题
名校
解题方法
3 . 溶液浓度是常用的物理量,下列说法正确的是( )
A.将5.85gNaCl固体溶于1L水,所得NaCl溶液物质的量浓度为 |
B.配制 溶液,需称量NaOH固体的质量为3.84g 溶液,需称量NaOH固体的质量为3.84g |
| C.质量分数为98%的浓硫酸与等体积水混合后,硫酸的质量分数大于49% |
D. 溶液和 溶液和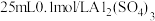 溶液中 溶液中 浓度相同 浓度相同 |
您最近一年使用:0次
2020-10-08更新
|
324次组卷
|
5卷引用:高一必修第一册(苏教2019)专题2 专题综合检测卷
4 . 已知某84消毒液瓶体部分标签如图所示,该84消毒液通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该84消毒液中NaClO的物质的量浓度为_________ 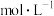 。(计算结果保留2位有效数字)
。(计算结果保留2位有效数字)
(2)某同学取100mL该84消毒液,稀释后用于消毒,稀释后的溶液中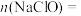
_________ mol。
(3)84消毒液与稀硫酸混合使用可增强其消毒能力,某消毒小组用98% 的浓硫酸配制
的浓硫酸配制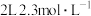 的稀硫酸,用于增强84消毒液的消毒能力,则需用浓硫酸的体积为
的稀硫酸,用于增强84消毒液的消毒能力,则需用浓硫酸的体积为______ mL.
(4)84消毒液与洁厕灵(通常含盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。实验室用密度为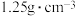 ,质量分数为36.5%的浓盐酸配制
,质量分数为36.5%的浓盐酸配制 的盐酸240mL.
的盐酸240mL.
①配制240mL 的盐酸应选用
的盐酸应选用_______ mL的容量瓶。
②判断下列操作对所配溶液的浓度的影响(填“偏大”“偏小”或“无影响”)。
A.定容时,俯视刻度线,浓度_____________ 。
B.定容时,仰视刻度线,浓度_____________ 。
C.定容摇匀后发现溶液凹液面最低处低于刻度线,加蒸馏水至刻度线,浓度_____________ 。
D.容量瓶在使用前未干燥,里面有少量蒸馏水,浓度_____________ 。

(1)该84消毒液中NaClO的物质的量浓度为
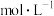 。(计算结果保留2位有效数字)
。(计算结果保留2位有效数字)(2)某同学取100mL该84消毒液,稀释后用于消毒,稀释后的溶液中
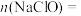
(3)84消毒液与稀硫酸混合使用可增强其消毒能力,某消毒小组用98%
 的浓硫酸配制
的浓硫酸配制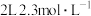 的稀硫酸,用于增强84消毒液的消毒能力,则需用浓硫酸的体积为
的稀硫酸,用于增强84消毒液的消毒能力,则需用浓硫酸的体积为(4)84消毒液与洁厕灵(通常含盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。实验室用密度为
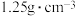 ,质量分数为36.5%的浓盐酸配制
,质量分数为36.5%的浓盐酸配制 的盐酸240mL.
的盐酸240mL.①配制240mL
 的盐酸应选用
的盐酸应选用②判断下列操作对所配溶液的浓度的影响(填“偏大”“偏小”或“无影响”)。
A.定容时,俯视刻度线,浓度
B.定容时,仰视刻度线,浓度
C.定容摇匀后发现溶液凹液面最低处低于刻度线,加蒸馏水至刻度线,浓度
D.容量瓶在使用前未干燥,里面有少量蒸馏水,浓度
您最近一年使用:0次
2020-09-13更新
|
309次组卷
|
2卷引用:鲁科版(2019)高一必修第一册第一章B 素养拓展区 过综合 章末素养综合检测
名校
解题方法
5 . 现用质量分数为98%的浓硫酸(密度为 )配制
)配制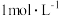 的稀硫酸100 mL。
的稀硫酸100 mL。
(1)经计算,需浓硫酸的体积为_______ mL。
(2)实验中应选用的仪器是_____ (填序号)。
①100mL量筒 ②托盘天平(带砝码) ③玻璃棒 ④50 mL容量瓶 ⑤10mL量筒 ⑥100mL烧杯 ⑦100mL容量瓶 ⑧胶头滴管
(3)此实验中玻璃棒的作用是___________ 。
(4)分析下列操作对所配溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①转移浓硫酸后,烧杯未洗涤:_______ ;
②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中:_______ ;
③定容时俯视容量瓶刻度线:________ ;
④移液前容量瓶内留有少量蒸馏水:________ ;
 )配制
)配制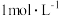 的稀硫酸100 mL。
的稀硫酸100 mL。(1)经计算,需浓硫酸的体积为
(2)实验中应选用的仪器是
①100mL量筒 ②托盘天平(带砝码) ③玻璃棒 ④50 mL容量瓶 ⑤10mL量筒 ⑥100mL烧杯 ⑦100mL容量瓶 ⑧胶头滴管
(3)此实验中玻璃棒的作用是
(4)分析下列操作对所配溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①转移浓硫酸后,烧杯未洗涤:
②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中:
③定容时俯视容量瓶刻度线:
④移液前容量瓶内留有少量蒸馏水:
您最近一年使用:0次
2020-09-13更新
|
748次组卷
|
4卷引用:鲁科版(2019)高一必修第一册高效手册——第1章 认识化学科学
6 . 某超酸的化学式可表示为 。试回答下列有关问题:
。试回答下列有关问题:
(1)这种超酸由_______ 种元素构成,其摩尔质量为_________ 。
(2)用 来表示阿伏加 德罗常数的值,则1mol该超酸中所含氢原子数为
来表示阿伏加 德罗常数的值,则1mol该超酸中所含氢原子数为_______ ;若称取该超酸706g,则所含硼原子数为_______ 。
(3)实验室需要 的这种超酸的水溶液,则配制该溶液时应选择的容量瓶规格是
的这种超酸的水溶液,则配制该溶液时应选择的容量瓶规格是________ ,用托盘天平称取的该超酸的质量是________ 。
 。试回答下列有关问题:
。试回答下列有关问题:(1)这种超酸由
(2)用
 来表示阿伏加 德罗常数的值,则1mol该超酸中所含氢原子数为
来表示阿伏加 德罗常数的值,则1mol该超酸中所含氢原子数为(3)实验室需要
 的这种超酸的水溶液,则配制该溶液时应选择的容量瓶规格是
的这种超酸的水溶液,则配制该溶液时应选择的容量瓶规格是
您最近一年使用:0次
名校
解题方法
7 . 用98%(密度为1.84g/cm3)的浓硫酸稀释成3mol/L的稀硫酸100mL,回答下列问题:
(1)需要取浓硫酸____________ mL
(2)配制操作可分解成如下几步,以下正确的操作顺序是_______
A. 向容量瓶中注入少量蒸馏水,检查是否漏水
B. 用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C. 用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D. 根据计算,用量筒量取一定体积的浓硫酸
E. 将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F. 盖上容量瓶塞子,振荡,摇匀
G. 用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H. 继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
(1)需要取浓硫酸
(2)配制操作可分解成如下几步,以下正确的操作顺序是
A. 向容量瓶中注入少量蒸馏水,检查是否漏水
B. 用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C. 用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D. 根据计算,用量筒量取一定体积的浓硫酸
E. 将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F. 盖上容量瓶塞子,振荡,摇匀
G. 用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H. 继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
您最近一年使用:0次
8 . 下列说法正确的是___ (填序号)。
①将1 mol NaCl溶解在1 L水中,可得1 mol·L-1NaCl的溶液
②将11.2 L HCl气体通入水配成0.5 L溶液,得到1 mol·L-1的盐酸
③1 L 10 mol·L-1的盐酸与9 L水混合,得到1 mol·L-1的盐酸
④将0.4 g NaOH溶解水中形成100 mL溶液,从中取出10 mL,所取溶液物质的量浓度为0.1 mol·L-1(不考虑溶液体积的变化)
⑤将1 mol Na2O溶于水配成1 L溶液,所得溶质的物质的量浓度为1 mol·L-1(不考虑溶液体积的变化)
①将1 mol NaCl溶解在1 L水中,可得1 mol·L-1NaCl的溶液
②将11.2 L HCl气体通入水配成0.5 L溶液,得到1 mol·L-1的盐酸
③1 L 10 mol·L-1的盐酸与9 L水混合,得到1 mol·L-1的盐酸
④将0.4 g NaOH溶解水中形成100 mL溶液,从中取出10 mL,所取溶液物质的量浓度为0.1 mol·L-1(不考虑溶液体积的变化)
⑤将1 mol Na2O溶于水配成1 L溶液,所得溶质的物质的量浓度为1 mol·L-1(不考虑溶液体积的变化)
您最近一年使用:0次
解题方法
9 . 实验室用质量分数为36.5%的浓盐酸(密度为1.25 g·mL-1),配制240 mL 0.1mol·L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为__________ 。
(2)配制240 mL 0.1 mol·L-1的盐酸,应量取浓盐酸体积__________ mL。
(3)应选用容量瓶的规格__________ 。
(1)浓盐酸的物质的量浓度为
(2)配制240 mL 0.1 mol·L-1的盐酸,应量取浓盐酸体积
(3)应选用容量瓶的规格
您最近一年使用:0次
名校
10 . 常温下,在27.5 g水中溶解12.5 g CuSO4•5H2O,恰好达到饱和,该溶液密度为1.18 g·cm-3,求:
(1)该溶液中阴阳离子的总物质的量._________________
(2)该溶液中CuSO4的物质的量浓度(保留二位小数)。________________
(3)取出20.0 mL该溶液,加入足量Ba(OH)2溶液,反应后可得到沉淀质量多少克?(保留一位小数)____________
(1)该溶液中阴阳离子的总物质的量.
(2)该溶液中CuSO4的物质的量浓度(保留二位小数)。
(3)取出20.0 mL该溶液,加入足量Ba(OH)2溶液,反应后可得到沉淀质量多少克?(保留一位小数)
您最近一年使用:0次
2020-02-06更新
|
89次组卷
|
3卷引用:人教版高中化学必修1第一章《从实验学化学》测试卷4



