名校
1 . 下列说法正确的是
| A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol·L-1 |
| B.从1 L 2 mol·L-1的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol·L-1 |
| C.500 mL 0.5 mol·L-1的CuSO4溶液中含有40 g CuSO4 |
| D.中和100 mL 1 mol·L-1的H2SO4溶液,需NaOH固体4 g |
您最近一年使用:0次
名校
2 . 下列说法正确的是
A.同浓度的 、 、 、 、 溶液体积之比为 溶液体积之比为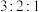 ,则 ,则 浓度之比为 浓度之比为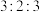 |
B.将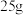 胆矾( 胆矾( )溶于水配成 )溶于水配成 溶液,该溶液的物质的量浓度为 溶液,该溶液的物质的量浓度为 |
C.欲将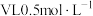 的盐酸浓度增大1倍,可将溶液加热浓缩到原体积的一半 的盐酸浓度增大1倍,可将溶液加热浓缩到原体积的一半 |
D.将 的 的 溶液和 溶液和 的 的 溶液等体积混合后,若忽略溶液体积变化, 溶液等体积混合后,若忽略溶液体积变化,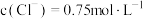 |
您最近一年使用:0次
2023-12-19更新
|
171次组卷
|
3卷引用:山东省实验中学2023-2024学年高一上学期11月期中考试化学试题
名校
3 . 下列实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 制备 | 向饱和食盐水中通入 后,再通 后,再通 |
| B | 配制1 L 1.0 mol/L NaCl溶液 | 将58.5 g NaCl固体直接溶于1 L水中 |
| C | 鉴别 和 和 | 取样,加入澄清石灰水,若有白色沉淀生成,则为 |
| D | 检验NaOH中的阳离子 | 用洁净的铂丝蘸取待测液,在酒精灯火焰上灼烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列叙述不正确的是
A.等质量的 和 和 中所含的氧原子数相同 中所含的氧原子数相同 |
| B.在一定的温度和压强下,各种气体的摩尔体积相等 |
C.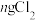 中有m个Cl原子,则阿伏加德罗常数 中有m个Cl原子,则阿伏加德罗常数 的数值可表示为35.5m/n 的数值可表示为35.5m/n |
D.4gNaOH溶解于500mL水中,所得溶液的物质的量浓度为 |
您最近一年使用:0次
2023-10-15更新
|
272次组卷
|
2卷引用:山东省泰安新泰市第一中学(东校)2023-2024学年高一上学期第一次质量检测化学试题
5 . 欲使 溶液的浓度增大一倍,可采取的合理措施是
溶液的浓度增大一倍,可采取的合理措施是
 溶液的浓度增大一倍,可采取的合理措施是
溶液的浓度增大一倍,可采取的合理措施是| A.加入20g固体NaOH,搅拌、溶解 |
| B.将溶液加热浓缩至500g |
C.加入 的NaOH溶液混合均匀 的NaOH溶液混合均匀 |
D.加入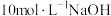 溶液0.1L,再稀释至1.5L 溶液0.1L,再稀释至1.5L |
您最近一年使用:0次
名校
6 . NaClO2是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出ClO2,某探究小组制备NaClO2所需装置如图所示(夹持装置略):

已知:①2ClO2+H2O2+2NaOH = 2NaClO2+O2+2H2O;
②ClO2气体极易溶于水,但不与水反应,可与碱溶液反应;纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
回答下列问题:
(1)完成该实验需要450 mL 4 mol·L-1的NaOH溶液,配制该溶液需要的玻璃仪器除烧杯、胶头滴管和量筒外,还需要_______ ,所需NaOH固体的质量为_______ 。
(2)仪器A的名称是_______ ,装置连接顺序为_______ (按气流方向,用小写字母表示,每个装置仅使用一次)。
(3)装置④中发生反应的化学方程式为_______ 。
(4)②中NaOH溶液的作用是_______ ;打开K通入足量空气的目的是_______ 。
(5)ClO2作消毒剂后转化为Cl-,则其消毒效率(以单位物质的量得到的电子数表示)是Cl2的_______ 倍。

已知:①2ClO2+H2O2+2NaOH = 2NaClO2+O2+2H2O;
②ClO2气体极易溶于水,但不与水反应,可与碱溶液反应;纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
回答下列问题:
(1)完成该实验需要450 mL 4 mol·L-1的NaOH溶液,配制该溶液需要的玻璃仪器除烧杯、胶头滴管和量筒外,还需要
(2)仪器A的名称是
(3)装置④中发生反应的化学方程式为
(4)②中NaOH溶液的作用是
(5)ClO2作消毒剂后转化为Cl-,则其消毒效率(以单位物质的量得到的电子数表示)是Cl2的
您最近一年使用:0次
2023-05-16更新
|
408次组卷
|
2卷引用:山东省烟台市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
7 . 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为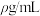 ,质量分数为
,质量分数为 ,物质浓度为c mol/L,则下列关系中正确的是
,物质浓度为c mol/L,则下列关系中正确的是
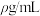 ,质量分数为
,质量分数为 ,物质浓度为c mol/L,则下列关系中正确的是
,物质浓度为c mol/L,则下列关系中正确的是A.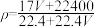 |
B.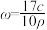 |
C.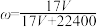 |
D. |
您最近一年使用:0次
2022-10-25更新
|
643次组卷
|
2卷引用:山东省青岛第五十八中学2022-2023学年高一上学期10月月考化学试题
名校
解题方法
8 . 下列有关物质的量浓度的叙述正确的是
A. 水中溶解了 水中溶解了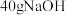 后,所得溶液浓度为 后,所得溶液浓度为 |
B.配制 的 的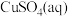 ,需用 ,需用 胆矾 胆矾 |
C.从 中取出 中取出 ,则这 ,则这 的物质的量浓度是原溶液的1/10 的物质的量浓度是原溶液的1/10 |
D. 的 的 中, 中, |
您最近一年使用:0次
9 . 氟化钾是一种重要的无机化合物,应用广泛。其一种制备工艺流程如下:

回答下列问题:
(1)“滤渣”中的主要成分是_______ (填化学式),写出该成分的一种用途:_______ 。
(2)写出制备 的反应的化学方程式:
的反应的化学方程式:_______ ;配制 的浓硫酸,需要用量筒量取密度为
的浓硫酸,需要用量筒量取密度为 的98%的浓硫酸
的98%的浓硫酸_______  。
。
(3)制备 的反应其基本反应类型为
的反应其基本反应类型为_______ 。
(4)写出“转化”时发生反应的化学方程式:_______ 。
(5)“系列操作”包括_______ 、过滤分离和干燥。

回答下列问题:
(1)“滤渣”中的主要成分是
(2)写出制备
 的反应的化学方程式:
的反应的化学方程式: 的浓硫酸,需要用量筒量取密度为
的浓硫酸,需要用量筒量取密度为 的98%的浓硫酸
的98%的浓硫酸 。
。(3)制备
 的反应其基本反应类型为
的反应其基本反应类型为(4)写出“转化”时发生反应的化学方程式:
(5)“系列操作”包括
您最近一年使用:0次
解题方法
10 . 配制500mL0.1mol·L-1硫酸铜溶液,需胆矾
| A.8.00 g | B.16.0 g | C.25.0 g | D.12.5 g |
您最近一年使用:0次



