名校
解题方法
1 . 日常生活及化学实验中,准确配制一定物质的量浓度的溶液至关重要。
(1)实验室需要用到240mL0.5mol/L硫酸,现实验室只有物质的量浓度为1mol/L的硫酸,该同学需要自己稀释,他需要量取_______ mL1mol/L的硫酸。
(2)实验室某浓盐酸试剂瓶标签如下图所示,试根据标签上的有关数据回答下列问题:

该浓盐酸中HCl的物质的量浓度为_______ 。
(3)某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol/L的Na2CO3溶液。溶液的配制过程如图所示:

a.请把配制过程中两处明显错误请改正过来_______ 、_______ 。
b.请分析下列情况对所配溶液浓度产生的影响:其中引起所配溶液浓度偏高的有_______ (填序号)。
①用“左物右码”的方法称量(使用游码)
②碳酸钠不纯,其中混有氯化钠
③容量瓶未经干燥使用
④称量碳酸钠时所用砝码生锈
⑤移液过程中有少量溶液溅出
(1)实验室需要用到240mL0.5mol/L硫酸,现实验室只有物质的量浓度为1mol/L的硫酸,该同学需要自己稀释,他需要量取
(2)实验室某浓盐酸试剂瓶标签如下图所示,试根据标签上的有关数据回答下列问题:

该浓盐酸中HCl的物质的量浓度为
(3)某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol/L的Na2CO3溶液。溶液的配制过程如图所示:

a.请把配制过程中两处明显错误请改正过来
b.请分析下列情况对所配溶液浓度产生的影响:其中引起所配溶液浓度偏高的有
①用“左物右码”的方法称量(使用游码)
②碳酸钠不纯,其中混有氯化钠
③容量瓶未经干燥使用
④称量碳酸钠时所用砝码生锈
⑤移液过程中有少量溶液溅出
您最近一年使用:0次
2021-03-10更新
|
144次组卷
|
3卷引用:广西来宾市2020-2021学年高一上学期期末教学质量检测化学试题
2 . 根据要求,回答下列问题:
Ⅰ.如图为实验室某浓盐酸试剂瓶标签上的有关数据。

(1)该浓盐酸中, 的物质的量浓度为
的物质的量浓度为___________  。
。
(2)取用任意体积的该浓盐酸时,下列物理量中不随所取体积的多少而变化的是___________ (填标号)。
A.溶液的密度
B.溶质 的物质的量
的物质的量
C.溶质 的物质的量浓度
的物质的量浓度
D.溶液中 的物质的量
的物质的量
(3)用该浓盐酸和蒸馏水配制 物质的量浓度为
物质的量浓度为 的稀盐酸。
的稀盐酸。
①需量取___________  该浓盐酸进行配制(保留1位小数)。
该浓盐酸进行配制(保留1位小数)。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”、“偏低”或“无影响”)。用量筒量取浓盐酸时俯视观察凹液面:___________ 。定容后经振荡、摇匀、静置,发现液面略有下降,再加适量的蒸馏水到容量瓶颈部的刻度线___________ 。
Ⅱ.将一定量的镁铝合金投入 一定浓度的盐酸中,充分反应,合金全部溶解。向合金溶解后所得溶液中滴加
一定浓度的盐酸中,充分反应,合金全部溶解。向合金溶解后所得溶液中滴加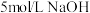 溶液,生成沉淀的质量与加入的
溶液,生成沉淀的质量与加入的 溶液的体积关系如图所示。
溶液的体积关系如图所示。

(1)原合金中,镁的质量为___________ g,铝的质量为___________ g。
(2)盐酸溶液中溶质的物质的量浓度为___________  。
。
Ⅰ.如图为实验室某浓盐酸试剂瓶标签上的有关数据。

(1)该浓盐酸中,
 的物质的量浓度为
的物质的量浓度为 。
。(2)取用任意体积的该浓盐酸时,下列物理量中不随所取体积的多少而变化的是
A.溶液的密度
B.溶质
 的物质的量
的物质的量C.溶质
 的物质的量浓度
的物质的量浓度D.溶液中
 的物质的量
的物质的量(3)用该浓盐酸和蒸馏水配制
 物质的量浓度为
物质的量浓度为 的稀盐酸。
的稀盐酸。①需量取
 该浓盐酸进行配制(保留1位小数)。
该浓盐酸进行配制(保留1位小数)。②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”、“偏低”或“无影响”)。用量筒量取浓盐酸时俯视观察凹液面:
Ⅱ.将一定量的镁铝合金投入
 一定浓度的盐酸中,充分反应,合金全部溶解。向合金溶解后所得溶液中滴加
一定浓度的盐酸中,充分反应,合金全部溶解。向合金溶解后所得溶液中滴加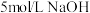 溶液,生成沉淀的质量与加入的
溶液,生成沉淀的质量与加入的 溶液的体积关系如图所示。
溶液的体积关系如图所示。
(1)原合金中,镁的质量为
(2)盐酸溶液中溶质的物质的量浓度为
 。
。
您最近一年使用:0次
3 . 分类法在化学中起着非常重要的作用,现有下列物质:①Cl2、②NaOH溶液、③Cu、④冰水混合物、⑤ 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
(1)属于纯净物的有_______ ,属于氧化物的有_______ 。
(2)能导电的物质有_______ ,属于电解质的有_______ 。
(3)实验室中制取少量氢氧化铁胶体的离子方程式为_______ 。
(4)已知Cl2与NaOH反应的化学方程式是 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取_______ mL1mol/L的硫酸。
 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:(1)属于纯净物的有
(2)能导电的物质有
(3)实验室中制取少量氢氧化铁胶体的离子方程式为
(4)已知Cl2与NaOH反应的化学方程式是
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取
您最近一年使用:0次
2021-02-07更新
|
198次组卷
|
2卷引用:广西河池市2020-2021学年高一上学期期末教学质量检测化学试题
名校
4 . 如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为____ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是____ 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸。该学生需要量取___ mL上述浓盐酸进行配制。

(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸。该学生需要量取
您最近一年使用:0次
2020-10-25更新
|
90次组卷
|
2卷引用:广西浦北中学2021-2022学年高一上学期期中考试化学试题



