1 . 某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐渐加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量_______ g。
(2)反应至A点时,溶液中钠元素的质量是_______ g。

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量
(2)反应至A点时,溶液中钠元素的质量是
您最近一年使用:0次
2021高三·全国·专题练习
2 . VL浓度为0.5mol·L-1的盐酸,欲使其浓度增大1倍,可将溶液加热浓缩到0.5VL。( )
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
3 . 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1。( )
您最近一年使用:0次
2022-07-08更新
|
178次组卷
|
5卷引用:考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量的浓度及溶液配制-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量浓度及溶液配制(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第9讲 物质的量浓度
2021高三·全国·专题练习
4 . 某同学购买了一瓶“84”消毒液,包装说明如下:
请根据以上信息和相关知识判断,下列分析不正确的是
| 主要成分:25%NaClO、1 000 mL、密度1.19 g·cm-3 使用方法:稀释100倍(体积比)后使用 注意事项:密封保存,易吸收空气中的CO2变质 |
| A.该“84”消毒液的物质的量浓度为4.0 mol·L-1 |
| B.一瓶该“84”消毒液敞口放置一段时间后浓度会变小 |
| C.取100 mL该“84”消毒液稀释100倍后用于消毒,稀释后的溶液中c(Na+)约为0.04 mol·L-1 |
| D.参阅该“84”消毒液的配方,欲用NaClO固体配制含25%NaClO的消毒液480 mL,需要称量的NaClO固体质量为143 g |
您最近一年使用:0次
2021-08-08更新
|
397次组卷
|
6卷引用:考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)2.2.1 物质的量浓度-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)(已下线)第一单元 化学计量在实验中的应用(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)考点03 物质的量的浓度及溶液配制-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量浓度及溶液配制(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
20-21高一·浙江·阶段练习
5 . 实验室欲配制480 mL0.5 mol/L的CuSO4溶液,据此回答下列问题:
(1)需称量胆矾CuSO4·5H2O___________ g。
(2)从配制好的CuSO4溶液中取出10 mL,将这10 mL的CuSO4溶液稀释至100 mL,稀释后CuSO4溶液的浓度变为___________ mol/L。
(1)需称量胆矾CuSO4·5H2O
(2)从配制好的CuSO4溶液中取出10 mL,将这10 mL的CuSO4溶液稀释至100 mL,稀释后CuSO4溶液的浓度变为
您最近一年使用:0次
名校
解题方法
6 . 下列有关浓度的说法正确的是
| A.10℃时,100 mL 0.35 mol/L的KCl饱和溶液蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度大于0. 35 mol/L |
| B.将标准状况下22. 4L HCl溶于1 L水中可得1 mol/L盐酸 |
| C.将78 gNa2O2溶于水,配成1 L溶液可得到浓度为1mol/L的溶液 |
| D.将25.0 g胆矾(CuSO4·5H2O)溶于水后配成100 mL溶液,所得溶液浓度为1 mol/L |
您最近一年使用:0次
2021-03-11更新
|
222次组卷
|
5卷引用:【浙江新东方】高中化学20210304-022
(已下线)【浙江新东方】高中化学20210304-022(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)安徽省泗县第一中学2021-2022学年高一上学期第一次月考化学试题辽宁省实验中学东戴河分校、兴城市高级中学2020-2021学年高一12月月考化学试题
20-21高一上·浙江绍兴·阶段练习
解题方法
7 . 下列关于物质的量浓度的配制和计算正确的是
| A.配制物质的量浓度为0.1 mol/L的CuSO4溶液80 mL时,用托盘天平称取2.00g胆矾 |
| B.配制稀盐酸用量筒量取浓盐酸时俯视刻度线,则所配溶液的浓度将偏高 |
| C.取58.5 g NaCl固体放入1 L水中充分溶解,所得溶液中NaCl的物质的量浓度为1 mol/L |
| D.将浓度为2 mol/L硫酸钠溶液10 mL加水稀释至200 mL,所得溶液浓度为0.1 mol/L |
您最近一年使用:0次
名校
解题方法
8 . 对1L1mol•L-1氯化镁溶液的理解,不正确的是
| A.95g无水氯化镁溶于1L水中即可得到上述溶液 |
| B.该溶液中含有95g溶质 |
| C.该溶液中氯离子的物质的量浓度为2mol•L-1 |
| D.从该溶液中取出100mL,其物质的量浓度为1mol•L-1 |
您最近一年使用:0次
2020-12-27更新
|
257次组卷
|
2卷引用:浙江省吴兴高级中学2021-2022学年高一上学期12月月考化学试题
名校
解题方法
9 . 环境问题是广大群众关注的热点话题之一,化工厂排放的废水、废渣一般利用化学原理可以进行排放物达标检测与无害化处理。某皮革厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:
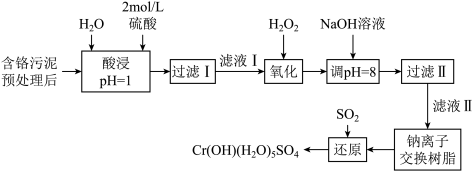
已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)如需配制480 mL酸浸环节所需的硫酸,需要用量筒量取18.4 mol·L-1的浓硫酸___________ mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需哪些仪器___________
(2)经氧化环节滤液Ⅰ中的Cr3+转化为Cr2O ,写出此反应的离子方程式:
,写出此反应的离子方程式:___________
(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O 转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因
转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因___________
(4)钠离子交换树脂的反应原理为Mn++nNaR MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有___________
(5)请写出流程中用SO2进行还原时发生反应的离子方程式:___________

已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4 | 9 |
| 沉淀溶解时的pH | — | — | >8溶解 | >9溶解 |
(2)经氧化环节滤液Ⅰ中的Cr3+转化为Cr2O
 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O
 转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因
转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因(4)钠离子交换树脂的反应原理为Mn++nNaR
 MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有(5)请写出流程中用SO2进行还原时发生反应的离子方程式:
您最近一年使用:0次
19-20高一·浙江·阶段练习
名校
10 . 如图为实验室某浓盐酸试剂瓶上标签的有关内容,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为__________ mol/L。
(2)取该溶液20.0mL逐滴滴入100mL2.00mol/L的碳酸钠溶液中,产生CO2在标准状况下的体积为_________ mL。(不考虑CO2在水中的溶解)

(1)该浓盐酸中HCl的物质的量浓度为
(2)取该溶液20.0mL逐滴滴入100mL2.00mol/L的碳酸钠溶液中,产生CO2在标准状况下的体积为
您最近一年使用:0次



