名校
解题方法
1 . 在t℃时,将agNH3完全溶于水,得到VmL溶液,该溶液的密度为ρg/cm3,质量分数为w,其中含 的物质的量为bmol。下列叙述正确的是( )
的物质的量为bmol。下列叙述正确的是( )
 的物质的量为bmol。下列叙述正确的是( )
的物质的量为bmol。下列叙述正确的是( )A.溶质的质量分数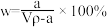 |
B.溶质的物质的量浓度 |
C.溶液中 |
D.上述溶液中再加入 水,所得溶液溶质的质量分数大于 水,所得溶液溶质的质量分数大于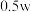 |
您最近一年使用:0次
2020-09-05更新
|
396次组卷
|
6卷引用:贵州省遵义市第一中学2022-2023学年高一上学期期中考试化学试题
贵州省遵义市第一中学2022-2023学年高一上学期期中考试化学试题(已下线)2013届安徽省望江二中高三(复读班)第三次月考化学试卷(已下线)2014届高考化学二轮复习 专题2常用化学计量——物质的量练习卷人教版(2019)高一必修第一册第二章 海水中的重要元素 第三节 物质的量 易错疑难集训(二)鲁科版(2019)高一必修第一册第一章易错疑难集训(二)江西省贵溪市实验中学2021届高三第一次月考化学试题
2020高三·全国·专题练习
名校
2 . 下列有关溶液浓度的说法正确的是
| A.将500mL1mol·L-1的硝酸溶液蒸发至100mL,浓度变为5mol·L-1 |
| B.将10mL18.4mol·L-1浓硫酸与90mL水混合,得到的稀硫酸浓度为1.84mol·L-1 |
| C.配制1mol·L-1KAl(SO4)2溶液100mL,应称取明矾晶体47.4g |
| D.实验室需要450mL0.2mol·L-1的NaOH溶液,应准确称量烧碱3.6g |
您最近一年使用:0次
名校
解题方法
3 . 下图为实验室某盐酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:
(1)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是____ (填字母)。
A.溶液中HCl的物质的量 B.溶液的物质的量浓度
C.溶液的密度 D.溶液中Cl-的数目
(2)某学生欲用上述浓盐酸和蒸馏水配制500 mL0.50 mol/L的稀盐酸。
①该学生需要量取____ mL上述浓盐酸进行配制。
②本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是_______ 。
(3)①假设该同学成功配制了0.50mol/L的盐酸,他又用该盐酸中和含0.4 g溶质的NaOH溶液,则该同学需取____ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g溶质的NaOH溶液,发现消耗的盐酸比①中所求体积偏小,则可能的原因是_______ (填字母)。
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.定容时,俯视容量瓶刻度线
D.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g·cm-3 物质的量浓度:11.9mol·L-1 |
A.溶液中HCl的物质的量 B.溶液的物质的量浓度
C.溶液的密度 D.溶液中Cl-的数目
(2)某学生欲用上述浓盐酸和蒸馏水配制500 mL0.50 mol/L的稀盐酸。
①该学生需要量取
②本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
(3)①假设该同学成功配制了0.50mol/L的盐酸,他又用该盐酸中和含0.4 g溶质的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4 g溶质的NaOH溶液,发现消耗的盐酸比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.定容时,俯视容量瓶刻度线
D.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
您最近一年使用:0次
2020-07-30更新
|
289次组卷
|
3卷引用:黑龙江省双鸭山市第一中学2021-2022学年高一上学期期末考试化学试题
18-19高一下·江苏·期中
名校
解题方法
4 . 如图是硫酸试剂标签上的部分内容。请回答下列问题:

(1)该浓硫酸中溶质、溶剂分子数目之比为___ ,现用该浓H2SO4来配制480mL、0.3mol·L-1的稀H2SO4,需量取该浓H2SO4的体积为___ mL。
(2)配制时,下列仪器中必须使用___ (填代号),还缺少的仪器是___ 、___ 。
①托盘天平(带砝码) ②10mL量筒 ③20mL量筒 ④烧杯 ⑤玻璃棒 ⑥100mL容量瓶 ⑦漏斗 ⑧烧瓶
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有___ (填代号)。
①用量筒量取98%的硫酸时俯视
②洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
③未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,仰视刻度线

(1)该浓硫酸中溶质、溶剂分子数目之比为
(2)配制时,下列仪器中必须使用
①托盘天平(带砝码) ②10mL量筒 ③20mL量筒 ④烧杯 ⑤玻璃棒 ⑥100mL容量瓶 ⑦漏斗 ⑧烧瓶
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有
①用量筒量取98%的硫酸时俯视
②洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
③未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,仰视刻度线
您最近一年使用:0次
2020-01-05更新
|
134次组卷
|
3卷引用:衔接点20 物质的量浓度-2022年初升高化学无忧衔接?
(已下线)衔接点20 物质的量浓度-2022年初升高化学无忧衔接?【全国百强校】江苏省海安高级中学2018-2019学年高一(创新实验班)下学期期中考试化学试题辽宁省滨海实验中学2019-2020学年高一上学期期末化学试题
名校
解题方法
5 . 相对分子质量为M的气态化合物VL (标准状况),溶于mg水中,得到质量分数为w、 物质的量浓度为c mol/L、密度为g/mL的溶液,下列说法正确的是
| A.相对分子质量 M=22.4mω/(1-ω)V |
| B.物质的量浓度c=ρv/(MV+22.4m) |
| C.溶液的质量分数ω=MV/22.4m |
| D.溶液密度ρ=cω/1000ρω |
您最近一年使用:0次
2019-12-27更新
|
420次组卷
|
3卷引用:黑龙江哈尔滨师范大学附属中学2021-2022学年高二下学期期末测试化学试题
黑龙江哈尔滨师范大学附属中学2021-2022学年高二下学期期末测试化学试题河南省郑州第四十七中2019-2020学年高一上学期第二次月考化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元01讲核心
名校
解题方法
6 . 欲配制100mL1.0 mol/L Na2SO4溶液,正确的方法是
①将14.2 g Na2SO4,溶于100mL水中
②将32.2g Na2SO4•10H2O溶于少量水中,再用水稀释至100 mL
③将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
①将14.2 g Na2SO4,溶于100mL水中
②将32.2g Na2SO4•10H2O溶于少量水中,再用水稀释至100 mL
③将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
| A.①② | B.②③ | C.①③ | D.①②③ |
您最近一年使用:0次
2019-12-13更新
|
1691次组卷
|
65卷引用:辽宁省葫芦岛市2022-2023学年高一上学期期中考试化学试题
辽宁省葫芦岛市2022-2023学年高一上学期期中考试化学试题福建省上杭县第一中学2022-2023学年高一上学期10月月考化学试题(已下线)2010年广东省中山一中高一上学期第二次段考化学试题(已下线)2010年广东省深圳高级中学高一上学期期中考试化学试卷(已下线)2010年青海省青海师大附中高一上学期期中考试化学试卷(已下线)2010年陕西省西安铁一中高一第一学期期中考试化学试卷(已下线)2010-2011学年甘肃省天水市一中高一第一学期段考化学试卷(已下线)2011-2012学年陕西省长安一中高一上学期期中考试化学试卷(已下线)2011-2012年湖南省师大附中高一上学期期中考试化学试卷(已下线)2011-2012学年陕西省师大附中高一上学期期中考试化学试卷(已下线)2011-2012学年陕西省师大附中高一上学期期中考试化学试卷(已下线)2012届内蒙古呼伦贝尔市牙克石林业一中高三上学期第一次模拟考试化学试卷(已下线)2011-2012学年浙江省杭州学军中学高一上学期期末考试化学试卷(已下线)2011—2012学年海南省洋浦中学高一第一学期期末考试化学试卷(已下线)2012-2013学年吉林省松原市扶余县一中高一第一次月考化学试卷(已下线)2012-2013学年吉林长春实验中学高一上学期第一次月考化学试卷(已下线)2013-2014学年广西北海市合浦县高一上学期期中考试化学试卷2015-2016河北石家庄第一中学高一上期中考试化学试卷2015-2016学年湖北航天高中、安陆二中等五校高一上期中化学试卷2015-2016学年福建省仙游一中高一上期中测试化学试卷2018版化学(苏教版)高考总复习专题一课时跟踪训练:物质的量浓度及其溶液的配制山东省临沂市蒙阴县实验中学2017-2018学年高一上学期期中考试化学试题2018-2019学年高中化学鲁科版必修1章末综合测评题(一)河南省鹤壁市淇县第一中学2018-2019学年高一上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期10月月考化学试题河南省新乡市新乡县龙泉中学2018-2019学年高一上学期10月月考理科综合化学试题【全国百强校】重庆市江津中学2018-2019学年高一上学期第一次阶段考试(10月)化学试题甘肃省卓尼县柳林中学2018-2019学年高一上学期第一次月考化学试题河南省永城高中2018-2019学年高一上学期第一次月考化学试题【全国百强校】吉林省延边市第二中学2018-2019学年高一上学期期中考试化学试题湖北省公安县车胤中学2017-2018学年高一3月月考化学试题(已下线)2019高考热点题型和提分秘籍 第一章 物质的量 第2讲 物质的量在化学实验中的应用( 题型专练)【全国百强校】四川省仁寿第一中学南校区2018-2019学年高一上学期11月份期中(第一次教学质量检测)化学试题河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题甘肃省张掖市山丹县第一中学2019-2020学年高一9月月考化学试题贵州省遵义航天高级中学2019-2020学年高一上学期第一次月考化学试题山东省枣庄市第八中学东校区2019-2020学年高一10月月考化学试题四川省乐山市沫若中学2019-2020学年高一上学期第一次月考化学试题河南省新乡市第三中学2019-2020学年高一上学期第一次月考化学试题新疆维吾尔自治区喀什第二中学2019-2020学年高一9月月考化学试题吉林省榆树市第一高级中学2019-2020学年高一上学期期中考试化学试卷宁夏青铜峡市高级中学2019-2020学年高一上学期期中考试化学试题河南省周口中英文学校2019-2020学年高一上学期期中考试化学试题广东省深圳市红岭中学2019-2020学年高一上学期第一学段检测化学试题黑龙江省大兴安岭漠河县第一中学2019-2020学年高一上学期第一次阶段考试化学试题湖南省郴州市湘南中学2019-2020学年高一上学期期中考试化学试题天津一中2018-2019学年高一上学期第一次月考化学试题宁夏海原县第一中学2019-2020学年高一上学期期末考试化学试题湖南省常德市石门县第二中学2019-2020学年高一上学期第一次月考化学试题2020届高三化学二轮冲刺新题专练——仪器的连接和实验的操作顺序(提升练)湖北省黄冈市黄梅国际育才高级中学2019-2020学年高一上学期10月月考化学试题河南省郑州市河南省实验中学2019-2020学年高一上学期第一次月考化学试题鲁科版(2019)高一必修第一册第1章 认识化学科学 总结检测四川省攀枝花市第十五中学2019-2020学年高一上学期第一次月考化学试题山东省新泰市第一中学老校区(新泰中学)2020-2021学年高一上学期第一次月考化学试题河南省洛阳市第一中学2020-2021学年高一上学期第一次月考化学试题陕西省西安市长安区第一中学2020-2021学年高一上学期第一次教学质量检测化学试题江苏省常州市戚墅堰高级中学2020-2021学年高一上学期期中质量调研考试化学试题(已下线)【浙江新东方】76.专题2 第二单元 溶液组成的定量研究-高中化学苏教2019版必修第一册新疆呼图壁县第一中学2020-2021学年高三上学期9月月考化学试题浙江省金华市云富高级中学2020-2021学年高一10月月考化学试题山东省济南市2020-2021学年高一上学期10月月考化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一上学期期末考试化学试题青海省西宁市第五中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
7 . 下列关于物质的量浓度表述正确的是( )
| A.0.3mol•L﹣1的Na2SO4溶液中含有Na+和SO42﹣的总物质的量为0.9mol |
| B.当22.4L氨气完全溶于水制得1L氨水时,其浓度是1mol•L﹣1 |
| C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42﹣的物质的量相等,则K+和Cl﹣的物质的量浓度一定相等 |
| D.10℃时,0.35mol/L的KCl饱和溶液100mL蒸发掉5g水,冷却到10℃时,其体积小于100mL,它的物质的量浓度仍为0.35mol/L |
您最近一年使用:0次
2019-11-25更新
|
76次组卷
|
2卷引用:新疆和田地区第二中学2022-2023学年高一上学期11月期中考试化学试题
名校
8 . 4℃时,100mL水中溶解了33.6L(STP)HCl气体,所得盐酸密度为1.18g·mL﹣1。下列有关说法不正确的是( )
| A.该盐酸的物质的量浓度为15mol·L﹣1 |
| B.该盐酸溶质的质量分数为35.4% |
| C.该温度下HCl的溶解度可能大于336(气体溶解度以体积比计算) |
| D.相同条件下,一定量水中溶解HCl气体越多,所得盐酸密度越大 |
您最近一年使用:0次
2019-11-22更新
|
143次组卷
|
3卷引用:江苏省常州市第一中学2022-2023学年高一上学期期中质量调研化学试题
19-20高一上·甘肃兰州·期中
9 . 配制240 mL 1 mol/L 的稀盐酸溶液,需要12 mol/L的浓盐酸的体积为 ( )
| A.12 mL | B.25 mL |
| C.20.8 mL | D.12.5 mL |
您最近一年使用:0次
2019-11-10更新
|
368次组卷
|
4卷引用:第06讲 一定物质的量浓度溶液的配制-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
(已下线)第06讲 一定物质的量浓度溶液的配制-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)甘肃省兰州市联片办学2019-2020学年高一上学期期中考试化学试题辽宁省营口市大石桥市第三高级中学2020-2021学年高一上学期第二次月考化学试题甘肃省兰州市第四片区2020-2021学年高一上学期期中考试化学试题
名校
10 . 下列有关实验原理或操作正确的是( )
| A.用20mL量筒量取15mL 酒精,加水5mL,配制质量分数为75%酒精溶液 |
| B.在200mL 某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属阳离子,不考虑水解问题,则该硫酸盐的物质的量浓度为2.5mol·L−1 |
| C.实验中需用2.0mol·L−1的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为 1000mL、201.4g |
| D.实验室配制500mL0.2mol·L−1的硫酸亚铁溶液,其操作是:用天平称15.2g绿矾(FeSO4·7H2O),放入小烧杯中加水溶解,转移到500mL容量瓶,洗涤、稀释、定容、摇匀 |
您最近一年使用:0次
2019-10-31更新
|
362次组卷
|
4卷引用:广东省汕头市潮阳黄图盛中学2021-2022学年高三下学期一模检验化学试题
广东省汕头市潮阳黄图盛中学2021-2022学年高三下学期一模检验化学试题吉林省长春市东北师范大学附中2020届高三上学期第一次摸底考试化学试题(已下线)考点20 化学实验基础知识-2020年高考化学命题预测与模拟试题分类精编福建省福州第一中学2021届高三下学期开学考试化学试题



