名校
1 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
523次组卷
|
5卷引用:吉林省长春市第五中学2023-2024学年高一下学期第一学程考试化学试题
解题方法
2 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。为除去溶液中的Fe2+,可先加入_______,(从下面四个选项选择)将Fe2+氧化为Fe3+
| A.CuO | B.Cl2 | C.Cu(OH)2 | D.H2O2 |
您最近一年使用:0次
3 . 室温下,在指定分散系中,下列各组微粒能大量共存的是
A.饱和氯水中: |
B. 胶体中: 胶体中: |
C.漂白粉溶液中: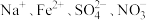 |
D. 的 的 溶液中: 溶液中: |
您最近一年使用:0次
名校
4 . 下列离子方程式正确的是
A.铜与稀硝酸: |
B.用 溶液吸收少量的 溶液吸收少量的 : : |
C. 溶液与足量NaOH溶液反应: 溶液与足量NaOH溶液反应: |
D.向 溶液中通入等物质的量的 溶液中通入等物质的量的 : :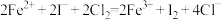 |
您最近一年使用:0次
2024-03-13更新
|
476次组卷
|
2卷引用:吉林省长春市第五中学2023-2024学年高一下学期第一学程考试化学试题
名校
解题方法
5 . 用钛白厂的副产品和氯化钾制备硫酸钾,并得到副产品颜料铁红的流程如图:
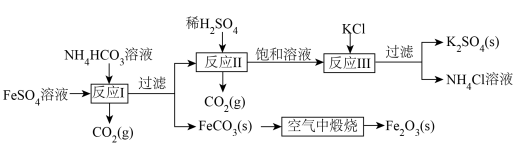
依据该流程回答下列问题:
已知:上述流程中,s表示固体,g表示气体。
(1)配制硫酸亚铁溶液时,通常加入少量的铁粉,加入铁粉的目的是______ ;“反应I”的离子方程式为______ ;如果向硫酸亚铁溶液中直接滴加氢氧化钠溶液,可观察到的现象是______ ,沉淀颜色变化的总反应的化学方程式为______ 。
(2)“空气中煅烧”制取铁红的反应的化学方程式为______ ,还原剂是______ (填化学式)。
(3)“反应Ⅲ”的离子方程式为______ ,该反应原理类似氨碱法制小苏打,利用了相同条件下物质溶解性差异的特点,其中______ (填名称)的溶解度相对其他物质比较小,可以以固体形式析出。

依据该流程回答下列问题:
已知:上述流程中,s表示固体,g表示气体。
(1)配制硫酸亚铁溶液时,通常加入少量的铁粉,加入铁粉的目的是
(2)“空气中煅烧”制取铁红的反应的化学方程式为
(3)“反应Ⅲ”的离子方程式为
您最近一年使用:0次
6 . 物质的性质复杂多变,下列由实验方案及现象得出的结论错误的是
选项 | 实验方案 | 实验现象 | 实验结论 |
| A | 向包有Na2O2粉末的脱脂棉上滴水 | 脱脂棉燃烧 | Na2O2与水反应放出热量 |
| B | 向FeCl2溶液中加入足量锌粉 | 溶液由浅绿色变成无色 | Fe2+具有氧化性 |
| C | 向Fe(SO4)3溶液中加入足量铜粉 | 溶液由棕黄色变成蓝色 | Fe3+具有氧化性 |
| D | 用洁净的铁丝蘸取某溶液置于酒精灯外焰上灼烧 | 焰色呈黄色 | 该溶液中含有NaCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列反应的离子方程式书写正确的是
A. 溶液与 溶液与 反应: 反应: |
B.碳酸钙与稀盐酸反应: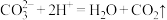 |
C.氧化铝和稀硫酸反应: |
D.稀硫酸清洗铁锈(氧化铁): |
您最近一年使用:0次
名校
解题方法
8 . 《新修本草》中关于“青矾”的描述:“本来绿色,新出窟未见风者,正如琉璃……,烧之赤色……。”下列说法正确的是
| A.青矾能被磁石吸引 | B.青矾的主要成分为FeSO4·7H2O |
| C.“烧”青矾的过程中未发生化学变化 | D.“烧之赤色”中的“赤”是Fe3O4的颜色 |
您最近一年使用:0次
名校
解题方法
9 . 铁及其化合物在生产,生活中有重要用途。某化学兴趣小组的同学设计了以下两个实验,请回答下列问题:
I.“铁与水反应”,并检验产物的性质。(夹持装置已略去)

(1)装置A中盛放碎瓷片的仪器的名称为_______ ,装置A的作用是_______ ;
(2)装置B中发生反应的化学方程式为_______ ;
(3)实验一段时间后,装置E中的实验现象为_______ ;
Ⅱ.制备Fe(OH)2。

已知:NaOH溶液是用去氧水配制的。
(4)仪器a使用之前需要采取的操作是_______ ,煤油的作用是_______ 。
(5)实验开始时的具体操作是_______ ,仪器b中产生均匀气泡后的操作是_______ 。
(6)设计实验检验仪器c中的金属离子:_______ 。
I.“铁与水反应”,并检验产物的性质。(夹持装置已略去)

(1)装置A中盛放碎瓷片的仪器的名称为
(2)装置B中发生反应的化学方程式为
(3)实验一段时间后,装置E中的实验现象为
Ⅱ.制备Fe(OH)2。

已知:NaOH溶液是用去氧水配制的。
(4)仪器a使用之前需要采取的操作是
(5)实验开始时的具体操作是
(6)设计实验检验仪器c中的金属离子:
您最近一年使用:0次
2024-01-11更新
|
227次组卷
|
2卷引用:吉林省白山市抚松县第一中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
10 . 某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
Ⅰ.探究FeCl2溶液的性质。
(1)从化合价的角度预测,FeCl2可能具有的性质___________ 。
(2)向FeCl2溶液中滴加酸性KMnO4溶液,可观察到的现象是___________ ,某同学认为上述现象并不能证明Fe2+具有还原性,他的理由___________ 。
Ⅱ.探究FeCl3溶液的性质
小组同学进行如下实验操作并观察到对应现象:
(3)iv中反应的离子方程式是___________
(4)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
Ⅲ.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b.SCN-被转化
(5)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(6)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________
Ⅰ.探究FeCl2溶液的性质。
(1)从化合价的角度预测,FeCl2可能具有的性质
(2)向FeCl2溶液中滴加酸性KMnO4溶液,可观察到的现象是
Ⅱ.探究FeCl3溶液的性质
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 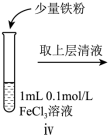 | 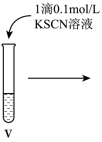 | 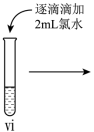 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色,而后红色褪去 |
(4)vi 中滴加氯水过程中,氯水反应的离子方程式是
Ⅲ.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b.SCN-被转化
(5)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(6)进一步预测SCN-可能被转化为SO
 ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象
您最近一年使用:0次



