名校
1 . 下列反应的离子方程式正确的是
A.少量 通入 通入 中: 中: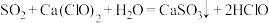 |
B.向二元弱酸 溶液中滴入足量烧碱溶液: 溶液中滴入足量烧碱溶液: |
C. 溶于HI溶液: 溶于HI溶液: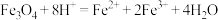 |
D.向含 的溶液通入标准状况下 的溶液通入标准状况下 : : |
您最近一年使用:0次
2 . 部分含铁物质的分类与相应铁元素的化合价关系如图。下列说法不正确的是
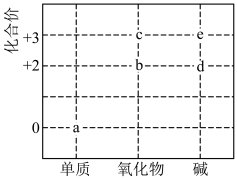
| A.b可被还原为a | B.d在空气中可被还原为e |
| C.一定条件下a能与水蒸气反应 | D.c溶于盐酸后所得溶液能使KSCN溶液变红 |
您最近一年使用:0次
3 . 铁是目前产量最大且使用最广泛的金属。下列含铁物质与其用途不匹配的是
| 选项 | 物质 | 用途 |
| A | Fe合金 | 高铁铁轨 |
| B | FeO | 涂料中的红色颜料 |
| C |  | 磁性材料 |
| D |  | 营养强化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
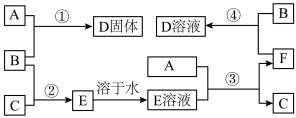
4 . 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按下面框图进行反应.又知D溶液为棕黄色,E溶液为无色,请回答:______ ,B是______ ,C是______ (填写化学式);
(2)反应①的化学方程式为______ ;
(3)反应④的化学方程式为______ ;
(4)往D的水溶液中滴加NaOH溶液,现象为______ ;
(5)检验D的水溶液中阳离子需要的试剂为______ ,现象为______ 。
(2)反应①的化学方程式为
(3)反应④的化学方程式为
(4)往D的水溶液中滴加NaOH溶液,现象为
(5)检验D的水溶液中阳离子需要的试剂为
您最近一年使用:0次
5 . 化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。
仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
(2)在实验②中,有部分同学在氯化亚铁溶液中滴入  溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:___________ ;你对实验员在配制氯化亚铁溶液时,提出的建议是___________ 。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、
 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
| 序号 | 实验设计 | 实验现象 | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴入稀硫酸 | 铁粉溶解,溶液由无色变成浅绿色,生成无色无味气体 | 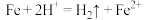 |  具有还原性 具有还原性 |
| ② |  溶液中滴入 溶液中滴入  溶液,再加氯水 溶液,再加氯水 | 滴入 溶液无明显变化,加入氯水立即变成红色 溶液无明显变化,加入氯水立即变成红色 | ||
| ③ |  溶液中加入锌片 溶液中加入锌片 |  | ||
| ④ |  |  具有氧化性 具有氧化性 |
 溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:
您最近一年使用:0次
名校
6 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液 | 溶液颜色变红 | 溶液X含有Fe2+ |
| B | 向饱和的Na2CO3溶液通入CO2 | 产生白色沉淀 | 溶解度:NaHCO3<Na2CO3 |
| C | 向CaCl2溶液中通入适量CO2 | 产生白色沉淀 | 白色沉淀为CaCO3 |
| D | 向FeCl3溶液滴加少量酸性KMnO4溶液以检验FeCl2杂质 | 紫红色褪去 | 混合溶液中有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 健康人体内含铁元素大约 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:_______ ,试剂2的化学式为_______ 。
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是_______ 。
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:_______ ,现象为_______ 。
 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验: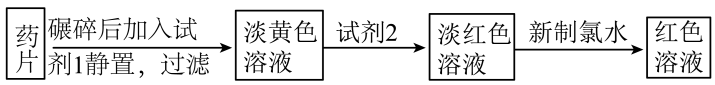
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的
 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:
您最近一年使用:0次
8 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.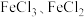 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近一年使用:0次
9 . 下图是一种综合处理SO2废气的工艺流程。下列说法正确的是
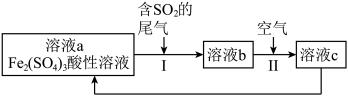
| A.操作Ⅱ发生反应的离子方程式为:2Fe2++4H++O2=2Fe3++2H2O |
| B.溶液b中阳离子只有Fe2+ |
| C.溶液a转化为溶液b的反应中,SO2被氧化 |
| D.加入FeO可以使溶液c转化为溶液a |
您最近一年使用:0次
名校
解题方法
10 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀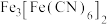 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
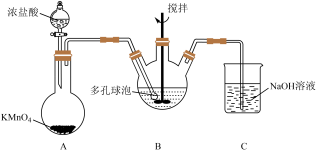
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀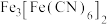 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次



