名校
解题方法
1 . 一种利用磁铁矿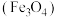 制备铁红的流程如下:
制备铁红的流程如下:
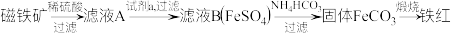
下列说法正确的是
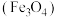 制备铁红的流程如下:
制备铁红的流程如下: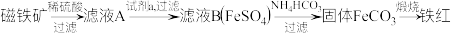
下列说法正确的是
| A.往滤液A中滴加少量酸性KMnO4溶液,可观察到紫红色褪去 |
B.可以用KSCN溶液和氯水检验滤液A中是否有 |
C.FeCO3在空气中煅烧的反应方程式为 |
| D.最终得到铁红中的Fe元素的质量小于原磁铁矿中的Fe元素的质量 |
您最近一年使用:0次
名校
解题方法
2 . 铁是人类使用最早的金属之一。运用所学知识,回答下列问题:
(1)电子工业用FeCl3,溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的化学方程式为______ 。
(2)某研究性学习小组为测定FeCl3溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有______ 。
②验证该溶液中是否含有Fe2+,正确的实验方法是______ (填序号)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液先滴入双氧水再滴入KSCN溶液,若溶液显红色,证明原溶液中含有Fe2+
D.取适量溶液,滴入K3[Fe(CN)6]溶液,若产生蓝色沉淀,证明含有Fe2+
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得FeCl3,溶液,设计如下方案:______ 。
②向滤液B和滤液E中通入F的目的是______ ,该反应的离子方程式为______ 。
③向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是______ (填序号)。
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
(1)电子工业用FeCl3,溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的化学方程式为
(2)某研究性学习小组为测定FeCl3溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有
②验证该溶液中是否含有Fe2+,正确的实验方法是
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液先滴入双氧水再滴入KSCN溶液,若溶液显红色,证明原溶液中含有Fe2+
D.取适量溶液,滴入K3[Fe(CN)6]溶液,若产生蓝色沉淀,证明含有Fe2+
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得FeCl3,溶液,设计如下方案:
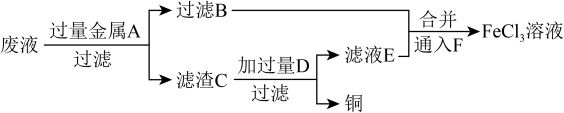
②向滤液B和滤液E中通入F的目的是
③向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
您最近一年使用:0次
名校
3 . 下列各组离子在给定条件下能大量共存的是
A.含有大量ClO‒的溶液:K+、H+、Cl‒、SO |
B.澄清透明的溶液中:Cu2+、Na+、SO 、NO 、NO |
C.遇铝能产生H2的溶液:NH 、K+、Cl‒、CO 、K+、Cl‒、CO |
D.使紫色石蕊溶液呈红色的溶液:Mg2+、Fe2+、SO 、NO 、NO |
您最近一年使用:0次
2024-05-27更新
|
245次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
解题方法
4 . 硫酸亚铁晶体 在医药上作补血剂。某课外小组取10片补血剂总质量wg,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量wg,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(1)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加___________ 后,溶液变为红色,证实了怀疑。
(2)步骤②反应的离子方程式为___________ ,下列物质中可以用来代替该步骤中的 是
是___________ (填序号)。
① 溶液②氯水③稀盐酸④碳酸钠
溶液②氯水③稀盐酸④碳酸钠
(3)服用维生素C可使食物中的 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的___________ 性。假设实验中的损耗忽略不计,则该补血剂含铁元素的质量分数为___________ 。
 在医药上作补血剂。某课外小组取10片补血剂总质量wg,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量wg,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(1)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加
(2)步骤②反应的离子方程式为
 是
是①
 溶液②氯水③稀盐酸④碳酸钠
溶液②氯水③稀盐酸④碳酸钠(3)服用维生素C可使食物中的
 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的
您最近一年使用:0次
5 . “协同去污,变废为宝”为处理工业废水提供了新思路。现有含 、
、 的电镀废液以及含
的电镀废液以及含 的废液。现联合处理废水,回收
的废液。现联合处理废水,回收 并生产铁红和媒染剂
并生产铁红和媒染剂 ,回收过程如下,请回答以下问题:
,回收过程如下,请回答以下问题:________ 。
(2)对于该工艺的说法错误的是________。
(3)写出铁铜废液中加入试剂1发生的离子方程式________ 。滤液与含酸性 的废液反应的离子方程式为
的废液反应的离子方程式为________ 。
(4)证明滤液已被试剂3完全氧化的实验方法是________ 。
(5)从 溶液制取
溶液制取 晶体的实验操作方法为蒸发浓缩、
晶体的实验操作方法为蒸发浓缩、________ 、过滤、________ 、干燥。
(6)已知 化学性质与
化学性质与 类似,若将流程中
类似,若将流程中 的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为________ 。
 、
、 的电镀废液以及含
的电镀废液以及含 的废液。现联合处理废水,回收
的废液。现联合处理废水,回收 并生产铁红和媒染剂
并生产铁红和媒染剂 ,回收过程如下,请回答以下问题:
,回收过程如下,请回答以下问题: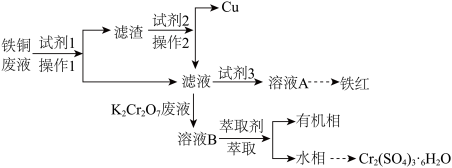
(2)对于该工艺的说法错误的是________。
| A.操作1和操作2都是过滤 |
B.试剂1是过量的 粉,试剂2是过量的 粉,试剂2是过量的 |
| C.可从有机相中提取出某成分加入到溶液A中,提高产量,剩余成分可循环利用 |
D.试剂3只能是 ,目的是将 ,目的是将 氧化成 氧化成 |
(3)写出铁铜废液中加入试剂1发生的离子方程式
 的废液反应的离子方程式为
的废液反应的离子方程式为(4)证明滤液已被试剂3完全氧化的实验方法是
(5)从
 溶液制取
溶液制取 晶体的实验操作方法为蒸发浓缩、
晶体的实验操作方法为蒸发浓缩、(6)已知
 化学性质与
化学性质与 类似,若将流程中
类似,若将流程中 的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
您最近一年使用:0次
名校
6 . 下列有关离子(或物质)的检验、现象及结论,都正确的是
| A.向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色,该溶液中一定含有Fe2+ |
| B.向某溶液中滴加KSCN溶液,溶液变成红色,该溶液中一定不存在Fe2+ |
| C.将某种铁的氧化物溶于足量的稀硫酸中,取其溶液滴加酸性KMnO4溶液,振荡,溶液褪色,原氧化物中含有+2价铁 |
| D.向久置的FeCl2溶液中滴入用硫酸酸化的H2O2溶液,溶液变黄,滴加KSCN溶液,溶液变成红色,说明发生氧化还原反应,且氧化性:H2O2<Fe3+ |
您最近一年使用:0次
7 . 黄铁矿(主要成分 ,含杂质
,含杂质 )是工业制硫酸的重要原料,还可用来制备绿矾晶体(
)是工业制硫酸的重要原料,还可用来制备绿矾晶体( ),工艺流程如下:
),工艺流程如下:______ 。
(2)试剂A为______ (写化学式),操作Ⅰ所用玻璃仪器为烧杯、______ 。
(3)结合下图,若想得到 ,“操作2”过程为蒸发浓缩,
,“操作2”过程为蒸发浓缩,______ ,过滤,……;母液放置在空气中一段时间,应返回“______ ”工序循环使用
ⅰ.快速称取样品 ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
ⅱ.向ⅰ所得溶液中滴加足量 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。
根据实验数据,样品中
______ (用含a,b的代数式表示),若样品溶于水后在空气中放置时间过长,测定结果将______ (填“偏大”、“偏小”或“无影响”)。
 ,含杂质
,含杂质 )是工业制硫酸的重要原料,还可用来制备绿矾晶体(
)是工业制硫酸的重要原料,还可用来制备绿矾晶体( ),工艺流程如下:
),工艺流程如下: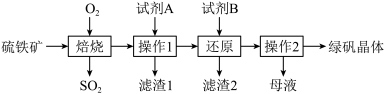
(2)试剂A为
(3)结合下图,若想得到
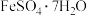 ,“操作2”过程为蒸发浓缩,
,“操作2”过程为蒸发浓缩,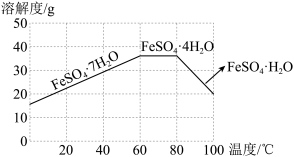
ⅰ.快速称取样品
 ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。ⅱ.向ⅰ所得溶液中滴加足量
 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。根据实验数据,样品中

您最近一年使用:0次
8 . 某中学趣味化学实验小组的同学想通过“ 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.
实验一:验证 的还原性
的还原性
(1)红棕色气体是____________ 。(写化学式)
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明___________________ 。
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的 或NO与溶液中的
或NO与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。
【实验与探究】
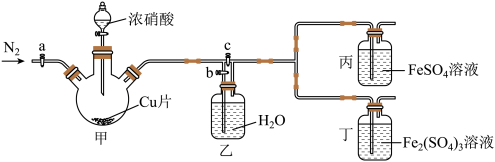
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅱ.向甲中加入适量浓 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。
(3)通入 的目的是
的目的是________________________ 。
(4)铜与浓硝酸反应的离子方程式是__________________________ 。
(5)装置乙的作用是_____________________ 。
(6)实验结论:溶液的深棕色可能是因为 。
【反思与改进】
实验三:验证 的还原性
的还原性
(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有____________ 的试管中滴入几滴____________ ,振荡。
 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.实验一:验证
 的还原性
的还原性实验操作 | 预期现象 | 实验现象 |
向盛有2mL  溶液的试管中,滴入几滴浓硝酸,振荡。 溶液的试管中,滴入几滴浓硝酸,振荡。 | 试管中产生红棕色气体,溶液变为黄色。 | 试管中产生红棕色气体,溶液变为深棕色。 |
(1)红棕色气体是
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的
 或NO与溶液中的
或NO与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。【实验与探究】
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅱ.向甲中加入适量浓
 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓
 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。(3)通入
 的目的是
的目的是(4)铜与浓硝酸反应的离子方程式是
(5)装置乙的作用是
(6)实验结论:溶液的深棕色可能是因为 。
A. 与NO发生了反应 与NO发生了反应 | B. 与 与 发生了反应 发生了反应 |
C. 与NO发生了反应 与NO发生了反应 | D. 与 与 发生了反应 发生了反应 |
【反思与改进】
实验三:验证
 的还原性
的还原性(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有
您最近一年使用:0次
9 . 下列物质放置在空气中易变质,因发生氧化反应而变质的是
| A.Na2O2 | B.NaOH | C.FeCl2 | D.NaClO |
您最近一年使用:0次
10 . 实验室通过下列过程制取草酸亚铁晶体。
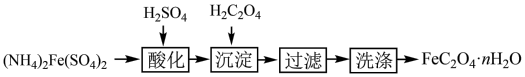
A.“酸化”后的溶液,根据电荷守恒存在等量关系:n( )+2×n(Fe2+)=2×n( )+2×n(Fe2+)=2×n( ) ) |
B.“沉淀”时发生反应的离子方程式:Fe2++ +nH2O=FeC2O4·nH2O↓ +nH2O=FeC2O4·nH2O↓ |
| C.可以用酸性KMnO4溶液检验“沉淀”后的上层清液中是否含有Fe2+ |
| D.“洗涤”时先水洗,再用乙醇洗涤,有利于晶体快速干燥和防止失去结晶水 |
您最近一年使用:0次



