1 . 亚硫酸钠(Na2SO3)受热会分解,它在有H2O存在时容易被空气中的氧气氧化为硫酸钠(Na2SO4)。实验室贮存亚硫酸钠的试剂瓶极易炸裂,你推测其原因可能是:①___________ ;②__________________ ;
您最近一年使用:0次
名校
解题方法
2 . 下列各组离子,在强碱性溶液中可以大量共存的是
A.K+、Na+、HSO | B.Ba2+、SO 、NO 、NO | C.NH 、Cl—、NO 、Cl—、NO | D.K+、Na+、ClO— |
您最近一年使用:0次
解题方法
3 . 长期存放的亚硫酸钠可能会被空气中的氧气氧化(2Na2SO3+O2=2Na2SO4)。某化学兴趣小组通过实验来测定某无水亚硫酸钠试剂的质量分数,设计了如图所示实验装置:
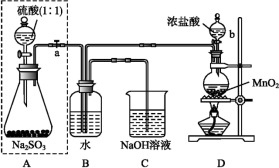
请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?______
(2)D装置中反应的化学方程式为______ ,B装置中反应的离子方程式为______
(3)称量a g Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀b g,原样品中Na2SO3的质量分数为______
(4)为保证实验测定的准确性,A中的硫酸什么时候滴加___________
(5)C装置中NaOH的作用是___________
(6)现有以下试剂:蒸馏水、稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法测定试样中亚硫酸钠的质量分数:___________

请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?
(2)D装置中反应的化学方程式为
(3)称量a g Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀b g,原样品中Na2SO3的质量分数为
(4)为保证实验测定的准确性,A中的硫酸什么时候滴加
(5)C装置中NaOH的作用是
(6)现有以下试剂:蒸馏水、稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法测定试样中亚硫酸钠的质量分数:
您最近一年使用:0次
21-22高一上·江苏镇江·期末
4 . 下列反应能产生SO2的是
①煅烧硫铁矿;②亚硫酸钠与硫酸反应;③点燃硫化氢气体;④蔗糖和浓硫酸反应
①煅烧硫铁矿;②亚硫酸钠与硫酸反应;③点燃硫化氢气体;④蔗糖和浓硫酸反应
| A.①②③ | B.②④ | C.②③④ | D.①②③④ |
您最近一年使用:0次
5 . 物质的类别和核心元素的化合价是研究物质性质的两个重要维度。右图为硫及其部分 化合物的“价类二维图'',下列说法正确的是
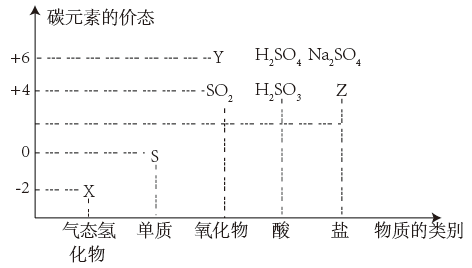

| A.S与O2在点燃下一步反应生成Y | B.Z参加氧化还原反应时只作还原剂 |
| C.X、Y属于非电解质 | D.X的水溶液在空气中放置,易被氧化 |
您最近一年使用:0次
2021-06-15更新
|
423次组卷
|
4卷引用:福建省莆田第二中学2019~2020学年高一下学期4月线上月考化学试题
福建省莆田第二中学2019~2020学年高一下学期4月线上月考化学试题海南省屯昌县2023届高三二模统考(A)化学试题(已下线)第一次月考卷?-2024年高考化学一轮复习考点通关卷(新高考通用)新疆阿克苏市实验中学2022-2023学年高一下学期期末考试化学试题
20-21高一下·浙江·阶段练习
6 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 常温下将铁片放入浓硝酸,无明显现象 | 铁与浓硝酸不反应 |
| B | 将某气体通入酸性KMnO4溶液,溶液褪色 | 该气体一定是SO2 |
| C | 向久置的Na2SO3溶液中,滴加足量盐酸,再滴加BaCl2溶液,有白色沉淀生成 | 久置的Na2SO3溶液中存在Na2SO4 |
| D | 某物质灼烧时,焰色为黄色 | 该物质中一定有钠元素,一定没有钾元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
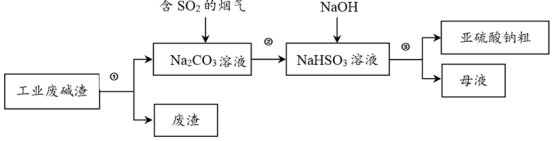
(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是_______ (写出一种即可)。
(2)过程①进行的操作是_______ 。
(3)上述流程中,加入NaOH后,发生反应的化学方程式为_______ 。
(4)亚硫酸钠粗品中含有少量Na2SO4,原因是_______ 。
(5)设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有Na2SO4。

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是
(2)过程①进行的操作是
(3)上述流程中,加入NaOH后,发生反应的化学方程式为
(4)亚硫酸钠粗品中含有少量Na2SO4,原因是
(5)设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
您最近一年使用:0次
2021-05-20更新
|
795次组卷
|
3卷引用:北京市宣武外国语实验学校2020-2021学年高一下学期期中考试化学试题
名校
解题方法
8 . 下列关于含硫化合物的叙述不正确的是
| A.将SO2通入被氨气饱和的BaCl2溶液中,有BaSO4白色沉淀生成 |
| B.白葡萄酒含维生素C等多种维生素,通常添加微量SO2的目的是防止营养成分被氧化 |
| C.Na2SO3溶液能使酸性KMnO4溶液褪色 |
| D.制备浓硫酸时,在吸收塔中用98.3%的浓硫酸吸收SO3 |
您最近一年使用:0次
2021·广东·模拟预测
解题方法
9 . 物质的类别和核心元素的化合价是研究物质性质的重要视角。以硫及其化合物的类别和价态变化为坐标的二维转化关系如图所示:

下列说法错误的是

下列说法错误的是
| A.用BaCl2溶液可鉴别c和d |
| B.常温下,a和f的浓溶液反应可生成b和c |
| C.向e的水溶液中滴加几滴紫色石蕊试液,溶液先变红后褪色 |
| D.常温下,等物质的量浓度的g、h两种钠盐溶液的pH:g>h |
您最近一年使用:0次
10 . 检验某未知液中是否含有SO 的下列操作最合理的是
的下列操作最合理的是
 的下列操作最合理的是
的下列操作最合理的是| A.加入硝酸酸化了的硝酸钡溶液,有白色沉淀生成 |
| B.加入盐酸酸化了的氯化钡溶液,有白色沉淀生成 |
| C.先加硝酸酸化,无沉淀,再加硝酸钡溶液,有白色沉淀生成 |
| D.先加盐酸酸化,无沉淀,再加氯化钡溶液,有白色沉淀生成 |
您最近一年使用:0次



