22. 硫酸亚铁铵[(NH
4)
2Fe(SO
4)
2·6H
2O]又名摩尔盐,是一种浅绿色晶体,易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,接近100℃时易失去结晶水,是分析化学中的重要试剂。某研究性学习小组用图所示的实验装置来制取摩尔盐。
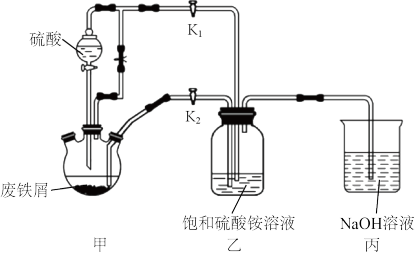
实验步骤如下:
①检查装置的气密性。
②往三颈烧瓶中依次加入过量的废铁屑(含杂质氧化铁和硫化亚铁)。
③关闭止水夹K
2、打开K
1,打开分液漏斗的旋塞并控制好滴速。
④把三颈烧瓶中的液体转移到装置乙中,当出现大量浅绿色晶体时,关闭分液漏斗的旋塞。
⑤将装置乙中所得晶体快速过滤.洗涤和干燥,得到产品。
回答下列问题:
(1)实验前需将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑。以下仪器中完成该操作不需要的有
__________(填编号)。
①铁架台②玻璃棒③普通漏斗 ④ 棉网⑤烧杯⑥通精灯⑦蒸发皿
(2)废铁屑中的杂质氧化铁和硫化亚铁无需在实验前除去,理由是(用离子方程式表示):
_____________。(3)步骤③向装置乙中通入氢气,通入氢气的目的是:
___________________装置丙中NaOH溶液的作用是
____________(4)通过调节K
1、K
2的开关可实现步骤④中三颈烧瓶中液体自动转移至装置乙中,具体的实验操作为
____________;
(5)产品中NH

、Fe
2+的检测。
①NH

的定性检测:取少量产品于试管中,加水溶解,
_____(填操作及现象),证明产品中含有NH

。
②测定产品中Fe
2+的含量:称取10.0g产品,溶于水,加入足量NaOH溶液过滤、洗涤灼烧、冷却、称量。重复灼烧、冷却、称影直到最后两次的质量相等为止。称得最终固体质量为2.0g)则产品中Fe
2+的质量分数为
___________(保留两位有效数字)