名校
1 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是___________ (写出一种即可)。
(2)将碳酸钠溶液吸收烟气中的SO2的化学方程式补充完整:___________ 。
SO2+Na2CO3+______=NaHSO3+CO2
(3)上述流程中,加入NaOH后,发生反应的化学方程式为___________ 。
(4)亚硫酸钠(Na2SO3)中硫的化合价是___________ 。亚硫酸钠粗品中常含有少量的硫酸钠,可能的原因是___________ 。

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是
(2)将碳酸钠溶液吸收烟气中的SO2的化学方程式补充完整:
SO2+Na2CO3+______=NaHSO3+CO2
(3)上述流程中,加入NaOH后,发生反应的化学方程式为
(4)亚硫酸钠(Na2SO3)中硫的化合价是
您最近一年使用:0次
名校
解题方法
2 . 设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。
ⅱ. 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。
某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,
溶液,___________ (填实验现象)。
上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是___________
(3)写出NO与碱性 溶液反应的离子方程式
溶液反应的离子方程式___________
(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: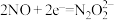 ,则氧化反应为:
,则氧化反应为:___________ 。
(5)某同学结合所学知识设计处理工业废气中 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式___________
②再向生成的溶液中加入一定量___________ ,以此溶液来吸收NO气体。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性
 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。资料:ⅰ.NO与碱性
 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。ⅱ.
 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和
 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴
 的
的 溶液,
溶液,上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是
(3)写出NO与碱性
 溶液反应的离子方程式
溶液反应的离子方程式(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性
 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: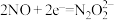 ,则氧化反应为:
,则氧化反应为:(5)某同学结合所学知识设计处理工业废气中
 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。①先用饱和纯碱溶液吸收废气中的
 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式②再向生成的溶液中加入一定量
您最近一年使用:0次
3 . 实验室用浓硫酸与铜丝加热生成的 制备少量
制备少量 并检验性质。
并检验性质。 并检验性质
并检验性质
操作及现象:点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,试管ⅲ中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。
(1)ⅰ中发生反应的化学方程式为_______ 。
(2)ⅱ中现象说明 具有
具有_______ 作用。
(3)若将试管ⅲ与试管ⅱ位置互换,石蕊溶液变为红色能否作为 是酸性氧化物的证据?说明理由:
是酸性氧化物的证据?说明理由:_______ 。
Ⅱ.制备 并检验性质
并检验性质
(4)ⅳ中反应的离子方程式为_______ 。
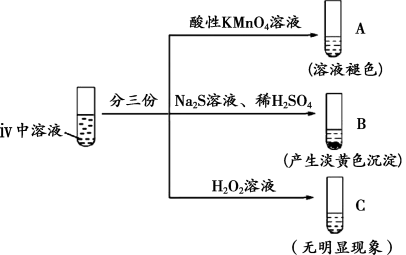
(5)进行实验: 具有
具有_______ 性。
②B中产生淡黄色沉淀的离子方程式为_______ 。
③C中无明显现象,甲同学通过检测 的生成证明
的生成证明 和
和 发生反应:取1
发生反应:取1 C中溶液于试管中,
C中溶液于试管中,_______ (填试剂和操作),产生白色沉淀。
乙同学认为甲同学的实验没有排除 的影响,设计对比实验:
的影响,设计对比实验:_______ 。
综合甲、乙同学的实验可知, 能将
能将 氧化。
氧化。
 制备少量
制备少量 并检验性质。
并检验性质。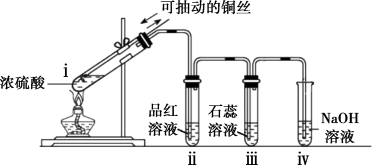
 并检验性质
并检验性质操作及现象:点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,试管ⅲ中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。
(1)ⅰ中发生反应的化学方程式为
(2)ⅱ中现象说明
 具有
具有(3)若将试管ⅲ与试管ⅱ位置互换,石蕊溶液变为红色能否作为
 是酸性氧化物的证据?说明理由:
是酸性氧化物的证据?说明理由:Ⅱ.制备
 并检验性质
并检验性质(4)ⅳ中反应的离子方程式为
(5)进行实验:
 具有
具有②B中产生淡黄色沉淀的离子方程式为
③C中无明显现象,甲同学通过检测
 的生成证明
的生成证明 和
和 发生反应:取1
发生反应:取1 C中溶液于试管中,
C中溶液于试管中,乙同学认为甲同学的实验没有排除
 的影响,设计对比实验:
的影响,设计对比实验:综合甲、乙同学的实验可知,
 能将
能将 氧化。
氧化。
您最近一年使用:0次
2022-07-10更新
|
743次组卷
|
4卷引用:北京市第五十五中学2022-2023学年高一下学期5月期中考试化学试题
4 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
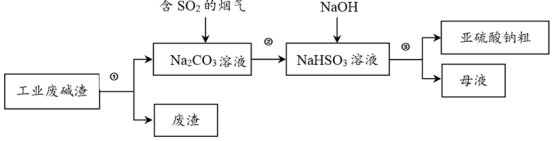
(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是_______ (写出一种即可)。
(2)过程①进行的操作是_______ 。
(3)上述流程中,加入NaOH后,发生反应的化学方程式为_______ 。
(4)亚硫酸钠粗品中含有少量Na2SO4,原因是_______ 。
(5)设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有Na2SO4。

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是
(2)过程①进行的操作是
(3)上述流程中,加入NaOH后,发生反应的化学方程式为
(4)亚硫酸钠粗品中含有少量Na2SO4,原因是
(5)设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
您最近一年使用:0次
2021-05-20更新
|
795次组卷
|
3卷引用:北京市宣武外国语实验学校2020-2021学年高一下学期期中考试化学试题
5 . 亚硫酸盐是一种常见的食品添加剂。为检验某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量计),某研究小组同学设计了如下实验流程(所加试剂均为足量)。

请回答:
(1)亚硫酸盐作为食品添加剂的作用是________ (填字母)。
a.防腐保鲜 b.增强营养
(2)反应①中通入N2的目的是_________ (填字母)。
a.冷却产生的气体
b.与生成的气体反应
c.将生成的气体全部赶出
(3)反应①~③中属于氧化还原反应的是________ (填序号)。
(4)若取样品X g,反应③消耗0.01 mol/L NaOH溶液100 mL,则1 kg样品中含SO2的质量是________ g(用含X的代数式表示)。

请回答:
(1)亚硫酸盐作为食品添加剂的作用是
a.防腐保鲜 b.增强营养
(2)反应①中通入N2的目的是
a.冷却产生的气体
b.与生成的气体反应
c.将生成的气体全部赶出
(3)反应①~③中属于氧化还原反应的是
(4)若取样品X g,反应③消耗0.01 mol/L NaOH溶液100 mL,则1 kg样品中含SO2的质量是
您最近一年使用:0次
2016-12-09更新
|
242次组卷
|
2卷引用:2014-2015北京市66中高二上学期期中考试化学(文)试卷



