1 . “事物的双方既相互对立又相互统一”的哲学观点在化学中有着诸多体现。
Ⅰ.硫和氮两种元素与人们的生活密切相关,自然界中硫、氮的循环是维持生态平衡的重要物质基础。
(1)下列说法错误的是______(填标号)。
(2)一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:
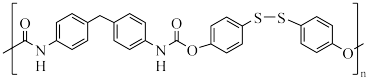
该聚合物由X(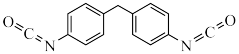 )和Y(
)和Y(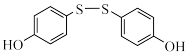 )聚合而成,下列说法正确的是______(填标号)。
)聚合而成,下列说法正确的是______(填标号)。
Ⅱ.含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。
(3)二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:ⅰ

ⅱ
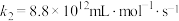
脱硫:ⅲ

ⅳ

其中k为速率常数。对于基元反应: ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。

①其它因素都相同时,ClO2氧化SO2的活化能______ (填“>”或“<”)ClO2氧化NO的活化能。
②请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由:______ 。
(4)CO也可以与NO反应生成无污染物: 。
。
已知:ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数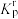 。
。
ⅱ 气体的相对分压等于其分压(单位为kPa)除以 (
(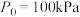 )。
)。
在某温度下,原料组成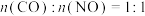 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
______ 。
(5)污水中的硝基苯可用铁炭混合物在酸性条件下处理。硝基苯转化过程如下:

①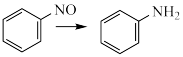 的电极反应式为
的电极反应式为______ 。
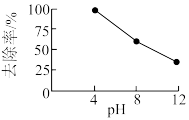
②其他条件一定,相同时间内,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的去除率越低的原因可能是______ 。
Ⅰ.硫和氮两种元素与人们的生活密切相关,自然界中硫、氮的循环是维持生态平衡的重要物质基础。
(1)下列说法错误的是______(填标号)。
| A.合成氨很大程度上解决了地球上因粮食不足而导致的饥饿问题 |
| B.组成生命体的蛋白质中含有硫和氮 |
| C.豆科植物的根瘤菌可实现自然固氮 |
| D.二氧化硫有毒,不可用作食品添加剂 |
(2)一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:

该聚合物由X(
 )和Y(
)和Y( )聚合而成,下列说法正确的是______(填标号)。
)聚合而成,下列说法正确的是______(填标号)。| A.X中碳氧双键比碳氮双键更容易与Y发生反应 |
| B.生成该聚合物反应的原子利用率为100% |
| C.其自修复性可能与—S—S—有关 |
| D.废弃的聚合物直接焚烧处理即可 |
Ⅱ.含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。
(3)二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:ⅰ


ⅱ

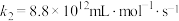
脱硫:ⅲ


ⅳ


其中k为速率常数。对于基元反应:
 ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。

①其它因素都相同时,ClO2氧化SO2的活化能
②请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由:
(4)CO也可以与NO反应生成无污染物:
 。
。已知:ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数
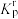 。
。ⅱ 气体的相对分压等于其分压(单位为kPa)除以
 (
(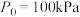 )。
)。在某温度下,原料组成
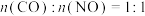 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
(5)污水中的硝基苯可用铁炭混合物在酸性条件下处理。硝基苯转化过程如下:

①
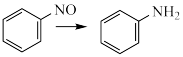 的电极反应式为
的电极反应式为②其他条件一定,相同时间内,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的去除率越低的原因可能是

您最近一年使用:0次
解题方法
2 . 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
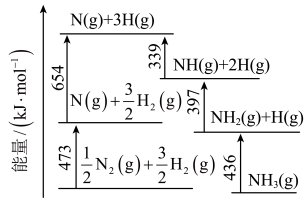
(1)根据下图数据计算反应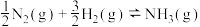

________  。
。
(2)合成氨工厂以“水煤气”和 为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、
为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、 、
、 、
、 的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为
的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为
 ,装置如图。
,装置如图。
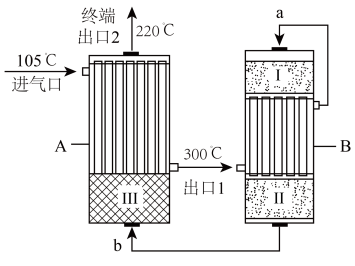
①温度比较:气流a_______ 气流b(填“>”“<”或“=”)。
②气体流速一定,经由催化剂Ⅰ到催化剂Ⅱ,原料转化率有提升,其可能原因是:_______ 。
③下列说法正确的是_______ 。
A.合成氨是目前自然固氮最重要的途径
B.利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气流速,有利于水煤气生成
C.体系温度升高,可能导致催化剂失活,用热交换器将原料气可预热并使反应体系冷却
D.终端出口2得到的气体,通过液化可分离出
(3)LiH-3d过渡金属复合催化剂也可用于催化合成氨,已知 先被吸附发生反应
先被吸附发生反应
 ,紧接着
,紧接着 被吸附发生的反应方程式
被吸附发生的反应方程式___________ 。
(4)工业上常用甲烷水蒸气重整制备所得的氢气用于合成氨的原料,体系中发生如下反应。
Ⅰ.
Ⅱ.
恒温恒压条件下,1mol (g)和1mol
(g)和1mol  (g)反应达平衡时,
(g)反应达平衡时, (g)的转化率为m,
(g)的转化率为m, (g)的物质的量为n mol,则反应Ⅰ的平衡常数
(g)的物质的量为n mol,则反应Ⅰ的平衡常数
___________ (写出含有m、n的计算式;对于反应 ,
,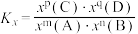 ,x为物质的量分数)。
,x为物质的量分数)。
(1)根据下图数据计算反应
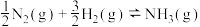

 。
。
(2)合成氨工厂以“水煤气”和
 为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、
为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、 、
、 、
、 的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为
的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为
 ,装置如图。
,装置如图。
①温度比较:气流a
②气体流速一定,经由催化剂Ⅰ到催化剂Ⅱ,原料转化率有提升,其可能原因是:
③下列说法正确的是
A.合成氨是目前自然固氮最重要的途径
B.利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气流速,有利于水煤气生成
C.体系温度升高,可能导致催化剂失活,用热交换器将原料气可预热并使反应体系冷却
D.终端出口2得到的气体,通过液化可分离出

(3)LiH-3d过渡金属复合催化剂也可用于催化合成氨,已知
 先被吸附发生反应
先被吸附发生反应
 ,紧接着
,紧接着 被吸附发生的反应方程式
被吸附发生的反应方程式(4)工业上常用甲烷水蒸气重整制备所得的氢气用于合成氨的原料,体系中发生如下反应。
Ⅰ.

Ⅱ.

恒温恒压条件下,1mol
 (g)和1mol
(g)和1mol  (g)反应达平衡时,
(g)反应达平衡时, (g)的转化率为m,
(g)的转化率为m, (g)的物质的量为n mol,则反应Ⅰ的平衡常数
(g)的物质的量为n mol,则反应Ⅰ的平衡常数
 ,
,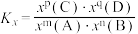 ,x为物质的量分数)。
,x为物质的量分数)。
您最近一年使用:0次
名校
解题方法
3 . 近日,大连理工大学在《ACS Catal》发文称:合成了一种B/N共掺杂多孔碳纳米管负载的Mo单原子位点(Mo/BCN),该材料在室温下能将 高效电还原为
高效电还原为 。相关机理如下如图2所示(图1为碳纳米管):
。相关机理如下如图2所示(图1为碳纳米管):
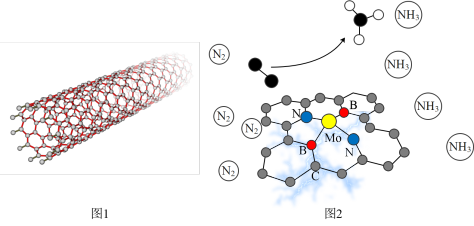
下列叙述不正确 的是
 高效电还原为
高效电还原为 。相关机理如下如图2所示(图1为碳纳米管):
。相关机理如下如图2所示(图1为碳纳米管):
下列叙述
| A.碳纳米管是一种新型非金属材料 |
| B.碳纳米管掺杂B、N的过程属于物理变化 |
C.该材料能降低 成为活化分子所需要的能量 成为活化分子所需要的能量 |
| D.该过程属于氮的固定中的人工固氮 |
您最近一年使用:0次
2023-01-08更新
|
216次组卷
|
2卷引用:广东省湛江一中、深圳实验两校三部2023届高三1月期末联考化学试题
4 . 氨基磺酸(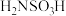 )是一元固体强酸,俗称“固体硫酸”,易溶于水和液氨,不溶于乙醇,溶于水时有存在如下反应:
)是一元固体强酸,俗称“固体硫酸”,易溶于水和液氨,不溶于乙醇,溶于水时有存在如下反应: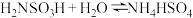 。在工业上常用作酸性清洗剂、阻燃剂、磺化剂等。某实验室用尿素和发烟硫酸(溶有
。在工业上常用作酸性清洗剂、阻燃剂、磺化剂等。某实验室用尿素和发烟硫酸(溶有 的硫酸)制备氨基磺酸的流程如图:
的硫酸)制备氨基磺酸的流程如图:
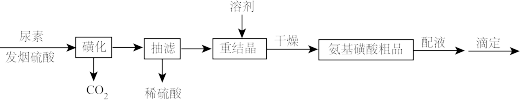
已知“磺化”步骤发生的反应为:
①

②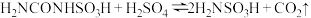
发生“磺化”步骤反应的装置如图所示:请回答下列问题:

(1)下列关于“磺化”与“抽滤”步骤的说法中正确的是_______ 。
A.仪器a的名称是三颈烧瓶
B.冷凝回流时,冷凝水应该从冷凝管的B管口通入
C.抽滤操作前,应先将略小于漏斗内径却又能将全部小孔盖住的滤纸平铺在布氏漏斗中,稍稍润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
D.抽滤结束后为了防止倒吸,应先关闭水龙头,再拆下连接抽气泵和吸滤瓶之间的橡皮管
(2)“磺化”过程温度与产率的关系如图所示,控制反应温度为75~80℃为宜,若温度高于80℃,氨基磺酸的产率会降低,可能的原因是_______ 。

(3)“抽滤”时,所得晶体要用乙醇洗涤,则洗涤的具体操作是_______ 。
(4)“重结晶”时,溶剂选用10%~12%的硫酸而不用蒸馏水的原因是_______ 。
(5)“配液及滴定”操作中,准确称取2.500g氨基磺酸粗品配成250mL待测液。取25.00mL待测液于锥形瓶中,以淀粉-碘化钾溶液做指示剂,用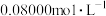 的
的 标准溶液进行滴定,当溶液恰好变蓝时,消耗
标准溶液进行滴定,当溶液恰好变蓝时,消耗 标准溶液25.00mL。此时氨基磺酸恰好被完全氧化成
标准溶液25.00mL。此时氨基磺酸恰好被完全氧化成 ,
, 的还原产物也为
的还原产物也为 。
。
①电子天平使用前须通电预热并调零校准。称量时,可先将洁净干燥的小烧杯放在称盘中央,显示数字稳定后按归零键,再缓缓加样品至所需质量时,停止加样,读数记录。
②试求氨基磺酸粗品的纯度:_______ (用质量百分数表示)。
③若以酚酞为指示剂,用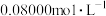 的NaOH标准溶液进行滴定,也能测定氨基磺酸粗品的纯度,但测得结果通常比
的NaOH标准溶液进行滴定,也能测定氨基磺酸粗品的纯度,但测得结果通常比 法
法_______ (填“偏高”或“偏低”)。
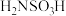 )是一元固体强酸,俗称“固体硫酸”,易溶于水和液氨,不溶于乙醇,溶于水时有存在如下反应:
)是一元固体强酸,俗称“固体硫酸”,易溶于水和液氨,不溶于乙醇,溶于水时有存在如下反应: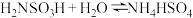 。在工业上常用作酸性清洗剂、阻燃剂、磺化剂等。某实验室用尿素和发烟硫酸(溶有
。在工业上常用作酸性清洗剂、阻燃剂、磺化剂等。某实验室用尿素和发烟硫酸(溶有 的硫酸)制备氨基磺酸的流程如图:
的硫酸)制备氨基磺酸的流程如图:
已知“磺化”步骤发生的反应为:
①


②
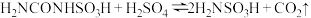
发生“磺化”步骤反应的装置如图所示:请回答下列问题:

(1)下列关于“磺化”与“抽滤”步骤的说法中正确的是
A.仪器a的名称是三颈烧瓶
B.冷凝回流时,冷凝水应该从冷凝管的B管口通入
C.抽滤操作前,应先将略小于漏斗内径却又能将全部小孔盖住的滤纸平铺在布氏漏斗中,稍稍润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
D.抽滤结束后为了防止倒吸,应先关闭水龙头,再拆下连接抽气泵和吸滤瓶之间的橡皮管
(2)“磺化”过程温度与产率的关系如图所示,控制反应温度为75~80℃为宜,若温度高于80℃,氨基磺酸的产率会降低,可能的原因是

(3)“抽滤”时,所得晶体要用乙醇洗涤,则洗涤的具体操作是
(4)“重结晶”时,溶剂选用10%~12%的硫酸而不用蒸馏水的原因是
(5)“配液及滴定”操作中,准确称取2.500g氨基磺酸粗品配成250mL待测液。取25.00mL待测液于锥形瓶中,以淀粉-碘化钾溶液做指示剂,用
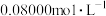 的
的 标准溶液进行滴定,当溶液恰好变蓝时,消耗
标准溶液进行滴定,当溶液恰好变蓝时,消耗 标准溶液25.00mL。此时氨基磺酸恰好被完全氧化成
标准溶液25.00mL。此时氨基磺酸恰好被完全氧化成 ,
, 的还原产物也为
的还原产物也为 。
。①电子天平使用前须通电预热并调零校准。称量时,可先将洁净干燥的小烧杯放在称盘中央,显示数字稳定后按归零键,再缓缓加样品至所需质量时,停止加样,读数记录。
②试求氨基磺酸粗品的纯度:
③若以酚酞为指示剂,用
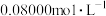 的NaOH标准溶液进行滴定,也能测定氨基磺酸粗品的纯度,但测得结果通常比
的NaOH标准溶液进行滴定,也能测定氨基磺酸粗品的纯度,但测得结果通常比 法
法
您最近一年使用:0次



