名校
1 . 化合物F是一种重要的医药中间体,可通过以下路线合成:
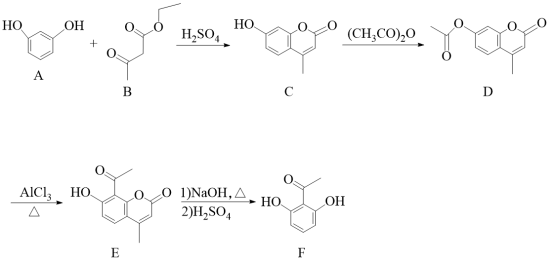
已知:①苯环取代定位规则:苯环上连有羟基时,新引入的基团主要进入羟基的邻位或对位
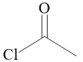
②傅克酰基化反应: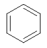 +
+ 

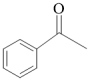 +HCl
+HCl
回答下列问题:
(1)A的化学名称为___________ ; B的官能团名称为___________ 。
(2)C生成D的化学方程式为___________ ,反应类型为___________ 。
(3)D与E的关系是___________ 。
(4)C的同分异构体中,属于萘(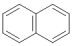 )的衍生物,且不含O—O键的共有
)的衍生物,且不含O—O键的共有___________ 种。
(5)若用A(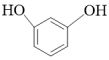 )与
)与 发生傅克酰基化反应,一取代产物是F(
发生傅克酰基化反应,一取代产物是F(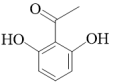 )和
)和___________ (填结构简式),但F的占比低于后者,主要原因是___________ 。
(6)以苯和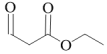 为主要原料,设计用不超过三步的反应合成香豆素(
为主要原料,设计用不超过三步的反应合成香豆素(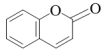 ),写出合成路线
),写出合成路线___________ 。

已知:①苯环取代定位规则:苯环上连有羟基时,新引入的基团主要进入羟基的邻位或对位
②傅克酰基化反应:
 +
+ 

 +HCl
+HCl回答下列问题:
(1)A的化学名称为
(2)C生成D的化学方程式为
(3)D与E的关系是
(4)C的同分异构体中,属于萘(
 )的衍生物,且不含O—O键的共有
)的衍生物,且不含O—O键的共有(5)若用A(
 )与
)与 发生傅克酰基化反应,一取代产物是F(
发生傅克酰基化反应,一取代产物是F( )和
)和(6)以苯和
 为主要原料,设计用不超过三步的反应合成香豆素(
为主要原料,设计用不超过三步的反应合成香豆素( ),写出合成路线
),写出合成路线
您最近一年使用:0次
2022-03-03更新
|
363次组卷
|
2卷引用:甘肃省武威市凉州区2021-2022学年高三下学期质量检测理综化学试题
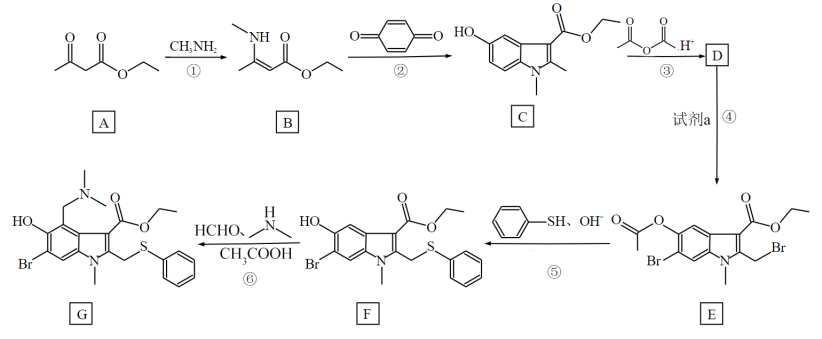
2 . 中国工程院院士、国家卫健委专家组成员李兰娟团队初步测试,在体外细胞实验中显示:阿比朵尔在10~30μmol浓度下,与药物未处理的对照组比较,能有效抑制新冠病毒达到60倍。阿比朵尔的合成路线如图:
已知: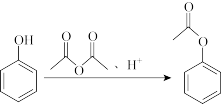 ,请回答:
,请回答:
(1)E的分子式为____ ,D的结构简式为____ 。
(2)反应①可看作分为两步进行,第一步为: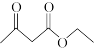 +CH3NH2→
+CH3NH2→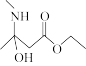 ;第二步反应的方程式为
;第二步反应的方程式为____ ,反应类型为____ 。
(3)反应③的试剂a是____ 。
(4)由C到F的过程中,设计反应③的目的是____ 。
(5)反应⑥在乙酸介质中进行,写出其化学方程式____ 。
(6)H是B的同分异构体,满足下列条件的H的结构有____ 种(不考虑立体异构)。
A.分子结构中含有五元环
B.分子结构中含有氨基(—NH2)
C.能与碳酸氢钠溶液反应产生气体
写出符合上述条件且核磁共振氢谱有五组峰的结构简式____ (只需写一种)。

已知:
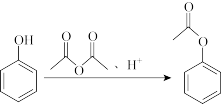 ,请回答:
,请回答:(1)E的分子式为
(2)反应①可看作分为两步进行,第一步为:
 +CH3NH2→
+CH3NH2→ ;第二步反应的方程式为
;第二步反应的方程式为(3)反应③的试剂a是
(4)由C到F的过程中,设计反应③的目的是
(5)反应⑥在乙酸介质中进行,写出其化学方程式
(6)H是B的同分异构体,满足下列条件的H的结构有
A.分子结构中含有五元环
B.分子结构中含有氨基(—NH2)
C.能与碳酸氢钠溶液反应产生气体
写出符合上述条件且核磁共振氢谱有五组峰的结构简式
您最近一年使用:0次
2022-04-20更新
|
1764次组卷
|
7卷引用:甘肃省兰州市2022届高三一诊理综化学试题
甘肃省兰州市2022届高三一诊理综化学试题(已下线)化学-2022年高考考前押题密卷(全国乙卷)(已下线)专题18有机化学基础(综合题)-2022年高考真题+模拟题汇编(全国卷)(已下线)专题19有机化学基础(选修)-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点45 有机化合物的合成-备战2023年高考化学一轮复习考点帮(全国通用)陕西省延安市第一中学2021-2022学年高二下学期期末考试化学试题(已下线)T18-有机综合题
解题方法
3 . 一种由X转化为Z的合成路线如图,下列有关化合物X、Y和Z的说法正确的是
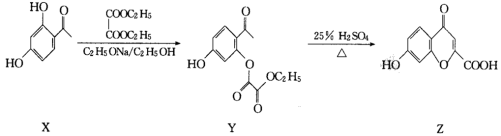

| A.Z中含有4种官能团 |
| B.Y的分子式为C11H10O6 |
| C.相同条件下,等物质的量的X、Y、Z与足量Na反应生成的气体体积之比为2:1:1 |
| D.Z既能使溴水褪色又能使酸性KMnO4溶液褪色 |
您最近一年使用:0次
2022-06-17更新
|
173次组卷
|
2卷引用:甘肃省平凉市2022届高三下学期第二次模拟考试理科综合化学试题
4 . 帕比司他是治疗某些恶性肿瘤的药物,其中间体(E)的合成路线如下:
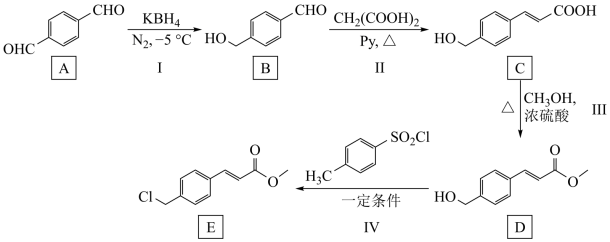
回答下列问题:
(1)A分子含有的官能团名称为_______ 。
(2)反应Ⅱ分两步进行: 。第一步反应为加成反应,则X的结构简式为
。第一步反应为加成反应,则X的结构简式为_______ ;第二步脱水的反应属于_______ (填反应类型)。
(3)若反应Ⅲ加热温度太高, 自身反应生成的副产物为
自身反应生成的副产物为_______ (填名称)。
(4)反应Ⅳ的化学方程式为_______ 。
(5)化合物Y是B的同分异构体,遇 溶液显紫色其核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。Y的结构简式为
溶液显紫色其核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。Y的结构简式为_______ 。

回答下列问题:
(1)A分子含有的官能团名称为
(2)反应Ⅱ分两步进行:
 。第一步反应为加成反应,则X的结构简式为
。第一步反应为加成反应,则X的结构简式为(3)若反应Ⅲ加热温度太高,
 自身反应生成的副产物为
自身反应生成的副产物为(4)反应Ⅳ的化学方程式为
(5)化合物Y是B的同分异构体,遇
 溶液显紫色其核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。Y的结构简式为
溶液显紫色其核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。Y的结构简式为
您最近一年使用:0次
2021-11-09更新
|
5844次组卷
|
11卷引用:甘肃省白银市白银区大成学校2021-2022学年高二下学期6月月考化学试题
甘肃省白银市白银区大成学校2021-2022学年高二下学期6月月考化学试题(已下线)专题19 有机化学基础(综合题)-三年(2020-2022)高考真题分项汇编福建省福安市第一中学2023届高三上学期第一次检测化学试题福建省连城县第一中学2022-2023学年高三上学期暑期月考化学试题福建省三明第一中学2022-2023学年高三上学期期中考试化学试题2021年新高考福建化学高考真题重庆市缙云教育联盟2021-2022学年高二11月质量检测化学试题(已下线)专题21 有机推断题(已下线)专题21 有机推断题福建省福州市福建师范大学附属中学2022-2023学年高二下学期期末化学试题福建省政和县第一中学2023-2024学年高三上学期第一次月考化学试题
名校
解题方法
5 . 习近平总书记在世界领导人气候峰会上指出,中国将在2030年前实现“碳达峰”、2060年前实现“碳中和”。这是中国基于推动构建人类命运共同体的责任担当和实现可持续发展的内在要求作出的重大战略决策。因此 的捕集、创新利用与封存成为科学家研究的重要课题。
的捕集、创新利用与封存成为科学家研究的重要课题。
(1)最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把 从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如图:
从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如图:

上述工艺中采用气液逆流接触吸收(空气从吸收池底部进入,溶液从顶部喷淋),其目的是_______ 。写出吸收池中反应的化学方程式_______ 。
(2) 和
和 合成甲烷也是
合成甲烷也是 资源化利用的重要方法。一定条件下
资源化利用的重要方法。一定条件下 催化剂可使
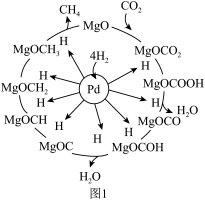
催化剂可使 “甲烷化”从而变废为宝,其反应机理如图1所示,该反应的化学方程式为
“甲烷化”从而变废为宝,其反应机理如图1所示,该反应的化学方程式为_______ ,反应过程中碳元素的化合价为-2价的中间体是_______ 。
(3)将 和
和 作为原料制造合成气的方法如下:200℃时,以镍合金为催化剂,向
作为原料制造合成气的方法如下:200℃时,以镍合金为催化剂,向 容器中通入
容器中通入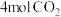 、
、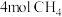 发生如下反应:
发生如下反应:
 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:
①此温度下该反应的平衡常数
_______ 。
②为了探究反应 的反应速率与浓度的关系,起始时向恒容密闭容器中通入
的反应速率与浓度的关系,起始时向恒容密闭容器中通入 与
与 ,使其物质的量浓度均为
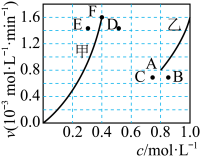
,使其物质的量浓度均为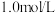 ,根据相关数据,粗略地绘制出两条速率—浓度关系曲线(如图):
,根据相关数据,粗略地绘制出两条速率—浓度关系曲线(如图):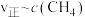 和
和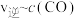 。则与
。则与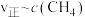 相对应曲线是图中
相对应曲线是图中_______ (填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度反应重新达到平衡,则此时 、
、 相应的平衡点分别为
相应的平衡点分别为_______ (填字母)。
 的捕集、创新利用与封存成为科学家研究的重要课题。
的捕集、创新利用与封存成为科学家研究的重要课题。(1)最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把
 从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如图:
从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如图:
上述工艺中采用气液逆流接触吸收(空气从吸收池底部进入,溶液从顶部喷淋),其目的是
(2)
 和
和 合成甲烷也是
合成甲烷也是 资源化利用的重要方法。一定条件下
资源化利用的重要方法。一定条件下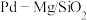 催化剂可使
催化剂可使 “甲烷化”从而变废为宝,其反应机理如图1所示,该反应的化学方程式为
“甲烷化”从而变废为宝,其反应机理如图1所示,该反应的化学方程式为
(3)将
 和
和 作为原料制造合成气的方法如下:200℃时,以镍合金为催化剂,向
作为原料制造合成气的方法如下:200℃时,以镍合金为催化剂,向 容器中通入
容器中通入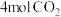 、
、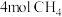 发生如下反应:
发生如下反应:
 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:| 物质 |  |  | CO |  |
| 体积分数 | 0.3 | 0.3 | 0.2 | 0.2 |

②为了探究反应
 的反应速率与浓度的关系,起始时向恒容密闭容器中通入
的反应速率与浓度的关系,起始时向恒容密闭容器中通入 与
与 ,使其物质的量浓度均为
,使其物质的量浓度均为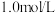 ,根据相关数据,粗略地绘制出两条速率—浓度关系曲线(如图):
,根据相关数据,粗略地绘制出两条速率—浓度关系曲线(如图):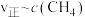 和
和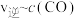 。则与
。则与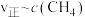 相对应曲线是图中
相对应曲线是图中 、
、 相应的平衡点分别为
相应的平衡点分别为
您最近一年使用:0次
2022-10-27更新
|
201次组卷
|
2卷引用:甘肃省平凉市第一中学2022-2023学年高二上学期第一次月考化学试题
6 . 二草酸合铜(Ⅱ)酸钾( )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸( )溶液中加入适量
)溶液中加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)由 配制Ⅰ中的
配制Ⅰ中的 溶液,下列仪器中不需要的是
溶液,下列仪器中不需要的是________ (填仪器名称)。

(2)长期存放的 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是________ 。
(3)Ⅰ中的黑色沉淀是________ (写化学式)。
(4)Ⅱ中原料配比为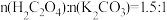 ,写出反应的化学方程式
,写出反应的化学方程式________ 。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入 应采取
应采取________ 的方法。
(6)Ⅲ中应采用________ 进行加热。
(7)Ⅳ中“一系列操作”包括________ 。
 )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:Ⅰ.取已知浓度的
 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。Ⅱ.向草酸(
 )溶液中加入适量
)溶液中加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)由
 配制Ⅰ中的
配制Ⅰ中的 溶液,下列仪器中不需要的是
溶液,下列仪器中不需要的是
(2)长期存放的
 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是(3)Ⅰ中的黑色沉淀是
(4)Ⅱ中原料配比为
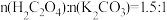 ,写出反应的化学方程式
,写出反应的化学方程式(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入
 应采取
应采取(6)Ⅲ中应采用
(7)Ⅳ中“一系列操作”包括
您最近一年使用:0次
2022-06-09更新
|
20236次组卷
|
26卷引用:甘肃省武威第十八中学2021-2022学年高二下学期期末考试化学试卷
甘肃省武威第十八中学2021-2022学年高二下学期期末考试化学试卷2022年高考全国乙卷化学真题(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国乙卷高考变式题(非选择题)(已下线)第10讲 金属材料及金属矿物的开发利用(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题14 化学实验综合题-备战2023年高考化学母题题源解密(全国通用)(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)吉林省延边第二中学2022-2023学年高三上学期开学调研考试化学试题山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题(已下线)第29讲 化学综合实验(练)-2023年高考化学一轮复习讲练测(全国通用)辽宁省名校联盟2022-2023学年高二上学期10月联考化学试题云南省临沧市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)专题27 物质制备类综合性实验题(学生版)-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 大题突破2 综合实验题题型研究(已下线)题型49 物质制备探究型综合实验(已下线)专题03 化学实验专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)湖北省武汉市第六中学2023-2024学年高三上学期第一次月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)黑龙江省哈尔滨市第三十二中学校2023-2024学年高三上学期11月期中考试化学试题(已下线)题型一 实验简答题答题规范-备战2024年高考化学答题技巧与模板构建2024届河南省郑州市第一中学高三下学期考前全真模拟考试理科综合试题-高中化学
名校
7 . 丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料,可以用有机物A和石油化工产品C、E等为原料进行合成
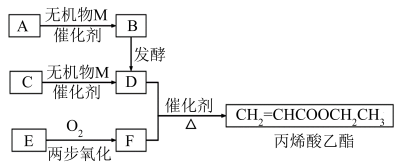
已知:A是遇碘水显蓝色的有机物;C是最简单的烯烃,其产量可以用来衡量一个国家石油化学工业的发展水平;E是C的同系物,其相对分子质量比C大14。回答下列问题
(1)①A的名称是_______ ,A的分子式为_______ 。
②E的结构简式为_______ 。
(2)C转化成D的化学方程式为_______ 。
(3)流程中C→D、D与F反应的反应类型分别是_______ 和_______ 。
(4)流程中,有机物B的结构简式为CH2OH-CHOH-CHOH-CHOH-CHOH-CHO,其所含官能团的名称是_______ 。
(5)写出丙烯酸乙酯自身发生加成聚合反应生成高聚物的化学方程式_______ 。
(6)工业上用162 t的A和足量的E为主要有机原料来生成丙烯酸乙酯,共得到100 t产品,则该生产过程的产率为_______ 。

已知:A是遇碘水显蓝色的有机物;C是最简单的烯烃,其产量可以用来衡量一个国家石油化学工业的发展水平;E是C的同系物,其相对分子质量比C大14。回答下列问题
(1)①A的名称是
②E的结构简式为
(2)C转化成D的化学方程式为
(3)流程中C→D、D与F反应的反应类型分别是
(4)流程中,有机物B的结构简式为CH2OH-CHOH-CHOH-CHOH-CHOH-CHO,其所含官能团的名称是
(5)写出丙烯酸乙酯自身发生加成聚合反应生成高聚物的化学方程式
(6)工业上用162 t的A和足量的E为主要有机原料来生成丙烯酸乙酯,共得到100 t产品,则该生产过程的产率为
您最近一年使用:0次
2021-08-17更新
|
795次组卷
|
2卷引用:甘肃省张掖市高台县第一中学2021-2022学年高一下学期6月月考化学试题



